 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Второе правило
| Если в незаполненной подоболочке атома находится не более половины максимально возможного для нее числа электронов, то J=|L-S |. Если же подоболочка заполнена более чем наполовину, то J=L+S. |
Правило Хунда является эмпирическим (то есть не выведенным из теории, а установленным экспериментально); второе правило выводится из него и из полученной выше формулы (5.19) для скалярного произведения S · L. Для облегчения применения правила Хунда полезно запомнить, что:
· надо рассматривать только незаполненную электронную подоболочку, так как моменты электронов в заполненных подоболочках взаимно компенсируются;
· значения S и L одинаковы для двух подоболочек, из которых одна имеет столько электронов, сколько не хватает для заполнения другой.
Для примера применения указанных правил рассмотрим атом серы. Его атомный номер Z=16 и, следовательно, электронная конфигурация имеет вид 1s22s22p63s23p4. Индексы справа вверху обозначают числа электронов в указанных состояниях. Видим, что незаполненной остается третья оболочка, на которой находятся четыре электрона с орбитальными моментами, равными единице. При данном L=1, согласно принципу Паули, параллельными могут быть лишь спины трех электронов, отличающихся значениями т=-1, 0,+1. Спин четвертого электрона должен быть направлен в противоположную сторону, и потому максимально возможное значение суммарного спина для данной конфигурации равно
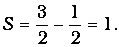
При этом значении S сумма проекций орбитальных моментов электронов с одинаково направленными спинами равна нулю, следовательно, максимально возможное значение проекции суммарного орбитального момента определяется четвертым электроном и равно единице. Поэтому L=1. Так как внешняя подоболочка заполнена более чем наполовину, то J=L+S=2. Мы пришли к выводу, что основным состоянием атома серы является 3Р2.
Для сравнения найдем основное состояние атома кремния (Z=14). От атома серы он отличается тем, что на внешней подоболочке у него находятся два, а не четыре р -электрона. Для ее заполнения не хватает четырех электронов, то есть столько, сколько их имеется у серы. Поэтому для атома кремния получаем те же значения S=1 и L=1. Внешняя подоболочка заполнена менее чем наполовину, откуда J=|L-S|=0. Поэтому основным состоянием кремния является 3Р0.
Поиск по сайту: