 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Горючее вещество – смесь газов. В состав технических газов входят метан, водород, оксид углерода, этан, бутан, пропан и другие газы
В состав технических газов входят метан, водород, оксид углерода, этан, бутан, пропан и другие газы. Количество и состав газообразных продуктов сгорания для смеси газов можно определить с помощью уравнений реакций горения входящих в смесь компонентов.
Рассмотрим порядок расчета состава и количества газообразных продуктов полного сгорания на примере светильного газа, состав которого приведен в табл. 4.7.
Таблица 4.7
Состав светильного газа
| Вещество | СО2 | СО | СН4 | Н2 |
| Содержание, объем.% |
· Запишем уравнения реакций горения входящих в смесь газов.
Горение угарного газа:
2СО+О2=2СО2.
Горение метана:
СН4+2О2=СО2+2Н2О.
Горение водорода:
2Н2+О2=2Н2О.
Углекислый газ является продуктом полного горения, поэтому для него уравнение реакции не записывается.
· Подставим в эти уравнения молекулярные массы входящих в них элементов.
Для горения угарного газа:
 .
.
Для горения метана:
 .
.
Для горения водорода:
 .
.
· Определим массу продуктов сгорания 1 кг каждого из компонентов смеси.
Для горения угарного газа:
 кг.
кг.
Для горения метана:
 кг;
кг;  кг.
кг.
Для горения водорода:
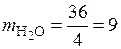 кг.
кг.
· Определим объем продуктов сгорания 1 кг каждого из компонентов по известным значениям их плотности при нормальных физических условиях.
Для горения угарного газа:
 м3.
м3.
Для горения метана:
 м3;
м3;  м3.
м3.
Для горения водорода:
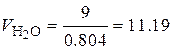 м3.
м3.
· Определим объем продуктов сгорания 1 м3 каждого из компонентов по известным значениям их плотности при нормальных физических условиях.
Для горения угарного газа (r=1.25 кг/м3):
 м3.
м3.
Для горения метана (r=0.717 кг/м3):
 м3;
м3; 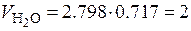 м3.
м3.
Для горения водорода (r=0.09 кг/м3):
 м3.
м3.
· Суммируя полученные объемы продуктов сгорания при горении угарного газа, метана и водорода (с учетом их процентного содержания в смеси), можно определить общее количество продуктов сгорания:
 ;
;
 .
.
Таким образом, суммарный объем продуктов сгорания
 ,
,
включая 0.05 м3 углекислого газа, содержащегося в исходной смеси.
Аналогичным способом можно рассчитать объем газообразных продуктов, образующихся при полном сгорании 1 м3 любого конкретного газа. Для некоторых распространенных газов результаты расчетов приведены в табл. 4.8.
Таблица 4.8
Состав и объем газообразных продуктов,
образующихся при полном сгорании 1 м3 газов
| Газ | Формула | СО2, м3 | Н2О, м3 | SO2, м3 |
| Водород | Н2 | — | — | |
| Оксид углерода | СО | — | — | |
| Сероводород | Н2S | — | ||
| Метан | СН4 | — | ||
| Ацетилен | С2Н2 | — | ||
| Этилен | С2Н4 | — |
С помощью табл. 4.8. можно определить как состав продуктов полного сгорания, так и их процентное содержание в любой горючей смеси, состоящей из приведенных в таблице газов.
Поиск по сайту: