 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
ХІ. 15. Реакції в розчинах
Теоретичний розгляд хімічних реакцій, що протікають у розчинах, значно складніші за реакції в газах. Це пояснюється тим, що молекули рідини знаходяться на більш близьких віддалях, коли сили взаємодії між ними не можна вважати малими або навіть відсутніми, що часто припустимо в газах. Не можна також нехтувати взаємодією молекул реагентів з молекулами розчинника, а також молекулами сторонніх речовин, що безпосередньої участі в даній реакції не беруть. Закономірності швидкостей реакцій, що експериментально спостерігаються в розчинах, неоднакові для реакцій різних типів. У деяких із них розчинник не відіграє значної ролі, в інших, навпаки, сильно впливає на швидкість реакції. Сторонні речовини прискорюють, сповільнюють або не впливають на реакцію. Швидкості реакцій у розчинах можуть сильно відрізнятись від розрахованих за теорією активних зіткнень як у той, так і інший бік. Стеричний фактор при цьому може бути як більшим, так і меншим одиниці.
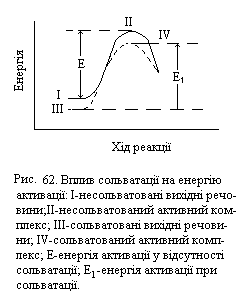 Розчинник, взаємодіячи з молекулами вихідних речовин і з активним комплексом, веде до їх сольватації. Енергія сольватованих частинок внаслідок самовільності процесу сольватації зменшується. Через це змінюється також енергія активації. Якщо сольватація вихідних частинок у порівнянні з сольватацією активного комплексу виражена сильніше, то висота енергетичного бар’єру підвищується, а швидкість реакції зменшується. При значній сольватації активного комплексу, навпаки, зменшується енергія активації (рис. 62)
Розчинник, взаємодіячи з молекулами вихідних речовин і з активним комплексом, веде до їх сольватації. Енергія сольватованих частинок внаслідок самовільності процесу сольватації зменшується. Через це змінюється також енергія активації. Якщо сольватація вихідних частинок у порівнянні з сольватацією активного комплексу виражена сильніше, то висота енергетичного бар’єру підвищується, а швидкість реакції зменшується. При значній сольватації активного комплексу, навпаки, зменшується енергія активації (рис. 62)
Для ряду мономолекулярних реакцій, що протікають у розчинах, спостерігаються майже такі ж швидкості, як і у випадку їх протікання в газовій фазі. Природа розчинника на швидкість таких реакцій впливає мало. На противагу цьому багато бімолекулярних реакцій у розчинах протікають значно швидше, ніж у газах. Швидкість таких реакцій помітно залежить від природи розчинника. Ці особливості реакцій у розчинах якісно неважко пояснити з позиції теорії активного комплексу.
Розглянемо бімолекулярну реакцію

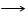 А + В (АВ) ¹ D
А + В (АВ) ¹ D
За теорією активного комплексу константа швидкості рівна
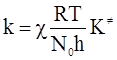 (ХІ.15.1)
(ХІ.15.1)
Через те, що термодинамічні властивості розчинів слід характеризувати не концентраціями, а активностями, вводять у це рівняння константу рівноваги К а ¹.
Враховуючи, що активність і концентрація якої-небудь речовини пов’язані співвідношенням а і = γі сі (де γі − коефіцієнт активності), одержуємо
 (ХІ.15.2)
(ХІ.15.2)
Тому
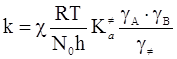 (ХІ.15.3)
(ХІ.15.3)
В ідеальній системі всі коефіцієнти активності рівні 1, значить, у цьому випадку константа швидкості
 (ХІ.15.4)
(ХІ.15.4)
Співставляючи цей вираз з попередньою формулою, одержуємо рівняння Бренстеда-Б’єрума, що зв’язує константи швидкості в реальній і ідеальній (k0) системах
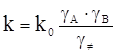 (ХІ.15.5)
(ХІ.15.5)
Вважаючи газ ідеальною системою, одержуємо константу швидкості деякої реакції в розчині в такому вигляді:
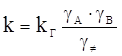 (ХІ.15.6)
(ХІ.15.6)
Приймаючи, що коефіцієнти активності вихідних речовин і активного комплексу приблизно однакові γA ≈ γB ≈ γ≠ ≈ γm, то в розчині реакція повинна протікати в γm раз швидше.
Поиск по сайту: