 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Формирование тонких слоев и покрытий электроосаждением (гальванотехника, гальваностегия, электролитическое осаждение)
К электроосаждению относятся способы получения на поверхности подложки тонких, обычно до нескольких десятков мкм, слоев металлов из растворов их солей под действием постоянного электрического тока в электролитической ячейке (Рис.2.18).
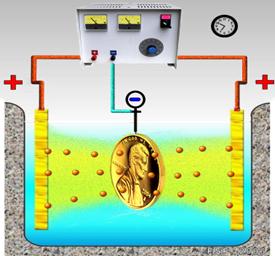
Рис.2.18. Схема электролитической ячейки.
При прохождении тока через раствор соли положительные ионы металла, образующиеся на аноде, присоединяют электроны на катоде и образуют нейтральные атомы, которые кристаллизуются и покрывают катод сплошным слоем металла. Восстановлению ионов в атомы металла предшествует их миграция (диффузия) в растворе. Катодом служит покрываемая подложка, анодом - обычно тот же металл, который выделяется на катоде. Если применяют нерастворимые аноды, в электролит периодически добавляют соединения осаждаемого металла; при этом вместо анодного растворения происходят другие анодные реакции, например, выделение О2. Эффективным средством регулирования свойств покрытия служит введение в электролит органических добавок, которые адсорбируясь на поверхности осаждаемого металла, меняют условия его кристаллизации. Многие металлы выделяются на катоде совместно с Н2, который понижает выход металла по току и изменяет свойства покрытий. Скорость выделения Н2 обычно регулируют добавлением в электролит буферных неорганических соединений. Для повышения электропроводности растворов в них дополнительно вводят неорганические соли.
Поиск по сайту: