 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Введение. Историческая справка. В 1839 г
|
Читайте также: |
Историческая справка. В 1839 г. в медных газопроводных трубах Нью-Йорка Джорж Торрей обнаружил красное порошкообразное вещество, взрывавшееся при ударе. Американец обнаружил ацетиленид меди – продукт взаимодействия ацетилена с соединениями меди, образовавшимися при окислении медной трубы.
В 1895 г. Ле-Шателье обнаружил, что ацетилен, сгорая в кислороде, дает очень горячее пламя (дл 30000С), поэтому его широко используют для сварки и резки тугоплавких металлов.
Ацетиленовые соединения последние десятилетия приобретают все большее значение. Если ранее изучался и использовался в промыш-ленности лишь один ацетилен, то сейчас синтезируются и всевозможные производные этого ряда, которые находят применение в промышленности.
Сам ацетилен широко используется для сварки и резания металлов, т.к. при горении его в кислороде развивается температура до 30000С. Из него получают как простейшие ключевые соединения основного органичес-кого синтеза (ацетальдегид, этанол, уксусная кислота, галогенпроизводные этилена, хлоруксусная кислота), так и целевую химическую продукцию – синтетические каучуки, пластмассы.
До широкого использования нефти, как дешевого сырья, ацетилен получали с помощью энергоемкого процесса через карбид кальция. В настоящее время ацетилен получают, главным образом, пиролизом легкой фракции нефти, которая раньше просто спекалась.
На основе ацетилена разработаны методы синтеза уксусного альдегида и уксусной кислоты, синтетических каучуков.
1.
|
Ацетиленовыми углеводородами (алкинами) называются углево-дороды, в молекулах которых имеется тройная связь между атомами углерода. R-C=C-R, где R=H или радикал.
Простейшим представителем ацетиленовых углеводородов является ацетилен – родоначальник гомологического ряда алкинов. Другие члены ряда можно получить, замещая атомы водорода в ацетилене на радикалы, например:
HCºCH C2H2
H3CCºCH C3H4
H3C-CºC-CH3 C4H6
H5C2-CºC-CH3 C5H8
Общая формула алкинов
С пН2п-2
Номенклатура
По рациональной номенклатуре ацетиленовые углеводороды рас-сматриваются как производные ацетилена. В названии указывается наименование радикалов, а в конце ставится слово ацетилен.
Например:
СН3 – С ºСН -метилацетилен
СН3 – СºС – СН3 - диметилацетилен
С2Н5 – СºС – СН3 - метилэтилацетилен
(СН3)2СН – СºС – СН3 - метилизопропилацетилен
Ацетиленовые углеводороды по систематической номенклатуре называют, пользуясь теми правилами, что и в случае предельных угле-водородов, но суффикс АН заменяется на ИН. Главная цепь выбирается так, чтобы в нее попала тройная связь. Место тройной связи показывают цифрой.
СН3 – СН3 - этан НС º СН этин
|
 |
 CH3-CH-CºC-C-CH3 - 2,5,5,6-тетраметилгептин-3
CH3-CH-CºC-C-CH3 - 2,5,5,6-тетраметилгептин-3
 |
CH3-CH-CºC-C-CH3 - 2,2,5-триметилгексин-3
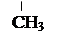 | |||
 |
Изомерия
Структурная изомерия ацетиленовых углеводородов начинается с С=4 (также,как и для алкенов).
Однако, изомеры С4Н6 могут отличаться только положением тройной связи.
СН3-СН2-СºСН - этилацетилен, бутин-1
СН3-СºС-СН3 - диметилацетилен, бутин-2
Изомерия скелета отсутствует. Последний вид структурной изомерии (т.е. изомерия скелета) начинается с С5 –три изомера.
СН3-СН2-СН2-СºСН пентин-1, пропилацетилен
СН3-СН2-СºС-СН3 пентин-2, метилэтилацетилен
В ряду ацетилена отсутствует геометрическая (цис-транс-) изомерия
Поиск по сайту: