 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Тангенциальная составляющая ускорения 12 страница
 (56.1)
(56.1)
т. е. работа, совершаемая за цикл, равна количеству полученной извне теплоты. Однако в результате кругового процесса система может теплоту как получать, так и отдавать, поэтому

где Q 1 — количество теплоты, полученное системой, Q 2 — количество теплоты, отданное системой. Поэтому термический коэффициент полезного действия для кругового процесса
 (56.2)
(56.2)

Термодинамический процесс называется обратимым, если он может происходить как в прямом, так и в обратном направлении, причем если такой процесс происходит сначала в прямом, а затем в обратном направлении и система возвращается в исходное состояние, то в окружающей среда и в этой системе не происходит никаких изменений. Всякий процесс, не удовлетворяющий этим условиям, является необратимым.
Любой равновесный процесс является обратимым. Обратимость равновесного процесса, происходящего в системе, следует из того, что се любое промежуточное состояние есть состояние термодинамического равновесия; для него «безразлично», идет процесс в прямом или обратном направлении. Реальные процессы сопровождаются диссипацией энергии (из-за трения, теплопроводности и т. д.), которая нами не обсуждается. Обратимые процессы — это идеализация реальных процессов. Их рассмотрение важно по двум причинам: 1) многие процессы в природе и технике практически обратимы; 2) обратимые процессы являются наиболее экономичными; имеют максимальный термический коэффициент полезного действия, что позволяет указать пути повышения к. п. д. реальных тепловых двигателей.
§ 57. Энтропия, ее статистическое толкование и связь с термодинамической вероятностью
Понятие энтропии введено в 1865 г. Р. Клаузиусом. Для выяснения физического содержания этого понятия рассматривают отношение теплоты Q, полученной телом в изотермическом процессе, к температуре Т теплоотдающего тела, называемое приведенным количеством теплоты.
Приведенное количество теплоты, сообщаемое телу на бесконечно малом участке процесса, равно dQ/T. Строгий теоретический анализ показывает, что приведенное количество теплоты, сообщаемое телу в любом обратимом круговом процессе, равно нулю:
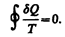 (57.1)
(57.1)
Из равенства нулю интеграла (57.1), взятого по замкнутому контуру, следует, что подынтегральное выражение dQ/T есть полный дифференциал некоторой функции, которая определяется только состоянием системы и не зависит от пути, каким система пришла в это состояние. Таким образом,
 (57.2)
(57.2)
Функция состояния, дифференциалом которой является dQ/T, называется энтропией и обозначается S.
Из формулы (57.1) следует, что для обратимых процессов изменение энтропии
 (57.3)
(57.3)
В термодинамике доказывается, что энтропия системы, совершающей необратимый цикл, возрастает:
 (57.4)
(57.4)
Выражения (57.3) и (57.4) относятся только к замкнутым системам, если же система обменивается теплотой с внешней средой, то ее энтропия может вести себя любым образом. Соотношения (57.3) и (57.4) можно представить в виде неравенства Клаузиуса
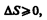 (57.5)
(57.5)
т. е. энтропия замкнутой системы может либо возрастать (в случае необратимых процессов), либо оставаться постоянной (в случае обратимых процессов).
Если система совершает равновесный переход из состояния 1 в состояние 2, то, согласно (57.2), изменение энтропии
 (57.6)
(57.6)
где подынтегральное выражение и пределы интегрирования определяются через величины, характеризующие исследуемый процесс. Формула (57.6) определяет энтропию лишь с точностью до аддитивной постоянной. Физический смысл имеет не сама энтропия, а разность энтропий.
Исходя из выражения (57.6), найдем изменение энтропии в процессах идеального газа. Taк как 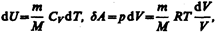 то
то

или
 (57.7)
(57.7)
т. е. изменение энтропии D S 1®2 идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида процесса перехода 1 ® 2.
Таккак для адиабатического процесса dQ = 0, то D S = 0 и, следовательно, S= const,т. е. адиабатический обратимый процесс протекает при постоянной энтропии. Поэтому его часто называют изоэнтропийным процессом. Из формулы (57.7) следует, что при изотермическом процессе (T 1= T 2)

при изохорном процессе (V 1 = V 2)

Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропий тел, входящих в систему. Свойством аддитивности обладают также внутренняя энергия, масса, объем (температура и давление таким свойством не обладают).
Более глубокий смысл энтропии вскрывается в статистической физике: энтропия связывается с термодинамической вероятностью состояния системы. Термодинамическая вероятность W состояния системы — это число способов, которыми может быть реализовано данное состояние макроскопической системы, или число микросостояний, осуществляющих данное макросостояние (по определению, W³ 1, т. е. термодинамическая вероятность не есть вероятность в математическом смысле (последняя £ 1!)).
Согласно Больцману (1872), энтропия системы и термодинамическая вероятность связаны между собой следующим образом:
 (57.8)
(57.8)
где k — постоянная Больцмана. Таким образом, энтропия определяется логарифмом числа микросостояний, с помощью которых может быть реализовано данное макросостояние. Следовательно, энтропия может рассматриваться как мера вероятности состояния термодинамической системы. Формула Больцмана (57.8) позволяет дать энтропии следующее статистическое толкование: энтропия является мерой неупорядоченности системы. В самом деле, чем больше число микросостояний, реализующих данное макросостояние, тем больше энтропия. В состоянии равновесия — наиболее вероятного состояния системы — число микросостояний максимально, при этом максимальна и энтропия.
Таккак реальные процессы необратимы, то можно утверждать, что все процессы в замкнутой системе ведут к увеличению ее энтропии — принцип возрастания энтропии. При статистическом толковании энтропии это означает, что процессы в замкнутой системе идут в направлении увеличения числа микросостояний, иными словами, от менее вероятных состояний к более вероятным, до тех пор пока вероятность состояния не станет максимальной.
Сопоставляя выражения (57.5) и (57.8), видим, что энтропия и термодинамическая вероятность состояний замкнутой системы могут либо возрастать (в случае необратимых процессов), либо оставаться постоянными (в случае обратимых процессов).
Отметим, однако, что эти утверждения имеют место для систем, состоящих из очень большого числа частиц, но могут нарушаться в системах с малым числом частиц. Для «малых» систем могут наблюдаться флуктуации, т. е. энтропия и термодинамическая вероятность состояний замкнутой системы на определенном отрезке времени могут убывать, а не возрастать, или оставаться постоянными.
§ 58. Второе начало термодинамики
Первое начало термодинамики, выражая закон сохранения и превращения энергии, не позволяет установить направление протекания термодинамических процессов. Кроме того, можно представить множество процессов, не противоречащих первому началу, в которых энергия сохраняется, а в природе они не осуществляются. Появление второго начала термодинамики связано с необходимостью дать ответ на вопрос, какие процессы в природе возможны, а какие нет. Второе начало термодинамики определяет направление протекания термодинамических процессов.
Используя понятие энтропии и неравенство Клаузиуса (см. § 57), второе начало термодинамики можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает.

Можно дать более краткую формулировку второго начала термодинамики: в процессах, происходящих в замкнутой системе, энтропия не убывает. Здесь существенно, что речь идет о замкнутых системах, так как в незамкнутых системах энтропия может вести себя любым образом (убывать, возрастать, оставаться постоянной). Кроме того, отметим еще раз, что энтропия остается постоянной в замкнутой системе только при обратимых процессах. При необратимых процессах в замкнутой системе энтропия всегда возрастает.
Формула Больцмана (57.8) позволяет объяснить постулируемое вторым началом термодинамики возрастание энтропии в замкнутой системе при необратимых процессах: возрастание энтропии означает переход системы из менее вероятных в более вероятные состояния. Таким образом, формула Больцмана позволяет дать статистическое толкование второго начала термодинамики. Оно, являясь статистическим законом, описывает закономерности хаотического движения большого числа частиц, составляющих замкнутую систему.
Укажем еще две формулировки второго начала термодинамики:
1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Можно довольно просто доказать (предоставим это читателю) эквивалентность формулировок Кельвина и Клаузиуса. Кроме того, показано, что если в замкнутой системе провести воображаемый процесс, противоречащий второму началу термодинамики в формулировке Клаузиуса, то он сопровождается уменьшением энтропии. Это же доказывает эквивалентность формулировки Клаузиуса (а следовательно, и Кельвина) и статистической формулировки, согласно которой энтропия замкнутой системы не может убывать.
В середине XIX в. возникла проблема так называемой тепловой смерти Вселенной. Рассматривая Вселенную как замкнутую систему и применяя к ней второе качало термодинамики, Клаузиус свел его содержание к утверждению, что энтропия Вселенной должна достигнуть своего максимума. Это означает, что со временем все формы движения должны перейти в тепловую. Переход же теплоты от горячих тел к холодным приведет к тому, что температура всех тел во Вселенной сравняется, т. е. наступит полное тепловое равновесие и все процессы во Вселенной прекратятся — наступит тепловая смерть Вселенной. Ошибочность вывода о тепловой смерти заключается в том, что бессмысленно применять второе начало термодинамики к незамкнутым системам, например к такой безграничной и бесконечно развивающейся системе, как Вселенная.
Первые два начала термодинамики дают недостаточно сведений о поведении термодинамических систем при нуле Кельвина. Они дополняются третьим началом термодинамика, или теоремой Нернста* — Планка: энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Кельвина:
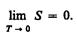
*В. Ф. Г. Нернст(1864—1941) — немецкий физик и химик.
Так как энтропия определяется с точностью до аддитивной постоянной, то эту постоянную удобно взять равной нулю. Отметим, однако, что это произвольное допущение, поскольку энтропия по своей сущности всегда определяется с точностью до аддитивной постоянной. Из теоремы Нернста — Планка следует, что теплоемкости Ср и СV при 0 К равны нулю.
§ 59. Тепловые двигатели и холодильные машины. Цикл Карно и его к. п. д. для идеального газа
Из формулировки второго начала термодинамики по Кельвину следует, что вечный двигатель второго рода — периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты, — невозможен. Для иллюстрации этого положения рассмотрим работу теплового двигателя (исторически второе начало термодинамики и возникло из анализа работы тепловых двигателей).
Принцип действия теплового двигателя приведен на рис. 85. От термостата* с более высокой температурой Т 1, называемого нагревателем, за цикл отнимается количество теплоты Q 1, а термостату с более низкой температурой Т 2, называемому холодильником, за цикл передается количество теплоты Q 2, при этом совершается работа А = Q 1 – Q 2.
*Термодинамическая система, которая может обмениваться теплотой с телами без изменения температуры.
Чтобы термический коэффициент полезного действия теплового двигателя (56.2) был равен 1, необходимо выполнение условия Q 2 = 0, т. е. тепловой двигатель должен иметь один источник теплоты, а это невозможно. Tax, французский физик и инженер Н. Л. С. Карно (1796 — 1832) показал, что для работы теплового двигателя необходимо не менее двух источников теплоты с различными температурами, иначе это противоречило бы второму началу термодинамики.
Двигатель второго рода, будь он возможен, был бы практически вечным. Охлаждение, например, воды океанов на 1° дало бы огромную энергию. Масса воды в Мировом океане составляет примерно 1018 т, при охлаждении которой на 1° выделилось бы примерно 1024 Дж теплоты, что эквивалентно полному сжиганию 1014 т угля. Железнодорожный состав, нагруженный этим количеством угля, растянулся бы на расстояние 1010км, что приблизительно совпадает с размерами Солнечной системы!
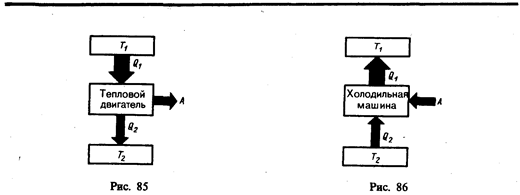
Процесс, обратный происходящему в тепловом двигателе, используется в холодильной машине, принцип действия которой представлен на рис. 86. Системой за цикл от термостата с более низкой температурой Т 2 отнимается количество теплоты Q 2 и отдается термостату с более высокой температурой Т 1 количество теплоты Q 1. Для кругового процесса, согласно (56.1), Q=A, но, по условию, Q = Q 2 – Q 1< 0, поэтому А< 0 и Q 2 – Q 1= –А, или Q 1 = Q 2 + A, т. е. количество теплоты Q 1, отданное системой источнику теплоты при более высокой температуре T 1 больше количества теплоты Q 2, полученного от источника теплоты при более низкой температуре T 2, на величину работы, совершенной над системой. Следовательно, без совершения работы нельзя отбирать теплоту от менее нагретого тела и отдавать ее более нагретому. Это утверждение есть не что иное, как второе начало термодинамики в формулировке Клаузиуса.
Однако второе начало термодинамики не следует представлять так, что оно совсем запрещает переход теплоты от менее нагретого тела к более нагретому. Ведь именно такой переход осуществляется в холодильной машине. Но при этом надо помнить, что внешние силы совершают работу над системой, т. е. этот переход не является единственным результатом процесса.
Основываясь на втором начале термодинамики, Карно вывел теорему, носящую теперь его имя: из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей (T 1) и холодильников (T 2), наибольшим к. п. д. обладают обратимые машины; при этом к. п. д. обратимых машин, работающих при одинаковых температурах нагревателей (T 1) и холодильников (T 2), равны друг другу и не зависят от природы рабочего тела (тела, совершающего круговой процесс и обменивающегося энергией с другими телами), а определяются только температурами нагревателя и холодильника.
Карно теоретически проанализировал обратимый наиболее экономичный цикл, состоящий из двух изотерм и двух адиабат. Его называют циклом Карно. Рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем.
Цикл Карно изображен на рис. 87, где изотермические расширение и сжатие заданы соответственно кривыми 1 — 2 и 3—4, а адиабатические расширение и сжатие — кривыми 2 — 3 и 4—1. При изотермическом процессе U= const, поэтому, согласно (54.4), количество теплоты Q 1, полученное газом от нагревателя, равно работе расширения А 12, совершаемой газом при переходе из состояния 1 в состояние 2:
 (59.1)
(59.1)
При адиабатическом расширении 2 — 3 теплообмен с окружающей средой отсутствует и работа расширения А 23 совершается за счет изменения внутренней энергии (см. (55.1) и (55.8)):
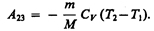

Количество теплоты Q 2, отданное газом холодильнику при изотермическом сжатии, равно работе сжатия А 34:
 (59.2)
(59.2)
Работа адиабатического сжатия
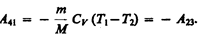
Работа, совершаемая в результате кругового процесса,

и, как можно показать, определяется площадью, заштрихованной на рис. 87. Термический к. п. д. цикла Карно, согласно (56.2),

Применив уравнение (55.5) для адиабат 2 — 3 и 4—1, получим

откуда
 (59.3)
(59.3)
Подставляя (59.1) и (59.2) в формулу (56.2) и учитывая (59.3), получаем
 (59.4)
(59.4)
т. е. для цикла Карно к. п. д. действительно определяется только температурами нагревателя и холодильника. Для его повышения необходимо увеличивать разность температур нагревателя и холодильника. Например, при T 1 = 400 К и T 2 = 300 К h = 0,25. Если же температуру нагревателя повысить на 100 К, а температуру холодильника понизить на 50 К, то h = 0,5. К. п. д. всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь гораздо меньше вычисленного для цикла Карно.
Обратный цикл Карно положен в основу действия тепловых насосов. В отличие от холодильных машин тепловые насосы должны как можно больше тепловой энергии отдавать горячему телу, например системе отопления. Часть этой энергии отбирается от окружающей среды с более низкой температурой, а часть — получается за счет механической работы, производимой, например, компрессором.
Теорема Карно послужила основанием для установления термодинамической шкалы температур. Сравнив левую и правую части формулы (59.4), получим
 (59.5)
(59.5)
т. е. для сравнения температур Т 1 и T 2 двух тел необходимо осуществить обратимый цикл Карно, в котором одно тело используется в качестве нагревателя, другое — холодильника. Из равенства (59.5) видно, что отношение температур тел равно отношению отданного в этом цикле количества теплоты к полученному. Согласно теореме Карно, химический состав рабочего тела не влияет на результаты сравнения температур, поэтому такая термодинамическая шкала не связана со свойствами какого-то определенного термометрического тела. Отметим, что практически таким образом сравнивать температуры трудно, так как реальные термодинамические процессы, как ухе указывалось, являются необратимыми.
Задачи
9.1. Азот массой 1 кг находится при температуре 280 К. Определить: 1) внутреннюю энергию молекул азота; 2) среднюю кинетическую энергию вращательного движения молекул азота. Газ считать идеальным. [1) 208 кДж; 2) 83,1 кДж]
9.2. Определить удельные теплоемкости сV и сp, некоторого двухатомного газа, если плотность этого газа при нормальных условиях 1,43 кг/м3. [ сV = 660Дж/(кг × К), сp = 910 Дж/(кг × К)]
9.3. Водород массой m = 20 г был нагрет на D T = 100 К при постоянном давлении. Определить: 1) количество теплоты Q, переданное газу; 2) приращение D U внутренней энергии газа; 3) работу А расширения. [1) 29,3 кДж; 2) 20,9 кДж; 3) 8,4 кДж]
9.4. Кислород объемом 2 л находится под давлением 1 МПа. Определить, какое количество теплоты необходимо сообщить газу, чтобы увеличить его давление вдвое в результате изохорного процесса. [5 кДж]
9.5. Некоторый газ массой 2 кг находится при температуре 300 К и под давлением 0,5 МПа. В результате изотермического сжатия давление газа увеличилось в три раза. Работа, затраченная на сжатие, A = –1,37 кДж. Определить: 1) какой это газ; 2) первоначальный удельный объем газа. [1) гелий; 2) 1,25 м3/кг]
9.6. Двухатомный идеальный газ занимает объем V 1 = 1 л и находится под давлением р 1 = 0,1 МПа. После адиабатического сжатия газ характеризуется объемом V 2 и давлением p 2. В результате последующего изохорного процесса газ охлаждается до первоначальной температуры, а его давление р 3 = 0,2 МПа. Определить: 1) объем V 2, 2) давление p 2. Представить эти процессы графически. [1) 0,5 л; 2) 0,26 МПа]
9.7. Идеальный газ количеством вещества v = 2 моль сначала изобарно нагрели так, что его объем увеличился в п = 2 раза, а затем изохорно охладили так, что давление газа уменьшилось в п = 2 раза. Определить приращение энтропии в ходе указанных процессов. [11,5 Дж/К]
9.8. Тепловая машина, совершая обратимый цикл Карно, за один цикл совершает работу 1 кДж. Температура нагревателя 400 К, а холодильника 300 К. Определить: 1) к. п. д. машины; 2) количество теплоты, получаемое машиной от нагревателя за цикл; 3) количество теплоты, отдаваемое холодильнику за цикл. [1) 25%; 2) 4 кДж; 3) 3 кДж]
9.9. Идеальный газ совершает цикл Карно, термический к. п. д. которого равен 0,3. Определить работу изотермического сжатия газа, если работа изотермического расширения составляет 300 Дж.[–210Дж]
Глава 10 Реальные газы, жидкости и твердые тела
§ 60. Силы и потенциальная энергия межмолекулярного взаимодействия
Модель идеального газа, используемая в молекулярно-кинетической теории газов, позволяет описывать поведение разреженных реальных газов при достаточно высоких температурах и низких давлеиижх. При выводе уравнения состояния идеального газа размерами молекул и их взаимодействием друг с другом пренебрегают. Повышение давления приводит к уменьшению среднего расстояния между молекулами, поэтому необходимо учитывать объем молекул и взаимодействие между ними. Taк, в 1 м3 газа при нормальных условиях содержится 2,68×1025 молекул, занимающих объем примерно 10–4 м3 (радиус молекулы примерно 10–10 м), которым по сравнению с объемом газа (1 м3) можно пренебречь. При давлении 500 МПа (1 атм = 101,3 кПа) объем молекул составит уже половину всего объема газа. Таким образом, при высоких давлениях и низких температурах указанная модель идеального газа непригодна.
При рассмотрении реальных газов — газов, свойства которых зависят от взаимодействия молекул, надо учитывать силы межмолекулярного взаимодействия. Они проявляются на расстояниях £ 10–9 м и быстро убывают при увеличении расстояния между молекулами. Такие силы называются короткодействующими.
В XX в., по мере развития представлений о строении атома и квантовой механики, было выяснено, что между молекулами вещества одновременно действуют силы притяжения и силы отталкивания. На рис. 88, а приведена качественная зависимость сил межмолекулярного взаимодействия от расстояния r между молекулами, где F о и F п — соответственно силы отталкивания и притяжения, a F — их результирующая. Силы отталкивания считаются положительными, а силы взаимного притяжения — отрицательными.
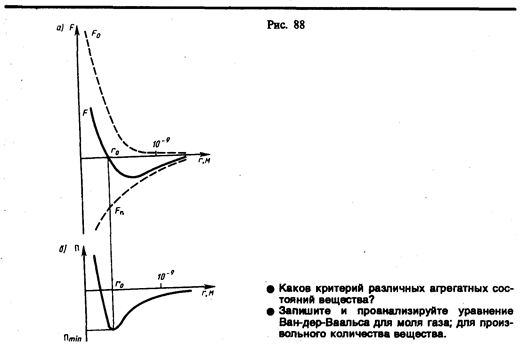
На расстоянии r=r 0 результирующая сила F = 0, т.е. силы притяжения и отталкивания уравновешивают друг друга. Таким образом, расстояние r 0 соответствует равновесному расстоянию между молекулами, на котором бы они находились в отсутствие теплового движения. При r < r 0 преобладают силы отталкивания (F> 0), при r > r 0 — силы притяжения (F <0). На расстояниях r > 10–9 м межмолекулярные силы взаимодействия практически отсутствуют (F ®0).
Элементарная работа dA силы F при увеличении расстояния между молекулами на d r совершается за счет уменьшения взаимной потенциальной энергии молекул, т. е.
 (60.1)
(60.1)
Из анализа качественной зависимости потенциальной энергии взаимодействия молекул от расстояния между ними (рис. 88, б) следует, что если молекулы находятся друг от друга на расстоянии, на котором межмолекулярные силы взаимодействия не действуют (r ®¥), то П=0. При постепенном сближении молекул между, ними появляются силы притяжения (F <0), которые совершают положительную работу (dA=F d r > 0).Тогда, согласно (60.1), потенциальная энергия взаимодействия уменьшается, достигая минимума при r = r 0. При r < r 0 с уменьшением r силы отталкивания (F >0) резко возрастают и совершаемая против них работа отрицательна (dA=F d r <0). Потенциальная энергия начинает тоже резко возрастать и становится положительной. Из данной потенциальной кривой следует, что система из двух взаимодействующих молекул в состоянии устойчивого равновесия (r = r 0) обладает минимальной потенциальной энергией.
Критерием различных агрегатных состояний вещества является соотношениемежду величинами Пmin и kT. Пmin — наименьшая потенциальная энергия взаимодействия молекул — определяет работу, которую нужно совершить против сил притяжения для того, чтобы разъединить молекулы, находящиеся в равновесии (r = r 0); kT определяет удвоенную среднюю энергию, приходящуюся на одну степень свободы хаотического (теплового) движения молекул.
Если Пmin<< kT, то вещество находится в газообразном состоянии, так как интенсивное тепловое движение молекул препятствует соединению молекул, сблизившихся до расстояния r 0, т. е. вероятность образования агрегатов из молекул достаточно мала. Если Пmin>> kT, то вещество находится в твердом состоянии, так как молекулы, притягиваясь друг к другу, не могут удалиться на значительные расстояния и колеблются около положений равновесия, определяемого расстоянием r 0. Если Пmin» kT, то вещество находится в жидком состоянии, так как в результате теплового движения молекулы перемещаются в пространстве, обмениваясь местами, но не расходясь на расстояние, превышающее r 0.
Поиск по сайту: