 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Задание. Физические свойства и химический состав подземных вод
|
Читайте также: |
Физические свойства и химический состав подземных вод
Подземные воды с гидрогеохимической точки зрения представляют собой сложнейшую систему, состав, состояние и свойства которой в каждом конкретном случае определяются:
1) свойствами самой воды;
2) свойствами содержащихся в ней веществ;
3) условиями взаимодействия их между собой и с окружающей средой.
Задание
Обработать химический анализ подземных вод для 15 варианта:
1. Пересчитать данные анализа из мольной формы (ммоль/дм3) в массовую ионную форму (мг/дм3).
2. Вычислить погрешность анализа.
3. Определить содержание анионов и катионов в процент-мольной форме (%-экв).при их сумме в 200 процентов.
4. Определить минерализацию (г/дм3).
5. Вычислить жесткость воды (ммоль/дм3).
6. Классифицировать воду по степени минерализации, по специфическим компонентам, газовому составу, агрессивности.
7. Записать анализ воды в виде формулы М.Г. Курлова, определить тип воды и дать ее название.
8. Изобразить состав воды графическим методом равносторонних треугольников Ферре.
Порядок расчета для варианта №15
Ниже приводятся подробные пояснения к расчетам по обработке результатов химического анализа подземных вод, отображенные в вышележащей таблице 2.
1. Расчет ионов из мольной формы (моль/дм3, мг-экв/л) в массовую ионную форму (мг/дм3,мг/л).
Зная содержание в воде иона в мольной форме (моль/дм3, мг-экв/л) можно определить его содержание в массовой форме (мг/дм3,мг/л).
Cl-=12*35,5=426 мг/дм3
SO42-=67*48,0=3216 мг/дм3
HCO3-=10*61= 610 мг/дм3
Na+=50*23=1150 мг/дм3
Mg2+=10*12.2=122 мг/дм3
Ca+2= 29*20,0=580 мг/дм3
К+=0*39,1= 0 мг/дм3
2. Для определения погрешности анализа воды отдельно суммируем содержание анионов и катионов в мольной (мл-эквивалентной) форме (моль/дм3, мг-экв/л). Сумма анионов равна 89 (моль/дм3, мг-экв/л), сумма катионов равна 89 (моль/дм3, мг-экв/л). Отсюда, относительная погрешность (Х) анализа равна:
 =0
=0
3. Далее выражают химический состав воды в в процент-мольной форме (%-моль, %-экв), приняв суммы анионов и катионов за 100 % каждую, и записывают по порядку в следующую графу таблицы.
Сумму анионов и катионов равную 178 (ммоль/дм3, мг-экв/л) принимают за 200 %.
Решая пропорцию, получаем значение хлора-иона в процент-мольной форме (%-экв), то есть:
Cl- = х = (12 • 200/178) =13,48 %-экв, и т.д. для всех ионов.
SO42-=(67 • 200/178)=75,3 %-экв
HCO3-=(10 • 200/178)=11,23 %-экв
Na+=(50 • 200/178)=56,18 %-экв
Mg2+=(10 • 200/178)=11,23 %-экв
Ca+2= (29• 200/178)=32,58 %-экв
К+=(0 • 200/178)=0 %-экв
4. В связи с тем, что при анализе воды сухой остаток не определялся, (то есть минерализация воды), вычисляют его приближенно. При выпаривании все не газообразные вещества, кроме гидрокарбоната-иона, переходят в сухой остаток. Гидрокарбонат-ион распадается по уравнению:

При этом в виде диоксида углерода и паров воды теряется около половины его массы (точно 0,508). Экспериментально определенный сухой остаток всегда больше вычисленного (с учетом 1/2 НСО3-), иногда на 5÷12 %.
Учитывая это, общую минерализацию (сухой остаток) приближенно вычисляют с учетом поправочного коэффициента равного 1,1 по уравнению:
 (2.8)
(2.8)
или расчетная минерализация равна:

5. Концентрация водородных ионов характеризует кислотно-щелочные свойства воды. Вода обладает общекислотной агрессией (рН = 7).
Классификация воды по общей минерализации, температуре и водородному показателю приведена в таблице 2.4.
6. Общую жесткость определяют как сумму катионов кальция и магния, выраженных в ммоль/дм3 или мг-экв/л, например:

По этому показателю данная вода классифицируется как очень жесткая (см. таблицу). Например, магнитная обработка воды резко снижает образование накипи на стенках котлов ТЭЦ.
7. В данном случае формула Курлова имеет такой вид:

В наименование состава воды включаются анионы сульфата - SO42- и катионы натрия и кальция – Na+ и Ca2+, содержание которых превышает 25 процент-молей (%-экв).
По этой записи воду следует называть: вода – железистая, углекислая, сильносолоноватая, гидрокарбонатно-натриево-кальциевая, кислая, теплая, очень жесткая. Вода высокодебитная, обладает общекислотной агрессией.
Таблица 2.4 - Классифицируемые показатели подземных вод
| Классифицируемые показатели | |||
| По минерализации | измерение | По температуре | измерение |
| г/дм3, г/л | °С | ||
| сверхпресные | < 0,2 | переохлажденные | < 0 |
| пресные | 0,2 ÷ 1 | холодные | 0 ÷ 20 |
| слабосолоноватые | 1 ÷ 3 | теплые | 20 ÷ 37 |
| сильносолоноватые | 3 ÷ 10 | горячие | 37 ÷ 50 |
| соленые | 10 ÷ 35 | весьма горячие | 50 ÷ 100 |
| рассольные | > 35 | перегретые | > 100 |
| По величине рН | измерение | По степени жесткости | измерение |
| б/р | ммоль/дм3 | ||
| очень кислые | < 5 | очень мягкие | < 1,5 |
| кислые | 5 ÷ 7 | мягкие | 1,5 ÷ 3,0 |
| нейтральные | умеренно жесткие | 3,0 ÷ 6,0 | |
| щелочные | 7 ÷ 9 | жесткие | 6,0 ÷ 9,0 |
| высокощелочные | > 9 | очень жесткие | > 9 |
Все воды, согласно классификации Алекина (см. рисунок 2.3) делятся по преобладающему аниону на три класса:
I класс – гидрокарбонатный – С – (НСО3-+CO32-), он объединяет маломинерализованные воды рек, пресных озер и немногие озера с повышенной минерализацией;
II класс – сульфатный – S – (SO42-), по распределению и минерализации занимает промежуточный характер между I и III классами;
III класс – хлоридный – C1 – (Cl-), объединяет минеральные воды морей, лиманов, реликтовых и материнских озер, подземные воды солончаковых районов, пустынь и полупустынь.
Распределение подземных вод на классы уточняется делением каждого класса на три группы по преобладанию одного из катионов: Ca2+, Mg2+, ∑Na++K+. Каждая группа подразделяется на три типа по соотношению между миллимолями ионов (ммоль/дм3).
Вывод:
Учитывая общую минерализацию, химический состав, содержание ионов водорода (рН), температуру и вычисленную жесткость, а также соотношение всех компонентов, показанных на графиках-треугольниках Ферре, окончательно дают воде наименование.
Вода - железистая, углекислая, сильносолоноватая, сульфатно-кальциево-натриевая, теплая, нейтральная, очень жесткая. Вода высокодебитная, обладает общекислотной агрессией. Вода относится к типу 2.
Итак, по классификации О.А. Алекина обозначение воды – SO42- IINаСа – класс сульфатных вод, группа кальциево-натриевая, тип второй.
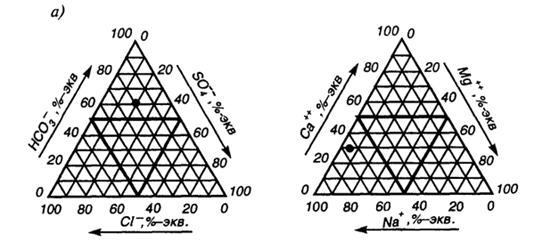
Таблица 2.3 – Физические свойства и химический состав подземной воды
| Проба воды | Глубина отбора | Запах | Мутность | Цветность | рH | Т °С | Q, м3/сут |
| 7,5 м | б/з | мутная | б/ц | 5,6 | |||
| Солевой состав | |||||||
| Компо-ненты | Единица измерения | Переводной коэффициент (см. таблицу 2.2) | |||||
| Общая минерализация | Содержание на 100 г воды | ||||||
| расчет | расчет | дано | расчет | ||||
| Ионы | тип воды | г/дм3; | мг/дм3; | ммоль/дм3; | %-моль; | Эквивалент | |
| г/л | мг/л | мг-экв/л | %-экв | ||||
| Cl- | - | - | 426,0 | 13,48 | 35,5 | ||
| SO42- | - | - | 3216,0 | 75,3 | 48,0 | ||
| HCO3- | - | - | 610,0 | 11,23 | 61,0 | ||
| Na+ | - | - | 1150,0 | 56,18 | 23,0 | ||
| Mg2+ | - | - | 122,0 | 11,23 | 12,2 | ||
| Ca2+ | - | - | 580,0 | 32,58 | 20,0 | ||
| К+ | - | - | 39,1 | ||||
| Сумма (а+к) | - | - | - | ||||
| Fe2+ | - | - | 0,03 | - | - | - | |
| NO2- | - | - | - | - | - | - | |
| CO2 | - | - | 0,15 | - | - | - | |
| М | сильно-солоноватая | 6,4 | - | - | - | - |
Примечание – Теоретически суммы анионов и катионов, выраженные в мольной форме (ммоль/дм3, мг-экв/л) должны быть равны, поэтому для определения погрешности обычно пересчитывают данные анализа из массовой ионной формы (мг/дм3, мг/л) в мольную форму (ммоль/дм3, мг-экв/л), используя пересчетные коэффициенты (таблица).
Поиск по сайту: