 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Особенности обмена углеводов
Глюкоза - главный энергетический субстрат нервной клетки. Запасы гликогена в мозге незначительны (0.1% от массы мозга). Гликоген сосредоточен, главным образом, в астроглии. Высокая потребность в энергии при низких запасах гликогена ставит нервные клетки в прямую зависимость от доставки глюкозы из крови. Из 8.9 мг глюкозы, окисленной в мозге, в сосудистое русло возвращается 1.2 мг лактата и 0.1 мг пировиноградной кислоты. Это свидетельствует о том, что основным способом окисления глюкозы является аэробное окисление. Активность гексокиназы в мозге почти в 20 раз превышает таковую в других тканях. Этот фермент прочно связан с митохондриями и в сравнении с гексокиназами мышц и печени имеет более высокое сродство к глюкозе. Подобно другим тканям, в мозге фосфофруктокиназа является основным ключевым ферментом, активность которого определяет скорость потребления глюкозы. Активаторами фермента являются фруктозо-6-фосфат, АДФ, АМФ, а ингибиторами - продукты реакции, АТФ и лимонная кислота. Перечисленные вещества позволяют осуществлять регуляцию расходования глюкозы в соответствии с метаболическими потребностями клетки.
Ферменты гликолиза расположены не только в теле нейрона, но находятся и в нервных окончаниях, где обеспечивают энергией работу синапсов. Во время роста и развития мозга довольно значительная доля глюкозы окисляется по пентозофосфатному пути. НАДФН+, образуемый в этом процессе, используется в реакциях синтеза холестерола, жирных кислот и в механизмах антиоксидантной защиты.
Потребность в глюкозе довольно высокая. В спокойном состоянии мозг потребляет около 5 мг глюкозы в мин на 100 г массы мозга. В обычных условиях эта потребность удовлетворяется, однако гипогликемия вызывает нарушения функции клеток мозга. Это выражается в потере сознания и судорогах. При голодании в первые часы происходит мобилизация глюкозы из депо, затем уровень глюкозы в крови поддерживается благодаря глюконеогенезу. В более поздние сроки (1 неделя) голодания в качестве источника энергии нервные клетки могут использовать кетоновые тела. Инсулин не оказывает прямого влияния на потребление глюкозы клетками мозга.

Особенности обмена белков и аминокислот
Поступление аминокислот из крови в клетки мозга зависит от особенностей клеток и от гемато-энцефалического барьера. Способность клеток нервной ткани к накоплению аминокислот ограничена. В мозге имеется несколько самостоятельных зависимых от ионов натрия транспортных систем для отдельных групп аминокислот: две системы для транспорта нейтральных аминокислот и отдельные системы для транспорта кислых и основных аминокислот. Преобладающими аминокислотами в клетках нервной ткани (75% от всех аминокислот) являются глутаминовая и аспарагиновая кислоты и их производные (N-ацетиласпарагиновая, глутамин, глутатион) и ГАМК. В более высокой концентрации в мозге, по сравнению с другими клетками, находятся таурин (для него даже есть специальная система транспорта), цистатионин. Некоторые аминокислоты мозга выполняют функции нейромедиаторов (глицин, глутаминовая кислота) или используются для их синтеза (тирозин - для дофамина и норадреналина, триптофан - для серотонина, глутаминовая кислота - для ГАМК).
Некоторые реакции обмена аминокислот в мозге с участием дикарбоновых аминокислот показаны на рис.18.5. Как известно, ГАМК образуется путем декарбоксилирования глутаминовой кислоты. В головном и спинном мозге она находится в больших концентрациях. ГАМК может подвергаться переаминированию с a-кетоглутаратом с образованием янтарного полуальдегида и глутаминовой кислоты. Первый окисляется до сукцината, который включается в цикл трикарбоновых кислот. Это так называемый “шунт ГАМК“. Через него проходит до 20% -кетоглутаровой кислоты мозга. Глутаминовая кислота занимает центральное место в обмене аминокислот мозга.
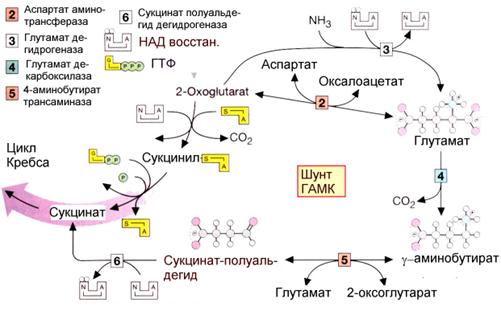
Рис. 18.5. Обмен аминокислот в мозге
В мозге открыта активность почти всех ферментов синтеза мочевины (кроме карбомоилфосфат синтетазы). Поэтому образование мочевины в мозге не происходит.
Нарушение поступления и обмена аминокислот вызывает значительные изменения функций.
Особенности образования аммиака
Аммиак образуется в мозге, главным образом, при участии аденилатдезаминазы (рис. 18.6). Атом азота аминокислоты через систему глутамат - аспартат попадает в аденилат (АМФ), который и дезаминируется. Аммиак оказывает токсическое действие на функции нейронов. Это связано с особенностями механизмов его обезвреживания в нервной ткани. Основное место в обезвреживании аммиака занимают реакции образования глютамина. В этом процессе принимают участие глутаматдегидрогеназа и глутаминсинтетаза. В качестве исходного субстрата для образования глутамина используется важный промежуточный продукт цикла трикарбоновых кислот - -кетоглутаровая кислота. Считается, что при увеличении концентрации аммиака в крови значительная часть этой кислоты используется для связывания аммиака. В результате происходит “утечка” субстратов из цикла трикарбоновых кислот. Это, в свою очередь, нарушает процессы окисления и ухудшает энергообеспеченность нервных клеток.
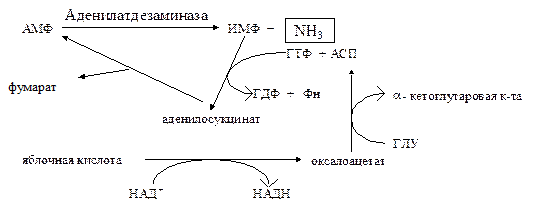
Рис.18.6. Схема образования аммиака в клетках мозга
Нервная ткань характеризуется высоким содержанием РНК и довольно большой скоростью образования этих молекул. В ткани мозга содержится полный набор ферментов синтеза de novo пуриновых нуклеотидов, а синтез de novo пиримидиновых нуклеотидов невозможен из-за отсутствия карбомоилфосфатсинтетазы. Зато нуклеозиды легко проходят гемато-энцефалический барьер и могут повторно включаться в синтез нуклеотидов. Недостаток одного из ферментов, катализирующих повторное использование нуклеозидов, приводит к тяжелому нарушению функций мозга (синдром Леш-Нихана).
Поиск по сайту: