 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
История средств защиты дыхания. Часть 2. Устройства с подачей воздуха по шлангу
Чтобы подогреть на спиртовке воду, надо выбирать
стакан из толстого стекла с целью уменьшения тепловых потерь;
стакан с тонкими стенками с целью улучшения условий передачи тепла воде, а не стеклу;
стакан со средней толщиной стенок, чтобы оптимизировать условия передачи тепла воде и уменьшения тепловых потерь.
Два сосуда одинаковых объемов доверху наполнены теплой водой. Чтобы остудить воду, первый сосуд ставят на лед, а на второй сосуд сверху кладут большой кусок льда. При этом
охлаждение будет эффективнее, если лед положить снизу, так как при этом улучшаются условия теплопередачи;
охлаждение будет эффективнее, если лед положить сверху, так как вода охлаждается быстрее при перемешивании теплых и холодных ее слоев, а чем вода холоднее, тем она тяжелее;
охлаждение в обоих сосудах будет одинаковым, так как основную роль при охлаждении играет теплопроводность, которая в обоих сосудах одинакова.
Внутреннее трение относится к явлениям переноса, потому что при этом осуществляется перенос
массы;
тепловой энергии;
импульса.
Явление диффузии характеризуется переносом
массы;
тепловой энергии;
импульса.
Явление теплопроводности характеризуется переносом
массы;
тепловой энергии;
импульса.
Коэффициент вязкости газов зависит
только от температуры;
только от давления;
от давления и температуры.
Процесс перехода жидкости в газообразное состояние называется
плавлением;
кристаллизацией;
парообразованием.
Диффузия, приводящая к выравниванию концентраций, т. е. к изменению разностей концентраций и самих концентраций компонентов, называется
стационарной диффузией;
нестационарной диффузией;
самодиффузией.
Диффузия, приводящая к частичному разделению однородной газовой смеси и превращению ее в неоднородную смесь, называется
термодиффузией;
нестационарной диффузией;
самодиффузией.
Тот факт, что ветер или буря с течением времени утихают, обусловлен явлением
диффузии;
вязкости;
теплопроводности.
ТЕСТЫ по молекулярной физике
Всего вопросов - 100
Количество вопросов в тесте – 5
Количество тем – 5
По каждой теме – 1 вопрос.
Количество баллов на один вопрос – 6.
ТЕМА 1
Какой из нижеприведённых величин соответствует выражение:
p·a·t4·v2, где: p - давление; a - ускорение; t - время; v - скорость?
удельной теплоемкости;
мощности;
+работе.
Какой из нижеприведённых величин соответствует выражение: 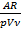 , где А – работа, R - универсальная газовая постоянная; р – давление, V – объем, ν – количество вещества?
, где А – работа, R - универсальная газовая постоянная; р – давление, V – объем, ν – количество вещества?
количеству теплоты;
+молярной теплоемкости;
удельной теплоемкости.
Какой из нижеприведённых величин соответствует выражение:  , где А – работа, R - универсальная газовая постоянная; р – давление, V – объем, ν – количество вещества, Т - температура?
, где А – работа, R - универсальная газовая постоянная; р – давление, V – объем, ν – количество вещества, Т - температура?
свободной энергии;
+энтропии;
удельной теплоемкости.
Какой из нижеприведённых величин соответствует выражение: 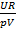 , где U – внутренняя энергия, R - универсальная газовая постоянная; р – давление, V - объем?
, где U – внутренняя энергия, R - универсальная газовая постоянная; р – давление, V - объем?
+энтропии;
количеству вещества;
удельной теплоемкости.
Какой из нижеприведённых величин соответствует выражение:
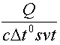 , где: Q - количество теплоты; с - удельная теплоемкость;
, где: Q - количество теплоты; с - удельная теплоемкость; 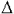 t° - изменение температуры; s - площадь; v - скорость; t - время.
t° - изменение температуры; s - площадь; v - скорость; t - время.
силе;
мощности;
+плотности.
Какой из нижеприведённых величин соответствует выражение:
 , где: c - удельная теплоёмкость;
, где: c - удельная теплоёмкость; 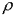 - плотность; t° - температура, l - длина; v - скорость.
- плотность; t° - температура, l - длина; v - скорость.
энергии;
+ мощности;
силе.
Какой из нижеприведённых величин соответствует выражение:
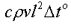 , где: c - удельная теплоёмкость;
, где: c - удельная теплоёмкость;  - плотность; t° - температура, l -длина; v - скорость?
- плотность; t° - температура, l -длина; v - скорость?
давлению;
силе;
+мощности.
Какой из нижеприведённых величин соответствует выражение:
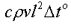 , где: c - удельная теплоёмкость;
, где: c - удельная теплоёмкость;  - плотность; t° - температура, l -длина; v - скорость?
- плотность; t° - температура, l -длина; v - скорость?
количеству теплоты;
силе;
+мощности.
Какой из нижеприведённых величин соответствует выражение:
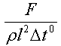 , где: F - сила;
, где: F - сила; 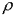 - плотность; l - длина: t°- температура.
- плотность; l - длина: t°- температура.
энергии;
+удельной теплоёмкости;
мощности.
Какой из нижеприведённых величин соответствует выражение:
 , где: F - сила;
, где: F - сила;  - плотность; l- длина: t°- температура?
- плотность; l- длина: t°- температура?
энергии;
давлению;
+удельной теплоёмкости.
Какое из нижеприведённых выражений соответствует единицам измерения удельной теплоёмкости?
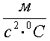
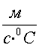
+ 
Какой из нижеприведённых величин соответствует выражение:  ,
,
где: А – работа; p - давление; a - ускорение; t - время; v - скорость.
времени;
мощности;
длине.
Какой из нижеприведённых величин соответствует выражение:
 Здесь:
Здесь: 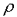 - плотность; V- объём; k - постоянная Больцмана; T - абсолютная температура; A - работа.
- плотность; V- объём; k - постоянная Больцмана; T - абсолютная температура; A - работа.
массе газа;
количеству вещества;
+молярной массе.
Какой из нижеприведённых величин соответствует выражение:
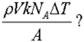 , где:
, где: 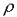 - плотность; V - объём; k - постоянная Больцмана; NA – постоянная Авогадро; T - абсолютная температура; A – работа?
- плотность; V - объём; k - постоянная Больцмана; NA – постоянная Авогадро; T - абсолютная температура; A – работа?
массе газа;
+ молярной массе;
количеству теплоты.
Какой из нижеприведенных величин соответствует выражение:
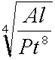 , где: А - работа, Р - давление, t - время, l - длина.
, где: А - работа, Р - давление, t - время, l - длина.
скорости;
+ускорению;
объёму.
Какой из нижеприведенных величин соответствует выражение:
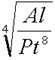 , где: А - работа, Р - давление, t - время, l – длина?
, где: А - работа, Р - давление, t - время, l – длина?
скорости;
+ ускорению;
изменению температуры.
Какая из нижеприведённых величин соответствует данному выражению
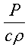 , где: Р - давление, c - удельная теплоёмкость,
, где: Р - давление, c - удельная теплоёмкость, 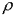 - плотность.
- плотность.
энергии;
+ температуре;
мощности.
Какой из нижеприведённых величин соответствует выражение:
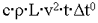 , где: с - удельная теплоемкость;
, где: с - удельная теплоемкость; 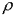 - плотность; L - длина; v - скорость; t - время;
- плотность; L - длина; v - скорость; t - время; 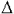 t° - изменение температуры.
t° - изменение температуры.
давлению;
+мощности;
работе.
Какой из нижеприведённых величин соответствует выражение:
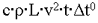 , где: с- удельная теплоемкость;
, где: с- удельная теплоемкость;  - плотность; L - длина; v - скорость; t - время;
- плотность; L - длина; v - скорость; t - время;  t° - изменение температуры?
t° - изменение температуры?
количеству теплоты;
+мощности;
плотности.
Какой из нижеприведённых величин соответствует выражение:
 , где: c - удельная теплоёмкость;
, где: c - удельная теплоёмкость; 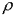 - плотность; t° - температура.
- плотность; t° - температура.
количеству теплоты;
скорости теплопередачи;
+давлению.
ТЕМА 2
На диаграмме показана зависимость работы идеального газа от его количества при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой изменения температур в указанных точках? 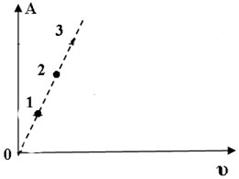
 T1 >
T1 >  T2 >
T2 >  T3;
T3;
 T1 <
T1 <  T2 <
T2 <  T3;
T3;
+  T1 =
T1 =  T2 =
T2 =  T3.
T3.
На диаграмме показана зависимость работы идеального газа от его количества при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой изменения температур в указанных точках? 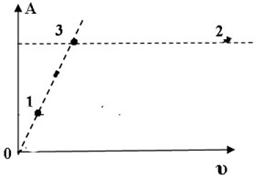
 T1 >
T1 >  T2 >
T2 >  T3;
T3;
 T1 <
T1 <  T2 <
T2 <  T3;
T3;
+  T1 =
T1 =  T3 >
T3 >  T2.
T2.
На диаграмме показана зависимость работы идеального газа от его количества при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой изменения температур в указанных точках? 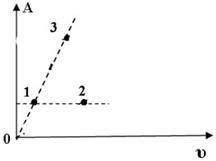
 T1 >
T1 >  T2 >
T2 >  T3;
T3;
 T1 <
T1 <  T2 <
T2 <  T3;
T3;
+  T1 =
T1 =  T3 >
T3 >  T2.
T2.
На диаграмме показана зависимость работы идеального газа от его количества при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой изменения температур в указанных точках? 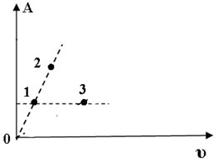
 T1 >
T1 >  T2 >
T2 >  T3;
T3;
 T1 <
T1 <  T2 <
T2 <  T3;
T3;
 T1 =
T1 =  T2>
T2>  T3.
T3.
На диаграмме показана зависимость работы идеального газа от его количества при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой изменения температур в указанных точках? 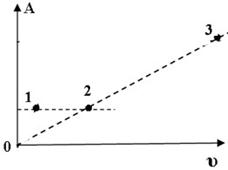
 T1 =
T1 =  T2 <
T2 <  T3;
T3;
+  T2 =
T2 =  T3 <
T3 <  T1;
T1;
 T1 <
T1 <  T2 <
T2 <  T3.
T3.
На диаграмме показана зависимость работы идеального газа от его количества при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой изменения температур в указанных точках? 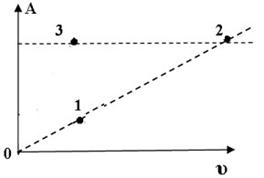
 T2 =
T2 =  T3 >
T3 >  T1;
T1;
+  T1 =
T1 =  T2 <
T2 <  T3;
T3;
 T1 =
T1 =  T3 <
T3 <  T2.
T2.
Температура двадцати молей идеального газа изменяется по закону:
T = αV2, где Т - абсолютная температура; V – объём, α = 10 К/м6. Определить работу этого газа при его расширение от 2 м3 до 4 м3.
+9972 Дж;
1662 Дж;
576Дж.
Некоторая масса идеального газа, изменяет своё давление по закону:
P=αV, где α = 1ат/м3. Определить работу внешних сил при изменении давления от 4 ат до 2ат.
6· 1010 Дж:
12 · 105 Дж;
+ 6 · 105 Дж.
Два шарика одинаковой массы — свинцовый и стальной — падают с одинаковой высоты на песок. При этом
больше нагреется тот шарик, теплоемкость материала которого меньше, т.е. свинцовый;
больше нагреется тот шарик, теплоемкость материала которого больше, т.е. стальной;
поскольку шарики падают с одинаковой высоты и массы их равны, то выделяются одинаковые количества теплоты, и температура шариков будет одинакова.
При изобарном расширении газ совершил работу в 100 Дж и изменил свою внутреннюю энергию на 150 Дж. Затем данный газ совершает изохорный переход, получая такое же количество теплоты, что и в первом переходе. Какой из нижеприведённых графиков соответствует указанным переходам? 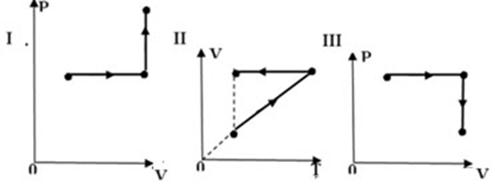
+ I;
II;
III.
При изобарном расширении газ совершил работу в 100 Дж и изменил свою внутреннюю энергию на 150 Дж. Затем данный газ совершает изохорный переход, получая такое же количество теплоты, что и в первом переходе. Чему равно изменение внутренней энергии в результате этих переходов?
100 Дж;
300 Дж;
400 Дж.
При изобарном расширении газ совершил работу в 100 Дж и изменил свою внутреннюю энергию на 150 Дж. Затем данный газ совершает изохорный переход, получая такое же количество теплоты, что и в первом переходе. Чему равно изменение внутренней энергии в результате изохорного перехода?
50 Дж;
+250 Дж;
300 Дж.
При изобарном расширении газ совершил работу в 100 Дж и изменил свою внутреннюю энергию на 150 Дж. Затем данный газ совершает изохорный переход, получая такое же количество теплоты, что и в первом переходе. Какой из нижеприведённых графиков соответствует указанным переходам? 
+I;
II;
III.
На рисунке приведён график зависимости температур трёх тел от сообщённого им количества теплоты. В каком из нижеприведённых соотношений находятся удельные теплоёмкости этих тел, если массы этих тел одинаковы? 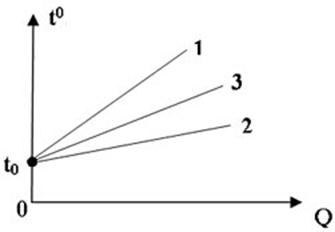
C2 < C1 < C3;
C1 > C3 > C2;
+C1 < C3 < C2.
На рисунке приведён график зависимости температур трёх тел, изготовленных из одного и того же вещества от сообщённого им количеств теплоты. В каком из нижеприведённых соотношений находятся массы этих тел? 
m3 > m1> m2
+ m1< m3 < m2;
m1> m3 > m2.
На диаграмме показана зависимость количества переданной теплоты от изменения температур для тел, изготовленных для одного и того же вещества. Какой из нижеуказанных точек, соответствует минимальная масса вещества? 
+ 1;
2;
3.
На диаграмме показана зависимость количества переданной теплоты от изменения температур для тел, изготовленных для одного и того же вещества. Какой из нижеуказанных точек, соответствует минимальная масса вещества? 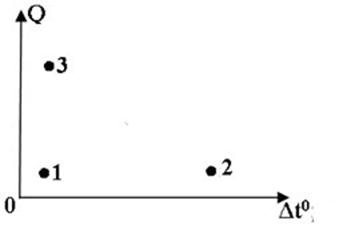
1;
+2;
3.
На диаграмме показана зависимость количества переданной теплоты от изменения температур для тел, изготовленных для одного и того же вещества. Какой из нижеуказанных точек, соответствует минимальная масса вещества? 
1;
2;
+3.
На диаграмме показана зависимость количества переданной теплоты от изменения температур для тел, изготовленных для одного и того же вещества. Какой из нижеуказанных точек, соответствует минимальная масса вещества? 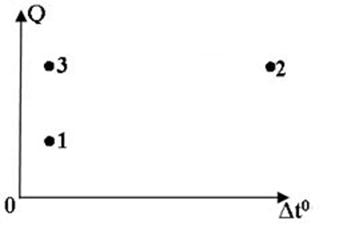
1;
+2;
3.
На диаграмме показана зависимость количества переданной теплоты от изменения температур для тел, изготовленных для одного и того же вещества. Какой из нижеуказанных точек, соответствует минимальная масса вещества? 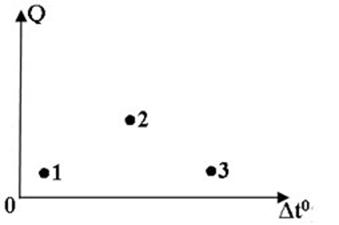
1;
2;
+ 3.
На диаграмме показана зависимость количества переданной теплоты от изменения температур для тел, изготовленных для одного и того же вещества. Какой из нижеуказанных точек, соответствует минимальная масса вещества? 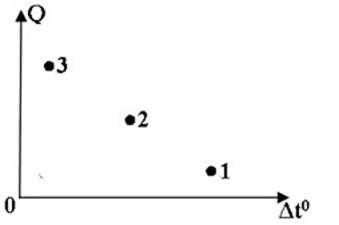
+1;
2;
3.
На рисунке представлен график зависимости температуры тела массой 100 г от количества полученной теплоты. Определить удельную теплоёмкость этого тела. 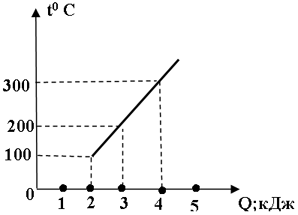
10  ;
;
+ 100  ;
;
200  .
.
На диаграмме представлены работы идеального газа при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой давления газов в этих точках? 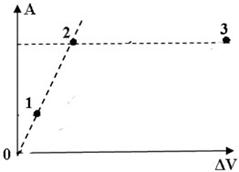
+p1 = p2 < p3;
p2 > p1 > p3;
p1 > p2 > p3.
На диаграмме представлены работы идеального газа при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой давления газов в этих точках? 
p2 > p1 > p3;
+ p1 = p2 < p3;
p1 > p2 > p3.
На диаграмме представлены работы идеального газа при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой давления газов в этих точках? 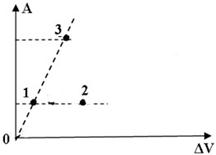
p1 = p3 < p2;
p2 > p1 > p3;
p1 > p2 > p3.
На диаграмме представлены работы идеального газа при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой давления газов в этих точках? 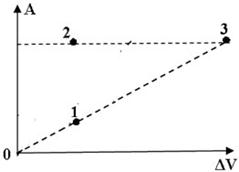
p1 = p3 < p2;
p2 < p1 < p3;
p1 = p2 > p3.
На диаграмме представлены работы идеального газа при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой давления газов в этих точках? 
p1 = p2 = p3;
+p1 > p2 > p3;
p1 < p2 < p3.
На диаграмме представлены работы идеального газа при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой давления газов в этих точках? 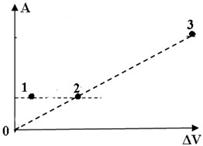
p1 = p2 < p3;
p1 < p2 < p3;
p2 = p3 < p1.
На диаграмме представлены работы идеального газа при изобарном процессе. В каком из нижеприведённых соотношений находятся между собой давления газов в этих точках? 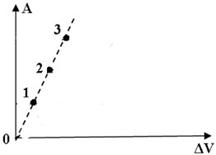
+p1 = p2 = p3;
p1 > p2 > p3;
p1 < p2 < p3.
Некоторая масса идеального газа изменяет свое состояние так, как показано на рисунке. Определить работу газа при данном процессе. 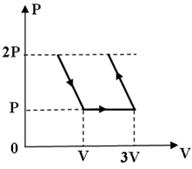
4PV;
+ 2PV
0.
ТЕМА 3
КПД идеальной тепловой машины 45%. Какова температура нагревателя, если температура холодильника 7 оС?
236 К;
+ 236 оС;
509 оС.
Какие физические параметры у двух тел должны быть разными для того, чтобы они не находились между собой в тепловом равновесии?
T, P и средняя квадратичная скорость;
Т и средняя квадратичная скорость;
+Т.
В идеальной тепловой машине за счет каждого килоджоуля энергии, получаемой от нагревателя, совершается работа в 300 Дж. КПД данной машины равен
70%;
37%;
+ 30%.
Первая теорема Карно гласит:
цикл Карно обладает наибольшим КПД по сравнению со всеми другими циклами в том же интервале температур;
+КПД идеального цикла Карно не зависит от рода рабочего тела;
для совершения полезной работы в циклической машине необходимо участие двух тел с различной температурой.
Вторая теорема Карно гласит:
+цикл Карно обладает наибольшим КПД по сравнению со всеми другими циклами в том же интервале температур;
КПД идеального цикла Карно не зависит от рода рабочего тела;
для совершения полезной работы в циклической машине необходимо участие двух тел с различной температурой.
Принцип Карно гласит:
цикл Карно обладает наибольшим КПД по сравнению со всеми другими циклами в том же интервале температур;
КПД идеального цикла Карно не зависит от рода рабочего тела;
+ для совершения полезной работы в циклической машине необходимо участие двух тел с различной температурой.
Формула 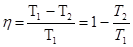 пригодна
пригодна
+только для расчёта КПД цикла Карно;
для расчета КПД любых циклов тепловых машин;
также для расчета КПД тепловой машины, работающей по циклу Дизеля.
Основное термодинамическое тождество имеет вид:
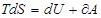 ;
;
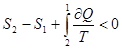 ;
;
δ Q = d U δA.
Неравенство Клаузиуса можно записать в виде:
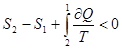 ;
;
 ;
;
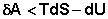 .
.
Энтропия изолированной термодинамической системы при необратимом процессе
не изменяется;
+возрастает;
уменьшается.
В изолированной термодинамической системе при любом обратимом изменении состояния её энтропия
+не изменяется;
возрастает;
уменьшается.
Если термодинамическая система не изолирована, то энтропия
всегда возрастает, так как отдает энергию окружающей среде;
всегда уменьшается, так как любая энергия стремится к состоянию с наименьшей энергией;
может как убывать, так и возрастать в зависимости от направления теплообмена.
Формулировка Клаузиуса второго начала термодинамики:
+теплота не может самопроизвольно перейти от более холодного тела к более нагретому без каких-либо других изменений в системе;
невозможно преобразовать в работу всю теплоту, взятую от тела с однородной температурой, не производя никаких других изменений в состоянии системы;
энтропия изолированной системы при реальных (необратимых) процессах всегда возрастает.
Формулировка Томсона (Кельвина) второго начала термодинамики:
теплота не может самопроизвольно перейти от более холодного тела к более нагретому без каких-либо других изменений в системе;
+невозможно преобразовать в работу всю теплоту, взятую от тела с однородной температурой, не производя никаких других изменений в состоянии системы;
энтропия изолированной системы при реальных (необратимых) процессах всегда возрастает.
Формулировка Больцмана второго начала термодинамики:
теплота не может самопроизвольно перейти от более холодного тела к более нагретому без каких-либо других изменений в системе;
невозможно преобразовать в работу всю теплоту, взятую от тела с однородной температурой, не производя никаких других изменений в состоянии системы;
энтропия изолированной системы при реальных (необратимых) процессах всегда возрастает.
Принцип Ле Шателье гласит:
+ если на систему, находящуюся в устойчивом термодинамическом равновесии, воздействуют внешние факторы, стремящиеся вывести её из этого состояния, то в системе возникают процессы, стремящиеся уничтожить изменения, вызываемые внешними воздействиями;
при всех возможных изменениях состояния системы, не влияющих на её энергию, изменение энтропии равно нулю или отрицательно;
при всех возможных изменениях состояния системы, не влияющих на её энтропию, изменение энергии равно нулю или положительно.
Одно из необходимых и достаточных условий устойчивости для изолированной термодинамической системы, сформулированных Гиббсом, гласит:
+при всех возможных изменениях состояния системы, не влияющих на её энергию, изменение энтропии равно нулю или отрицательно;
если на систему, находящуюся в устойчивом термодинамическом равновесии, воздействуют внешние факторы, стремящиеся вывести её из этого состояния, то в системе возникают процессы, стремящиеся уничтожить изменения, вызываемые внешними воздействиями;
при абсолютном нуле температуры любые изменения состояния происходят без изменения энтропии.
Одно из необходимых и достаточных условий устойчивости для изолированной термодинамической системы, сформулированных Гиббсом, гласит:
если на систему, находящуюся в устойчивом термодинамическом равновесии, воздействуют внешние факторы, стремящиеся вывести её из этого состояния, то в системе возникают процессы, стремящиеся уничтожить изменения, вызываемые внешними воздействиями;
при абсолютном нуле температуры любые изменения состояния происходят без изменения энтропии;
+при всех возможных изменениях состояния системы, не влияющих на её энтропию, изменение энергии равно нулю или положительно.
Теорема Нернста гласит:
+ при абсолютном нуле температуры любые изменения состояния происходят без изменения энтропии;
невозможно создать вечный двигатель второго рода.
при всех возможных изменениях состояния системы, не влияющих на её энергию, изменение энтропии равно нулю или отрицательно;
Под тепловой машиной понимают устройство,
в котором при подведении к газу некоторой энергии совершается работа;
+ преобразующее некоторую часть внутренней энергии рабочего тела в механическую работу;
в котором процессы преобразования теплоты в работу периодически повторяются.
Циклом Карно называется
+ цикл, при помощи которого количество теплоты, отнятое от какого-нибудь тела, можно наилучшим образом преобразовать в механическую работу;
процесс, начало и конец которого при совершении полезной работы совпадают;
цикл, в котором для совершения полезной работы необходимо участие двух тел с различной температурой.
ТЕМА 4
Отклонение свойств газа от идеальности наблюдается, если
средняя длина свободного пробега молекул сравнима с эффективным диаметром молекул;
+средняя кинетическая энергия молекул становится сравнимой с потенциальной энергией взаимодействия молекул;
среднее время свободного пробега молекул сравнимо с длительностью соударений.
В реальных газах между молекулами действуют силы, называемые
силами обменного взаимодействия;
+силами Ван-дер-Ваальса;
силами ионной связи.
Отклонение свойств газов от идеальности обусловлено
+взаимодействием Ван-дер-Ваальса;
увеличением числа взаимодействующих частиц;
конденсацией части газа.
Фазами называются.
вещества, находящиеся в разных агрегатных состояниях;
+ физически однородные части, разделённые границами, на которые распалась система;
различные состояния вещества, возникающие вследствие изменения температуры и давления.
В критическом состоянии
+ нет различия между жидким и газообразном состояниями;
изменение объема газа становится невозможным;
система стремится значительно увеличить свой обем.
В критическом состоянии
происходит переход вещества из одной фазы в другую, и появляется четкая граница раздела между ними;
+нет границы раздела между фазами;
вещество начинает оказывать сильное сопротивление изменению объёма.
При температурах выше критической
даже небольшое увенличение давления приводит к превращению газа в жидкость;
образование жидкости возможно при повышении давления выше критического;
+образование жидкости ни при каких давлениях невозможно.
Физический смысл поправки bв уравнении Ван-дер-Ваальса заключается в том, что
+ поправка на объём численно равна предельному объёму, который бы занял 1 моль реального газа при бесконечно большом давлении;
учитываются силы притяжения между молекулами газа, которые вызывают уменьшение давления на стенки сосуда;
эта поправка равна реальному физическому объему молекул газа.
Температура реального газа
меняется только при изменении его внутренней энергии;
+может меняться даже в том случае, когда его внутренняя энергия остаётся постоянной;
в отличие от идеального газа, не определяет его внутренней энергии.
Внутренняя энергия реального газа
так же, как и идеального, не зависит от его объема;
+зависит не только от температуры, но и от объёма;
не зависит ни от его температуры, ни от его объема, а определяется только его критическими параметрами.
Показатель адиабаты для реального газа
так же, как и идеального, не зависит от температуры;
так же, как и идеального, не зависит от давления;
в отличие от идеального, зависит от температуры и давления.
Процесс Джоуля-Томсона протекает
с увеличением энтальпии: H1<H 2;
с уменьшением энтальпии: H1>H 2;
+при постоянной энтальпии: H1=H 2.
Эффект Джоуля-Томсона заключается
в исчезновении границы между фазами при критической температуре;
+ в изменении температуры реального газа в результате адиабатного дросселирования;
в том, что при расширении в пустоту идеальный газ не совершает работы.
Лаборантка утром взвесила на особо точных весах открытый сосуд с только что вскипевшим маслом. К концу дня, когда масло остыло, она взвесила сосуд еще раз. Каким оказался результат взвешивания?
масса содержимого в сосуде не изменилась;
масса содержимого в сосуде уменьшилась вследствие испарения в течение дня;
+масса содержимого в сосуде увеличилась, так как при остывании масло опять поглощает молекулы воздуха, «ушедшего» из масла при кипячении.
В кастрюле с тяжелой крышкой вскипятили воду. Кастрюлю сняли с плиты, сняли крышку и в спокойную воду насыпали чайную заварку. При этом
+вода бурно закипела, так как увеличивается испарение воды изнутри вблизи возникших центров парообразования — чаинок;
испарение воды прекратилось, так как часть энергии была потрачена на нагревание чаинок;
начинается конденсация паров, находящихся над поверхностью воды, и объем воды в кастрюле увеличивается.
В стакан с сахаром и в стакан без сахара налили горячий чай из одного чайника. При этом
+сладкий чай холоднее, так как внутренняя энергия горячей воды, налитой в стакан с сахаром, частично идет на растворение сахара;
чай без сахара холоднее, так как в стакане с сахаром при растворении сахара выделяется дополнительное тепло;
температура чая в стакане не зависит от наличия сахара, а определяется только температурой чая в чайнике.
Продукты в холодильнике
+ сохнут быстрее, чем на открытом воздухе;
сохнут медленнее, чем на открытом воздухе;
сохнут с той же скоростью, как на открытом воздухе;
Какие предметы сохнут в холодильнике быстрее – холодные или теплые?
+теплые предметы сохнут быстрее, так как вода легче будет отбираться у более нагретых тел;
холодные предметы сохнут быстрее, так как часть энергии надо затратить и на их охлаждение;
холодные и теплые предметы сохнут одинаково быстро.
«Сухие» предметы охлаждаются в холодильнике
медленнее, чем «влажные», так как испарение воды из «влажных» приводит к их дополнительному охлаждению;
быстрее, чем «влажные», так как не надо тратить дополнительную энергию для их «высушивания»;
так же быстро, как влажные.
ТЕМА 5
Чтобы подогреть на спиртовке воду, надо выбирать
стакан из толстого стекла с целью уменьшения тепловых потерь;
+ стакан с тонкими стенками с целью улучшения условий передачи тепла воде, а не стеклу;
стакан со средней толщиной стенок, чтобы оптимизировать условия передачи тепла воде и уменьшения тепловых потерь.
Два сосуда одинаковых объемов доверху наполнены теплой водой. Чтобы остудить воду, первый сосуд ставят на лед, а на второй сосуд сверху кладут большой кусок льда. При этом
охлаждение будет эффективнее, если лед положить снизу, так как при этом улучшаются условия теплопередачи;
+ охлаждение будет эффективнее, если лед положить сверху, так как вода охлаждается быстрее при перемешивании теплых и холодных ее слоев, а чем вода холоднее, тем она тяжелее;
охлаждение в обоих сосудах будет одинаковым, так как основную роль при охлаждении играет теплопроводность, которая в обоих сосудах одинакова.
Внутреннее трение относится к явлениям переноса, потому что при этом осуществляется перенос
массы;
тепловой энергии;
+ импульса.
Явление диффузии характеризуется переносом
+массы;
тепловой энергии;
импульса.
Явление теплопроводности характеризуется переносом
массы;
+ тепловой энергии;
импульса.
Коэффициент вязкости газов зависит
только от температуры;
только от давления;
+ от давления и температуры.
Процесс перехода жидкости в газообразное состояние называется
плавлением;
кристаллизацией;
+ парообразованием.
Диффузия, приводящая к выравниванию концентраций, т. е. к изменению разностей концентраций и самих концентраций компонентов, называется
стационарной диффузией;
+нестационарной диффузией;
самодиффузией.
Диффузия, приводящая к частичному разделению однородной газовой смеси и превращению ее в неоднородную смесь, называется
термодиффузией;
нестационарной диффузией;
самодиффузией.
Тот факт, что ветер или буря с течением времени утихают, обусловлен явлением
диффузии;
+вязкости;
теплопроводности.
История средств защиты дыхания. Часть 2. Устройства с подачей воздуха по шлангу.
Источник: http://www33.brinkster.com/iiiii/gasmask/page.html
Поиск по сайту: