 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Состав литосферы. Формы нахождения химических элементов в земной коре
Содержание
Введение3
1 Состав литосферы. Формы нахождения химических элементов
в земной коре4
2 Факторы миграции химических элементов9
2.1 Виды миграции11
2.2 Миграция углерода19
3 Миграция токсичных элементов в литосфере 21
3.1 Миграция ртути22
3.2 Миграция алюминия23
4 Мероприятия по защите окружающей среды
от токсичных металлов24
Заключение25
Список использованной литературы26
Введение
Три наружные оболочки Земли, различающиеся фазовым состоянием, — твердая земная кора, жидкая гидросфера и газовая атмосфера — тесно связаны между собой, а вещество каждой из них проникает в пределы других. Подземные воды пронизывают верхнюю часть земной коры, значительный объем газов находится не в атмосфере, а растворен в гидросфере и заполняет пустоты в почве и горных породах. В свою очередь, вода и мелкие твердые минеральные частицы насыщают нижние слои атмосферы.
В земной коре находится основной резерв химических элементов, которые вовлекаются в миграционные процессы под воздействием живого вещества. Концентрации и распределение химических элементов в земной коре оказывают сильное влияние на состав живых организмов суши и всего живого вещества Земли [9].
Состав литосферы. Формы нахождения химических элементов в земной коре
В состав земной коры входят все известные химические элементы. Но распределены они в ней неравномерно. Наиболее распространены 8 элементов (кислород, кремний, алюминий, железо, кальций, натрий, калий, магний), которые составляют 99,03% от общего веса земной коры; на долю остальных элементов (их большинство) приходится всего 0,97%, т. е. менее 1%. В природе, благодаря геохимическим процессам нередко образуются значительные скопления какого-либо химического элемента и возникают его месторождения, а другие элементы находятся в рассеянном состоянии [7].
Из щелочных элементов наиболее широко распространены в природе натрий (2,27 мас.%) и калий (1,84 мас.%), причем благодаря высокой химической активности они встречаются исключительно в виде соединений. Основными источниками натрия и калия являются каменная соль, глауберова соль или мирабилит Na2SO4  10H2O, сильвин KCl, сильвинит KCl
10H2O, сильвин KCl, сильвинит KCl  NaCl, карналлит KCl
NaCl, карналлит KCl  MgCl2
MgCl2  6H2O и др. В отличие от натрия и калия соединения лития (
6H2O и др. В отличие от натрия и калия соединения лития ( мас.%), рубидия (
мас.%), рубидия ( мас.%) и цезия (
мас.%) и цезия ( мас.%) в природе встречаются значительно реже, поэтому эти элементы относят к числу редких и рассеянных. Хотя по содержанию в земной коре рубидий несколько опережает литий и цезий, он не образует самостоятельных минералов, а сопутствует калию, что объясняется сходством их ионных радиусов. Литий и цезий входят в состав различных силикатов и алюмосиликатов. Важнейшим минералом лития является сподумен LiAl(SiO3)2.
мас.%) в природе встречаются значительно реже, поэтому эти элементы относят к числу редких и рассеянных. Хотя по содержанию в земной коре рубидий несколько опережает литий и цезий, он не образует самостоятельных минералов, а сопутствует калию, что объясняется сходством их ионных радиусов. Литий и цезий входят в состав различных силикатов и алюмосиликатов. Важнейшим минералом лития является сподумен LiAl(SiO3)2.
Из элементов второй группы в природе наиболее распространены магний и кальций (1,4 и 1,5 мас.% соответственно). Содержание стронция ( мас.%) и бария (
мас.%) и бария ( мас.%) в земной коре на два порядка ниже. Бериллий (
мас.%) в земной коре на два порядка ниже. Бериллий ( мас.%) относят к редким элементам. Низкое содержание этого элемента в земной коре объясняется тем, что основные процессы образования химических элементов в звездах приводит к синтезу лишь нуклида 8Be, который быстро распадается на две α-частицы.
мас.%) относят к редким элементам. Низкое содержание этого элемента в земной коре объясняется тем, что основные процессы образования химических элементов в звездах приводит к синтезу лишь нуклида 8Be, который быстро распадается на две α-частицы.
Бор сравнительно мало распространен в земной коре (9*10-4мас.%), где он встречается в виде кислородных соединений: боратов и боросиликатов.
Содержание кремния в земной коре составляет по разным данным 27,6—29,5 % по массе. Чаще всего в природе кремний встречается в виде кремнезёма — соединений на основе диоксида кремния (IV) SiO2 (около 12 % массы земной коры). Основные минералы и горные породы, образуемые диоксидом кремния — это песок (речной и кварцевый), кварц и кварциты, кремень, полевые шпаты.
Алюминий по содержанию в земной коре (8,3 мас.%) занимает третье место, уступая только кислороду (45,5 мас.%) и кремнию (25,7 мас.%). Алюминий – наиболее распространенный металл, его важнейшими рудами и минералами являются бокситы Al2O3  2H2O, корунд Al2O3 и нефелин Na3K[AlSiO4]4, также он входит в состав полевых шпатов, слюд, глин и др.
2H2O, корунд Al2O3 и нефелин Na3K[AlSiO4]4, также он входит в состав полевых шпатов, слюд, глин и др.
Галлий (4,6*10-4мас.%), индий ( мас.%) и таллий (
мас.%) и таллий ( мас.%) относятся к редким элементам. Вследствие близости ионных радиусов галлий сопутствует алюминию в бокситах, а таллий – калию в алюмосиликатах.
мас.%) относятся к редким элементам. Вследствие близости ионных радиусов галлий сопутствует алюминию в бокситах, а таллий – калию в алюмосиликатах.
Углерод находится в природе в виде стабильных изотопов 12C (99,89 %) и 13С (1,11 %) и радиоактивного изотопа 14С, образующегося в верхних слоях атмосферы при взаимодействии атомов азота с нейтронами космического излучения. В природе углерод встречается в виде простых веществ (графит, алмаз, фуллерены), оксидов CO2 и СО, карбонатов СаСО3 (мрамор), MgCO3 (магнезит), FeCO3 (сидерит), ископаемого топлива (уголь, нефть, газ). Хотя по содержанию в земной коре углерод занимает 17-е место (0,048 мас.%), его доля в живых организмах значительно выше, чем в среднем в неживой природе.
Германий и олово близки по распространенности в земной коре – они занимаю 48-е и 53-е место ( и
и  мас.%, соответственно). Однако если олово встречается главным образом в виде минерала касситерита SnO2, то германий преимущественно рассеян, сопутствует сульфидным рудам, силикатам. Довольно много германия (до 1 %) содержится в некоторых сортах каменного и бурого углей.
мас.%, соответственно). Однако если олово встречается главным образом в виде минерала касситерита SnO2, то германий преимущественно рассеян, сопутствует сульфидным рудам, силикатам. Довольно много германия (до 1 %) содержится в некоторых сортах каменного и бурого углей.
Значительно большая распространенность свинца (1,3  10-4 мас.%) по сравнению с германием и оловом связана тем, что три (
10-4 мас.%) по сравнению с германием и оловом связана тем, что три (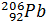 ,
,  ) из четырех его стабильных изотопов образовались как конечные продукты радиоактивного распада природных урана и тория. Только изотоп
) из четырех его стабильных изотопов образовались как конечные продукты радиоактивного распада природных урана и тория. Только изотоп  (1,4 мас.%) имеет нерадиогенное происхождение. Основная свинцовая руда – галенит PbS.
(1,4 мас.%) имеет нерадиогенное происхождение. Основная свинцовая руда – галенит PbS.
Содержание азота в земной коре составляет  мас.%
мас.%
Фосфор содержится в земной коре в виде фосфатов, на его долю приходится 0,04 % от общего числа атомов земной коры (0,1 мас.%). Мышьяк ( мас. %), а сурьма
мас. %), а сурьма 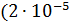 мас. %), висмут (
мас. %), висмут ( мас.%) встречаются в природе в основном в виде сульфидов: аурипигмента As2S3, реальгара As4S4, мышьякового колчедана FeAsS, а также кислородных соединений, например скородита
мас.%) встречаются в природе в основном в виде сульфидов: аурипигмента As2S3, реальгара As4S4, мышьякового колчедана FeAsS, а также кислородных соединений, например скородита  .
.
Кислород – самый распространенный элемент земной коры, на его долю приходится чуть меньше половины (49 %) от ее общей массы. Кислород входит в состав воды, кремнезема, силикатов и алюмосиликатов, известняков, мраморов, базальтов, бокситов, гематита и многих других минералов и горных пород, слагающих верхнюю оболочку Земли. Сера, селен, теллур в природе сконцентрированы в рудных месторождениях, где они связаны преимущественно с металлами. Значительная часть серы находится либо в самородном состоянии (вулканическая сера), либо в форме сульфидов и сульфитов (халькопирит CuFeS2, сфалерит ZnS, гипс  , мирабилит
, мирабилит  ).
).
Содержание фтора, хлора, брома и иода в земной коре составляет 0,06, 0,02,  мас. % соответственно.
мас. % соответственно.
Фтор встречается в природе в виде фторидов, например CaF2. Хлор встречается в природе в основном в виде хлоридов.
Гелий – второй (после водорода) элемент по распространенности во Вселенной. В то же время масса «земного» гелия составляет лишь одну миллионную массы земной коры.
Из металлов четвертой группы в природе наиболее распространен титан (0,63 мас. %), он занимает девятое место среди всех элементов. Из минералов титана наибольшее значение имеют рутил TiO2, ильменит FeTiO3, из минералов циркония – балделеит ZrO2 и циркон ZrSiO4.
Элементы пятой группы относятся к числу распространенных. По содержанию в земной коре (0,014 мас. %) ванадий занимает пятое место среди переходных элементов, уступая лишь железу, титану, марганцу и цирконию. Количество присутствующих в земной коре ниобия (0,0020 %%) и тантала (0,0017 %) сопостовимо с содержанием азота.
Ванадий, ниобий и тантал – рассеянные элементы, т.е. встречающиеся преимущественно не в форме отдельных минералов, а в виде примесей к рудам других металлов.
Элементы шестой группы относятся к четным и поэтому чаще встречаются в земной коре, чем нечетные элементы пятой и седьмой групп. Наиболее распространен в природе хром. Его содержание в земной коре составляет 0,012 мас. %. Молибден ( мас. %) и вольфрам (
мас. %) и вольфрам ( мас. %) относят к редким и рассеянным металлам. Важнейший промышленный минерал хрома – хромистый железняк FeCr2O4.Основная форма нахождения молибдена и вольфрама в природе – полевые шпаты, пироксены.
мас. %) относят к редким и рассеянным металлам. Важнейший промышленный минерал хрома – хромистый железняк FeCr2O4.Основная форма нахождения молибдена и вольфрама в природе – полевые шпаты, пироксены.
Металлы седьмой группы по распространенности резко отличаюся друг от друга. В то время как рений принадлежит к редким элементам (в земной коре его 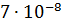 мас. %) и очень сильно рассеян, а технеций вообще не имеет стабильных изотопов, марганец, по содержанию в земной коре (0,106 мас. %) занимает двенадцатое место среди всех элементов и третье место среди переходных металлов, уступая только железу и титану. В первичных отложениях марганец встречается в силикатах и гранитах. Наиболее важны вторичные отложения, образованные пиролюзитом MnO2, гаусманнитом Mn3O4. Рений собственных месторождений не образует. Он встречается в молибдените, халькопирите и других минералах в изоморфных примесей.
мас. %) и очень сильно рассеян, а технеций вообще не имеет стабильных изотопов, марганец, по содержанию в земной коре (0,106 мас. %) занимает двенадцатое место среди всех элементов и третье место среди переходных металлов, уступая только железу и титану. В первичных отложениях марганец встречается в силикатах и гранитах. Наиболее важны вторичные отложения, образованные пиролюзитом MnO2, гаусманнитом Mn3O4. Рений собственных месторождений не образует. Он встречается в молибдените, халькопирите и других минералах в изоморфных примесей.
Среди элементов 8-10 групп по распространенности в природе безусловным лидером является железо, точнее – его изотоп 56Fe. По содержанию в земной коре железо стоит на четвертом месте (4,1 %), уступая лишь кислороду, кремнию и алюминию; никель (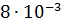 %) входит во вторую десятку, кобальт (
%) входит во вторую десятку, кобальт ( %) – в третью, а платиновые металлы относят к числу редких (Ru 10-7 %, Pt 10-7 %, Pd
%) – в третью, а платиновые металлы относят к числу редких (Ru 10-7 %, Pt 10-7 %, Pd  %, Rh
%, Rh  %, Os 10-8 %, Ir
%, Os 10-8 %, Ir  %). В земной коре железо представлено главным образом гематитом Fe2O3 (красный железняк), магнетитом Fe3O4 (магнитный железняк) и др. Земная мантия содержит значительное количество железа в форме шпинелей, силикатов, оксидов.
%). В земной коре железо представлено главным образом гематитом Fe2O3 (красный железняк), магнетитом Fe3O4 (магнитный железняк) и др. Земная мантия содержит значительное количество железа в форме шпинелей, силикатов, оксидов.
В природе медь ( мас. %), серебро (
мас. %), серебро ( мас. %) и золото (
мас. %) и золото ( мас. %) встречаются как в самородном виде, так и в виде соединений. Значительная часть меди и серебра находится в земной коре в форме сульфидов («медный блеск», или халькозин Cu2S, «серебряный блеск», или аргентит AgS, халькопирит CuFeS2). Медь также входит в состав некоторых кислородных соединений – оксидов (куприт Cu2O) и карбонатов. Золото распространено преимущественно в самородном состоянии (95 %), хотя известны и природные минералы, представляющие собой химические соединения, например калаверит AuTe2, ауростибит AuSb2.
мас. %) встречаются как в самородном виде, так и в виде соединений. Значительная часть меди и серебра находится в земной коре в форме сульфидов («медный блеск», или халькозин Cu2S, «серебряный блеск», или аргентит AgS, халькопирит CuFeS2). Медь также входит в состав некоторых кислородных соединений – оксидов (куприт Cu2O) и карбонатов. Золото распространено преимущественно в самородном состоянии (95 %), хотя известны и природные минералы, представляющие собой химические соединения, например калаверит AuTe2, ауростибит AuSb2.
Цинк, кадмий, ртуть благодаря высокому сродству к сере встречаются в земной коре преимущественно в форме сульфидов. По распространенности цинк ( %) близок к рубидию и меди. Содержание кадмия почти на три порядка ниже, чем цинка, но в два раза превышает содержание ртути.
%) близок к рубидию и меди. Содержание кадмия почти на три порядка ниже, чем цинка, но в два раза превышает содержание ртути.
Среди цинкосодержащих минералов наибольшее значение имеют сфалерит ZnS, а также вюрцит.
Кадмий – типичный редкий и рассеянный элемент. Важнейшим источником кадмия служит цинковые руды, в которых часть атомов цинка изоморфно замещена на кадмий.
Уран принадлежит к числу редких и рассеянных элементов. В земной коре его содержится около  %, т.е. больше, чем кадмия, серебра, ртути и висмута. Общие запасы урана на Земле исчисляется миллионами тонн [5].
%, т.е. больше, чем кадмия, серебра, ртути и висмута. Общие запасы урана на Земле исчисляется миллионами тонн [5].
Поиск по сайту: