 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Структура микромира
Структура атома. Идеи античных атомистов были возрождены в научном естествознании в XVIII в. английским ученым Дальтоном (1766 – 1844). К XIX в. стало ясно, что мельчайшая частица химического элемента «атом» (с греческого - «неделимый») обладает внутренней структурой, и, будучи в целом электрически нейтральной, включает компоненты с противоположным знаком электрического заряда. Отрицательно заряженная частица, входящая в состав атома - электрон, открыта в 1897 г. Дж. Дж. Томсоном (1856 – 1940). В начале XX в. английский физик Э. Резерфорд экспериментально исследовал внутреннее строение атома, используя радиоактивные α - частицы. Оказалось, что положительный заряд и основная масса атома сосредоточены в очень малом объеме - ядре (~10-15 м), в то время как размеры атома (~10-10 м) определяются электронной оболочкой. Заряды в микромире принято выражать в единицах элементарного заряда (заряда электрона) - 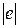 . Заряд электрона в такой системе равен (-1), протона - (+1). Исследования показали, что выраженный в таких единицах заряд ядра, а следовательно, и количество электронов в оболочке атома равны порядковому номеру химического элемента в таблице Менделеева. Периодический закон Менделеева отражает периодичность строения электронных оболочек атома и обусловленных ими химических свойств. При этом оказалось, что существуют атомы (ядра) одного элемента, обладающие разной массой. Они получили название изотопы («топ» – место). Указанное в таблице Менделеева массовое число определено для природной смеси изотопов данного элемента.
. Заряд электрона в такой системе равен (-1), протона - (+1). Исследования показали, что выраженный в таких единицах заряд ядра, а следовательно, и количество электронов в оболочке атома равны порядковому номеру химического элемента в таблице Менделеева. Периодический закон Менделеева отражает периодичность строения электронных оболочек атома и обусловленных ими химических свойств. При этом оказалось, что существуют атомы (ядра) одного элемента, обладающие разной массой. Они получили название изотопы («топ» – место). Указанное в таблице Менделеева массовое число определено для природной смеси изотопов данного элемента.
Отрицательно заряженные электроны оболочки атома движутся в электромагнитном поле, создаваемом положительно заряженным ядром и другими электронами. Учет волновых свойств электронов позволяет определить их возможные состояния и соответствующие им волновые функции. При этом, как уже отмечалось, для электрона в атоме понятие траектории неприменимо, можно говорить только о вероятности его нахождения на разных расстояниях от ядра. Энергия электрона в атоме квантована, то есть принимает определенный набор разрешенных значений. Состояние с наименьшей энергией называется основным, остальные – возбужденными. Атом может переходить в возбужденное состояние поглощая энергию электромагнитного излучения, если величина кванта соответствует разнице между разрешенными значениями энергии, т.е. если фотон имеет определенное значение частоты. Возвращаясь в основное состояние, атом испускает фотон той же частоты. Для каждого химического элемента существует свой набор (спектр) частот, испускаемых (или поглощаемых) атомами. Это позволяет, исследуя спектральный состав излучения, испускаемого веществом в атомарном состоянии, сделать выводы о его химическом составе. Спектральный анализ широко используется как в технике, так и в научных исследованиях, в частности в астрономии.
Структура атомного ядра. Структура атомных ядер была определена в 30-е годы ХХ в. Частицы, из которых состоит ядро, имеют общее название – нуклоны. Масса нуклона почти в 2000 раз больше массы электрона, и ее приближенное значение принято за атомную единицу массы (а. е. м.). В а. е. м. измеряется масса ядер. Существуют два типа нуклонов – протон и нейтрон. Протон несет положительный электрический заряд, величина которого равна элементарному, и совершенно стабилен. Нейтрон несколько тяжелее протона, электрически нейтрален и в свободном состоянии способен самопроизвольно превращаться в протон с образованием электрона и антинейтрино. Используя общепринятые обозначения частиц: протон – р, нейтрон – n, электрон – е, нейтрино – ν, фотон – γ, и обозначая заряд частицы нижним индексом, а массовое число – верхним, данное превращение можно записать следующим образом:
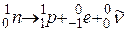 . (4.12)
. (4.12)
(Знак «~» означает, что в данной реакции возникает антинейтрино). Видно, что в этом превращении выполняются законы сохранения заряда и массового числа.
Зная порядковый номер (Z) и массовое число некоторого изотопа  , легко определить число протонов и нейтронов в нем. Очевидно, что общее число нуклонов равно А, а количество заряженных протонов – Z (заряд ядра равен порядковому номеру изотопа), следовательно, количество нейтронов равно (A – Z). Таким образом, становится ясным, что изотопы элемента, имеющие разные массы, различаются количеством нейтронов, а количество протонов для всех изотопов данного химического элемента постоянно.
, легко определить число протонов и нейтронов в нем. Очевидно, что общее число нуклонов равно А, а количество заряженных протонов – Z (заряд ядра равен порядковому номеру изотопа), следовательно, количество нейтронов равно (A – Z). Таким образом, становится ясным, что изотопы элемента, имеющие разные массы, различаются количеством нейтронов, а количество протонов для всех изотопов данного химического элемента постоянно.
Между нуклонами в ядре осуществляется электромагнитное, сильное и слабое взаимодействия. Электростатическое отталкивание одноименно заряженных протонов компенсируется не зависящим от заряда сильным (ядерным) взаимодействием между всеми нуклонами – и протонами, и нейтронами.
Чтобы разложить ядро на составляющие его нуклоны, надо затратить энергию, называемую энергией связи ядра. При образовании же ядра из нуклонов выделяется энергия, равная энергии связи. Данный процесс сопровождается уменьшением суммарной массы системы на величину, называемую дефектом массы ( m).
m).
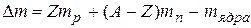 , (4.13)
, (4.13)
здесь: Z – порядковый номер элемента; А – его массовое число; mp, mn, mядра – масса соответствующих частиц.
По закону взаимосвязи массы и энергии энергия связи ядра (Есв) пропорциональна дефекту массы ( m):
m):
 . (4.14)
. (4.14)
Энергия связи, приходящаяся на один нуклон, закономерно изменяется в зависимости от массового числа, причем максимальное её значение соответствует ядрам со средними значениями атомной массы. Это делает энергетически выгодными два типа процессов – слияние легких ядер (реакции синтеза) и деление тяжелых ядер (реакции распада). В настоящее время считается, что именно реакции первого типа – слияние ядер водорода (Z = 1) с образованием ядер гелия (Z=2), протекающие в недрах звезд, являются источником их энергии, поддерживающим температуру в десятки миллионов кельвинов. Процессы деления тяжелых ядер, в частности урана и плутония, позволяют получать энергию в атомных реакторах. Исторически сложилось так, что, хотя в обоих случаях речь идет о ядерной энергии, энергию, выделяющуюся при расщеплении атомных ядер принято называть атомной энергией, а при слиянии – термоядерной. Данные процессы являются примером превращения одних изотопов в другие. До XX в. такие процессы считались невозможными, а с открытием радиоактивности их исследование стало одним из важнейших направлений в физике микромира.
Радиоактивность – самопроизвольное превращение одних изотопов в другие, сопровождающееся испусканием излучения. Это явление открыто французским ученым А. Беккерелем (1852 – 1908) в 1896 г. при изучении люминесценции солей урана. Исследование состава радиоактивного излучения, его природы, различных радиоактивных веществ проводились Пьером Кюри (1859 – 1906)и Марией Кюри-Склодовской (1867 – 1934), а также Резерфордом. Из встречающихся в природе минералов радиоактивны соединения изотопов урана, тория, радия и др. Характеристикой устойчивости изотопа относительно распада является период полураспада – время, за которое распадается половина первоначального количества ядер. Ни физические, ни химические условия не влияют на радиоактивный распад, поэтому данное явление является источником наших знаний о геологической шкале времени. Определяя процентное содержание исходных и образовавшихся ядер, можно достаточно точно определить возраст, например, горных хребтов.
Исследования радиоактивного излучения показали, что существует три вида продуктов распада, обозначаемых греческими буквами α, β и γ.
При α – распаде из атомного ядра вылетает α-частица, состоящая из двух протонов и двух нейтронов, то есть ядро гелия 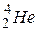 , и возникает новое ядро
, и возникает новое ядро 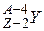 . Данный вид превращения обусловлен сильным взаимодействием и свойственен тяжелым ядрам (А>80). При β-распаде из ядра вылетает электрон, новое ядро имеет то же массовое число, но порядковый номер на единицу больше исходного
. Данный вид превращения обусловлен сильным взаимодействием и свойственен тяжелым ядрам (А>80). При β-распаде из ядра вылетает электрон, новое ядро имеет то же массовое число, но порядковый номер на единицу больше исходного 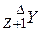 . Этот процесс интересен появлением в результате распада ядра частицы, в нем не содержащейся. Теорию β-распада создал итальянский ученый Ферми. Оказалось, что β-распад обусловлен взаимными превращениями протонов и нейтронов, вызванным слабым взаимодействием. Примером такого превращения является рассмотренный ранее распад свободного нейтрона (3.12). Изучение закономерностей β-распада привело к гипотезе о существовании нейтральной частицы с нулевой массой – нейтрино, которая возникает одновременно с электроном. Экспериментально нейтрино было открыто в 1956 г. Для искусственных изотопов β-распад может протекать с возникновением античастицы электрона – позитрона; жесткое коротковолновое электромагнитное излучение, то есть поток фотонов большой энергии (γ- лучи) сопутствует двум выше упомянутым видам распада.
. Этот процесс интересен появлением в результате распада ядра частицы, в нем не содержащейся. Теорию β-распада создал итальянский ученый Ферми. Оказалось, что β-распад обусловлен взаимными превращениями протонов и нейтронов, вызванным слабым взаимодействием. Примером такого превращения является рассмотренный ранее распад свободного нейтрона (3.12). Изучение закономерностей β-распада привело к гипотезе о существовании нейтральной частицы с нулевой массой – нейтрино, которая возникает одновременно с электроном. Экспериментально нейтрино было открыто в 1956 г. Для искусственных изотопов β-распад может протекать с возникновением античастицы электрона – позитрона; жесткое коротковолновое электромагнитное излучение, то есть поток фотонов большой энергии (γ- лучи) сопутствует двум выше упомянутым видам распада.
Радиоактивные изотопы широко применяются в современной науке и технике прежде всего потому, что каждый из них – «меченый» атом, местонахождение которого можно определить по его излучению. Кроме того, используется проникающая и ионизирующая способности радиоактивных излучений. Наряду с радиоактивностью, реакциями распада и синтеза к ядерным превращениям относятся и различные ядерные реакции, протекающие при взаимодействии ядра с элементарными частицами и другими ядрами. Таким образом, атомы одного элемента могут превращаться в атомы другого. Эти процессы происходят как самопроизвольно (радиоактивность), так и искусственным путем посредством различных ядерных реакций. Следует отметить, что в данных процессах всегда выполняются как фундаментальные законы сохранения, так и законы сохранения, специфичные для микромира.
Классификация элементарных частиц. Нуклоны (протоны и нейтроны), электроны, нейтрино, фотоны являются элементарными частицами. Их элементарность заключается не в простоте или отсутствии структуры, а в том, что из них «построен» весь материальный мир и их невозможно разбить на более мелкие свободно существующие составляющие. К элементарным относится и множество других частиц –гипероны, мюоны и т.д., которые существуют в свободном состоянии, возникают при ядерных реакциях, доходят до нас в составе космических лучей, но более сложных структур (подобных атомам) не образуют. Элементарные частицы разнообразны по массе, заряду, времени жизни, другим специфическим параметрам, не свойственным макротелам. В настоящее время принята следующая их классификация.
Частицы, участвующие в сильном взаимодействии, образуют класс адронов. В него входят мезоны, обладающие целым спином, т.е. бозоны (например, пионы)и барионы, имеющие полуцелый спин, т.е. фермионы (например, нуклоны). Адроны участвуют в сильном, слабом, гравитационном и электромагнитном взаимодействиях. Согласно описанной выше модели, адроны имеют внутреннюю структуру и состоят из кварков. Все многообразие адронов (более трехсот) формируется комбинациями шести кварков (и шести антикварков), находящихся в различных квантовых состояниях. Мезоны строятся из двух кварков, барионы - из трех. Кварки нельзя выделить как свободные частицы, но именно они считаются мельчайшими структурными составляющими адронов.
Второй класс частиц – лептоны. Лептоны не участвуют в сильном взаимодействии и в современых теориях считаются бесструктурными. К ним относятся также шесть частиц: электрон и электронное нейтрино, мюон и мюонное нейтрино, таон и таонное нейтрино. Соответственно для каждой из этих частиц существует античастица.
Третий класс составляют частицы – переносчики фундаментальных взаимодействий: глюоны, фотоны, промежуточные бозоны, гравитоны (последние экспериментально пока не обнаружены
Поиск по сайту: