 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
І. 1. Системи, стани
Будь-яке тіло чи група тіл, що складаються з великого числа частинок і виділені з навколишнього середовища реальними або уявними поверхнями розділу, називають термодинамічною системою або просто системою. Наприклад, рідина і пар в ректифікаційній колоні, розчин в колбі, вода і шматки льоду в посудині, стиснутий газ під поршнем тощо.
Стан системи повністю визначається, якщо задані параметри стану (об’єм, тиск, температура, кількість і природа речовин в ній, енергія та інші).
Величини значень ряду пораметрів (вага, температура, тиск, густина та ін.) вимірюються відповідними приладами. Для інших (внутрішня енергія, ентропія і ін.) визначаються лише як похідні виміряних, або на підставі положень, що називаються першим і другим началом термодинаміки.
Сукупність всіх фізичних і хімічних властивостей називається термодинамічним станом системи (або просто станом). При зміні будь-якого числа параметрів змінюється і стан системи.
Тіла, що знаходяться поза межами термодинамічної системи, в сукупності називають навколишнім середовищем.
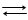 Нехай система складається із певних об’ємів газів СО і О2, що мають однакову температуру (Т), тиск (р) і розділені діафрагмою. Якщо діафрагму видалити, то гази почнуть змішуватись, і матиме місце хімічне утворення СО2, при цьому, якщо р = const, Т = const, то об’єм системи почне зменшуватись і після того, як утвориться деяка певна кількість СО2, подальша зміна об’єму системи припиниться, оскільки наступить стан хімічної рівноваги 2СО + О2 2СО2. З цього моменту стан системи буде незмінним при умові, що р і Т суміші підтримуються сталими і в навколишньому середовищі не відбувається ніяких змін.
Нехай система складається із певних об’ємів газів СО і О2, що мають однакову температуру (Т), тиск (р) і розділені діафрагмою. Якщо діафрагму видалити, то гази почнуть змішуватись, і матиме місце хімічне утворення СО2, при цьому, якщо р = const, Т = const, то об’єм системи почне зменшуватись і після того, як утвориться деяка певна кількість СО2, подальша зміна об’єму системи припиниться, оскільки наступить стан хімічної рівноваги 2СО + О2 2СО2. З цього моменту стан системи буде незмінним при умові, що р і Т суміші підтримуються сталими і в навколишньому середовищі не відбувається ніяких змін.
Стан системи, який залишається незмінним при одночасній незмінності навколишнього середовища, називається станом термодинамічної рівноваги системи. Термодинамічна система, стикаючись з навколишнім середовищем, може вступати з ним в обмін речовиною й енергією. Якщо відбуваються такі процеси, то термодинамічна система називається відкритою. Система, що не має можливості обмінюватись з навколишнім середовищем як речовиною так і енергією, називається ізольованою. Такі системи мають лише теоретичне значення. Система, яка не має можливості масообміну з навколишнім середовищем, але може обмінюватись енергією з ним, називається закритою. Система, всередині якої немає поверхні розділу між її частинами, з однаковими властивостями у всіх точках, називається гомогенною. Якщо в середині системи є така поверхня розподілу, то вона називається гетерогенною. Розрізняють також неперервні системи. В них поверхні розділу відсутні, але деякі характеристики змінюються безперервно від точки до точки. Наприклад, в металічному бруску, на кінцях якого підтримуються різні температури, встановлюється деякий градієнт температур. У вертикальному стовпі газу тиск буде наближено змінюватись зі зміною його висоти.
Хімічно індивідуальна складова частина термодинамічної системи називається компонентом. Однокомпонентні термодинамічні системи називаються простими. Наприклад, дистильована вода, чисті ртуть, азот та ін. Системи, що складаються з декількох компонентів, називають складними. Наприклад, природна питна вода, сплави, повітря та ін. Частина або сукупність частин системи з однаковими хімічними та термодинамічними властивостями, що відокремленні від інших її частин видимою поверхнею розділу, називається фазою. Система, що складається з однієї фази, називається гомогенною. Прикладами можуть бути суміш газів, ненасичений розчин, суміш нафтопродуктів та ін. Якщо система складається з двох або більшого числа фаз, то вона називається гетерогенною. Наприклад, суміш води з нафтопродуктами, рідина з паром над нею, шматки льоду і вода та ін.
Властивості системи визначаються її фізико-хімічними параметрами. Величини, що дозволяють визначити стан системи, називаються параметрами стану. Параметри стану, що піддаються безпосередньому визначенню, прийнято вважати основними. До них відносять температуру, тиск, густину, мольний (питомий) об’єм, концентрацію. Внутрішня енергія, ентальпія, ентропія і інші параметри розглядаються як функції основних. Параметри стану системи, або незалежні змінні, також ділять на дві групи. До однієї групи відносять такі параметри, які відповідають властивостям, що залежать від розмірів системи. Це екстенсивні властивості (об’єм, маса, ентропія і ін.). друга група параметрів визначає властивості, що не залежать від розмірів системи – інтенсивні властивості (температура, потенціал, тиск, мольний або питомий об’єм і т. д.).
Сукупність термодинамічних параметрів описує термодинамічний стан системи. Для однозначної характеристики стану системи немає потреби вказувати всі параметри чи навіть значну їх частину. Справа в тому, що між ними існують певні функціональні співвідношення. Тому в більшості випадків достатньо вказати деяке невелике число параметрів, а решта може бути строго визначена. В найпростішому випадку для систем, що складаються з чистої речовини відомої маси, для однозначної характеристики стану достатньо вказати всього два яких-небудь параметри. Частіше всього цю пару параметрів вибирають із трьох так званих основних параметрів – мольного об’єму v, тиску р і температури Т.
Рівняння, що встановлює зв’язок між параметрами стану системи, називається рівнянням стану. Рівняння стану системи, що знаходиться в умовах, коли ззовні на неї діють безмежно малі сили, має вигляд
f (р, V, T) = 0 (І.1.1)
Функція f є функцією стану, якщо значення цієї функції залежать лише від параметрів стану і не визначаються, зокрема, процесами, що передують цьому стану.
Поиск по сайту: