 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Розчинів електролітів
|
Читайте также: |
ХII1. Розчини електролітів
ХІІІ. 1. Електролітична дисоціація та специфіка
розчинів електролітів
Перші пояснення особливостей розчинів електролітів були дані Ареніусом у 1887 році. Основна ідея запропонованої ним теорії електролітичної дисоціації полягала в тому, що в будь-яких розчинах з достатньо високою діелектричною проникливістю молекули розчиненої речовини самочинно дисоціюють з утворенням протилежно заряджених іонів. Число іонів кожного знаку визначається стехіометричними коефіцієнтами в формулі електроліту при збереженні закону електронейтральності, у відповідності з яким сума позитивних зарядів рівна сумі негативних. Таким чином, не дивлячись на двоякість іонів, розчин електроліту залишається нейтральним.
У кристалах з іонним зв’язком іони розташовуються у вузлах кристалічної гратки. При внесенні кристалів у воду іони переходять у розчин внаслідок взаємодії кристалу з полярними молекулами води, що веде до гідратації іонів.
За сучасними уявленнями іони в розчині сольватовані, тобто оточені певним числом орієнтованих диполів розчинника, які міцно утримуються поблизу іона і беруть участь у тепловому русі разом з іоном. Такі утворення називають сольватами. При взаємодії електроліту з водою іони утворюють з молекулами води сполуки, які називають гідратами. Число молекул води, що зв’язані в гідрат-іон, називають числом гідратації; за іншою термінологією гідрат і число гідратації відповідно називають аквакомплексом і координаційним (лігандним) числом.
Катіони лужних і лужноземельних металів координують (зв’язують) молекули води в гідрати переважно за допомогою електростатичної іон-дипольної взаємодії. Останнє залежить від заряду і радіуса катіона, його маси і магнітного моменту, дипольного моменту води, поляризації іону і води і від кінетичних параметрів (імпульс, момент кількості руху тощо).Між катіонами перехідних металів і молекулами води виникає, дякуючи наявності вакантних атомних орбіталей у катіонів і неподілених пар електронів молекули води, донорно-акцепторний зв’язок. Часто електростатичний і донорно-акцепторний види зв’язку в гідраті катіона проявляються разом.
Володіючи неподільними електронними парами, аніон координує молекули води, утворюючи водневі зв’язки. Цьому сприяють акцепторні властивості молекули води, обумовлені наявністю надлишкового позитивного заряду на атомах водню. Так, у аніона Cl -, що має чотири електронні пари, чотири донорно-акцепорні зв’язки дають гідрат:

 О
О
Н Н
·
·

 · О
· О

 Н Н · · · Cl¯ · · · Н Н
Н Н · · · Cl¯ · · · Н Н
О
·
·
·

 Н Н
Н Н
О
Молекули води в гідраті іона не закріплені “намертво”: вони обмінюються з молекулами води з розчину. Методами ЯМР і ізотопного обміну визначено середній час τ перебування молекул води в гідраті (аквакомплексі катіонів). В залежності від природи катіона значення τ коливаються в досить широких межах. У лабільних аквакомплексів, наприклад, Cr 2+ і Mn 2+, він дуже малий, і, значить, обмін води протікає дуже швидко. Навпаки, в інертних аквакомплексів,, Cr 3+ і Rh 3+ обмін відбувається дуже повільно.
Середній час τ перебування молекул води в гідратах деяких катіонів при 298К такий:
Катіони τ,с Катіони τ,с
Cu2+ 0,13·10-9 Ga3+ 10-4
Cr2+ 0,14·10-9 Be2+,Ni2+ 0,33·10-4
Mn2+ 0,33·10-7 Fe3+ 0,33·10-3
Fe2+ 0,33·10-6 Al3+ ≈1
Mg2+, Ba2+,Sn2+, < 10-4 Cr3+ 0,2·107
Hg2+,Bi2+ Rh3+ 0,25·108
Сукупність взаємодій, що приводять до утворення гідрату, складає первинну гідратацію. Молекули води, що зв’язані з іоном у гідрат, утворюють першу гідратну сферу (рис.72). Електростатичне поле іона діє і на більш віддалені від нього молекули води, які входять в її квазікристалічну структуру або є вільними. Іон-дипольна взаємодія, що виникає, здатна лише орієнтувати молекули води. Ця орієнтація може порушуватись під дією полів
 інших іонів. Область часткової орієнтації в полі іона складає його другу гідратну сферу, а саму взаємодію з полярними молекулами води в другій гідратній сфері відносять до вторинної гідратації. Інколи також говорять про область неорієнтованої води, на яку не розповсюджується вплив іонів.
інших іонів. Область часткової орієнтації в полі іона складає його другу гідратну сферу, а саму взаємодію з полярними молекулами води в другій гідратній сфері відносять до вторинної гідратації. Інколи також говорять про область неорієнтованої води, на яку не розповсюджується вплив іонів.
Електроліти, молекули яких розпадаються на два іони, називаються бінарними або симетричними. Якщо при цьому утворюються однозарядні іони, то електроліт відносять до типу 1,1-зарядних електролітів (NaCl, HCl і інші). Якщо двохзарядні – до типу 2,2-зарядних (MgSO4, ZnSO4 і інші).Для несиметричних електролітів (K2SO4, MgCl2 і інші) тип електроліту встановлюється також за зарядністю іонів: K2SO4 відносять до типу 1,2-зарядних, MgCl2 – до 2,1-зарядних тощо.
Електроліти зазвичай ділять на сильні і слабі, інколи виділяють групу електролітів середньої сили. До сильних електролітів відносять речовини, які в розчинах повністю розпадаються на іони. У водних розчинах сильними електролітами є більшість мінеральних кислот, лугів, солей. До слабких електролітів відносять речовини, які в розчинах розпадаються на іони лише частково (H2CO3, H3BO3, CH3COOH, NH4OH, HgCl2 та інші). Сила електроліту залежить від природи розчинника. Одна і та ж речовина в одному розчиннику може бути сильним електролітом, а в іншому – слабким.
Розчин слабкого електроліту є сумішшю молекул розчинника, молекул і іонів електроліту. Таким чином, дисоціації піддається лише певна частина молекул електроліту. Ця частина (α) відповідає ступеню електролітичної дисоціації електроліту і рівна відношенню числа молекул, що розпались на іони (n), до загального числа (N) розчинених молекул:

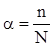 (ХІІІ.1.1.)
(ХІІІ.1.1.)
Між недисоційованими молекулами і іонами встановлюється динамічна рівновага. Ступінь електролітичної дисоціації електроліту в деякому розчиннику (при р, Т = const) залежить від природи розчиненої речовини і концентрації розчину. Ступінь дисоціації залежить і від природи розчинника. Чим вища діелектрична проникливість розчинника, тим більша ступінь дисоціації електроліту. Розчинники класифікують на невілюючі і диференціюючі. В невілюючих розчинниках розчинені речовини дисоційовані приблизно однаково і майже повністю, в диференціюючих – ступінь дисоціації електролітів різко відрізняється. Типовим невілюючим розчинником є вода, типовим диференціюючим – ацетон.
Важливою кількісною характеристикою стану електроліту в розчині є константа дисоціації (Кд). Так, для електроліту АВ, що дисоціює в розчині за схемою:
 АВ А+ + В-
АВ А+ + В-
вираз для константи дисоціації Кд має вигляд:
 (ХІІІ.1.2)
(ХІІІ.1.2)
Якщо с – концентрація електроліту, а α – ступінь дисоціації, то рівноважні концентрації частинок будуть рівні відповідно:
сА+ = с·α; сВˉ = с·α; сАВ = с(1-α) (ХІІІ.1.3)
Підставляючи ці співвідношення в рівняння (ХІІІ.1.2), отримаємо
 (ХІІІ.1.4)
(ХІІІ.1.4)
Рівняння (ХІІІ.1.4) називається законом розведення Освальда.
При невеликих значеннях α можна прийняти, що 1- α ≈ 1. Тоді рівняння (ХІІІ.1.4) переходить у
 (ХІІІ.1.5)
(ХІІІ.1.5)
Як видно, ступінь дисоціації обернено пропорційний кореню квадратному з концентрації електроліту. При зменшенні концентрації електроліту, наприклад, в 100 разів ступінь дисоціації зростає в 10 разів.
Константа дисоціації залежить від природи розчинника і температури, але не залежить від концентрації електроліту в розчині.
Теорія Арреніуса дозволила пояснити багато властивостей розчинів слабких електролітів при невеликій концентрації (реакції гідролізу, значення концентрацій водневих іонів, тощо). Проте поведінка концентрованих розчинів слабких електролітів і розчинів сильних електролітів кількісно описати з позицій цієї теорії виявилось неможливим. Користуючись теорією Арреніуса, неможливо було пояснити, наприклад, чому різні методи визначення Кд різних електролітів дають різні значення, чому для ряду електролітів Кд залежить від концентрації розчину, а також той експериментальний факт, що для деяких електролітів при високих концентраціях розчину одержувалась a >1. Теорія ж вказувала причини, що викликають дисоціацію молекул на іони, і не пояснювала, за рахунок яких сил вона відбувається.
Подальші дослідження показали, що властивості розчинів електролітів суттєво відрізняються від властивостей ідеальних розчинів, і відхилення від ідеальності в розчинах електролітів більш значні, ніж в розчинах неелектролітів тієї ж концентрації. Це пояснюється збільшенням числа частинок у розчині електроліту за рахунок дисоціації. Було знайдено, що підвищення температури кипіння, зниження температури замерзання і осмотичний тиск в розчинах електролітів значно більший, ніж в розчинах неелектролітів тієї ж концентрації. Вант-Гофф виявив, що осмотичний тиск розчинів електролітів П підкоряється рівнянню:
П = i cRT, (ХІІІ.І.6)
де і – ізотонічний коефіцієнт Вант-Гоффа (і > 1).
У водних розчинах NaCl ізотонічний коефіцієнт близький до двох, у розчинах BaCl2 – до трьох і т.д., тобто ізотонічний коефіцієнт наближено показує число іонів, на які розпадається молекула сильного електроліту.
У слабких електролітів ізотонічний коефіцієнт пов’язаний зі ступінню дисоціації a. Якщо електроліт із концентрацією с моль/л має ступінь дисоціації a і з його молекули при дисоціації утворюється n іонів, то
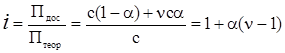 (ХІІІ.1.7)
(ХІІІ.1.7)
З рівняння (ХІІІ.1.7) випливає, що при a = 0 (розчин неелектроліту) і = 1,. а при a = 1 (розчин повністю дисоційованого електроліту) і = n. Цілочисельних значень і практично не спостерігається, оскільки, рівняння (ХІІІ.1.7) не враховує сил міжіонної взаємодії і ін. Проте при a = 0 коефіцієнт і буде близький до 1, а при a = 1 близький до числа йонів, на які розпадаються електроліти.
Класична теорія електролітичної дисоціації не розглядала взаємодію між частинками розчину електроліту, а тому не могла пояснити механізму його утворення. А між тим головною причиною утворення розчину електроліту є якраз взаємодія розчиненого електроліту з розчинником. Врахування взаємодії частинок електроліту між собою і з частинками розчинника, а також взаємодій більш складних утворень, що містять частинки розчиненої речовини і розчинника разом необхідні для пояснення більшості властивостей розчину електроліту.
З сучасної точки зору основні рівноваги, що існують у розчині електроліту при дисоціації сполуки АВ в розчиннику можна показати такою схемою:
Кнест Kд К-1ас

 АВ + nM АВМn А+с + Bc‾ Ac+Bc‾
АВ + nM АВМn А+с + Bc‾ Ac+Bc‾
Кпер
Згідно з цією схемою процесу дисоціації передує реакція сольватації, що характеризується константою нестійкості (Кнест):
 (ХІІІ.1.8)
(ХІІІ.1.8)
Оскільки в розбавленому розчині активність а м стала, то:
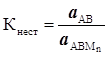 (ХІІІ.1.9)
(ХІІІ.1.9)
Продукт приєднання молекул розчинника М до молекули АВ – соль ватована молекула АВМn – дисоціює з утворенням сольватованих іонів А+с і В¯с. Цій реакції відповідає константа дисоціації:
 (ХІІІ.1.10)
(ХІІІ.1.10)
Сольватовані іони, в свою чергу, внаслідок електростатичної взаємодії об’єднуються, утворюючи іонні двійники (асоціати) А+сВ¯с. Цей процес характеризується константою асоціації:
 (ХІІІ.1.11)
(ХІІІ.1.11)
Така схема передбачає можливість прямого перетворення неіонізованого продукту АВМn в іонну пару А+сВ¯с. Цій реакції відповідає константа перетворення:
 (ХІІІ.1.12)
(ХІІІ.1.12)
Загальна константа рівноваги Кзаг подальших реакцій може бути виражена через константи окремих стадій таким чином:
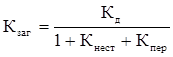 (ХІІІ.1.13)
(ХІІІ.1.13)
або
 (ХІІІ.1.14)
(ХІІІ.1.14)
Якщо розчинена речовина повністю вступає у взаємодію з розчинником, то:
 (ХІІІ.1.15)
(ХІІІ.1.15)
Про такі динамічні рівноваги в розчинах можна вести мову, якщо електроліт не є сильним. Багато експериментальних даних вказують на практично повну дисоціацію сильних електролітів.
Багаточисельні аномалії у властивостях таких електролітів і є наслідком повної дисоціації. Залежність електричної провідності, осмотичного тиску і інших властивостей розчинів сильних електролітів від концентрації насправді була пов’язана з дією міжіонних сил і сольватаційними ефектами, а не зі зміною ступеня електролітичної дисоціації.
Поиск по сайту: