 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ СТРЕПТОЦИДА»
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ СТУДЕНТАМ
ДЛЯ САМОПОДГОТОВКИ К ПРАКТИЧЕСКОМУ ЗАНЯТИЮ №16
ТЕМА 3.3.3.:«НИТРИТОМЕТРИЯ.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ СТРЕПТОЦИДА».
ЦЕЛИ ЗАНЯТИЯ:
1.Закрепить теоретические знания по методу нитритометрии;
2. Научиться проводить количественный анализ лекарственного средства (субстанции) стрептоцида методом нитритометрии;
3.Научиться выполнять расчет и делать заключение (по количественному содержанию) о качестве лекарственной субстанции.
МЕСТО ПРОВЕДЕНИЯ: лаборатория химии.
ПРОДОЛЖИТЕЛЬНОСТЬ ЗАНЯТИЯ: 90 минут
ОСНАЩЕНИЕ ЗАНЯТИЯ: Таблица «Периодическая таблица химических
элементов Д.И.Менделеева»
Исследуемое вещество: стрептоцид 0,25;
Реактивы: рабочий раствор натрия нитрита с молярной концентрацией эквивалента 0,1 моль/л; раствор хлороводородной кислоты с молярной концентрацией эквивалента 4 моль/л; индикатор тропеолин 00;калия бромид кристаллический;
Оборудование: мерные пипетки, колбы для титрования,мерные пробирки, пробирки.
ПЗ №16 ФГОС 2009 года – 2 –
К занятию студенты должны ЗНАТЬ:
1. Основные сведения о титриметрическом анализе.
2.Точка эквивалентности и способы ее фиксации. Индикаторы.
3.Требования к реакциям в титриметрическом анализе.
4.Классификация методов и способы титрования.
5. Способы выражения концентрации рабочего раствора.
Растворы с молярной концентрацией эквивалента, молярные
растворы. Титр.
6. Титрованные растворы. Растворы с титром приготовленным и
титром установленным.
7. Исходные вещества. Требования к исходным веществам.
8. Вычисления в титриметрическом анализе.
9.Понятие о поправочном коэффициенте. Способы его нахождения.
10.Теоретические основы методов окислительно-восстановительного титрования.
11. Классификация методов окислительно – восстановительного титрования.
12.Метод нитритометрии:
- рабочий раствор
- стандартный раствор
- фиксирование точки эквивалентности с помощью
внешнего и внутреннего индикаторов
- условия титрования
- примеры нитритометрического определения
ПЗ №16 ФГОС 2009 года – 3 –
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ:
1. Какой анализ называют титриметрическим?
2. Что показывает молярная концентрация эквивалента?
3. Что показывает титр раствора?
4. Что такое точка эквивалентности?
5. Как фиксируют точку эквивалентности?
6. Какие требования предъявляют к реакциям в титриметрическом анализе?
7. Какие существуют методы титриметрического анализа?
8. Какие методы называются методами оксидиметрии или окислительно - восстановительного титрования (ОВТ)?
9. Как классифицируются методы ОВТ?
10. Какой метод называется методом нитритометрии?
11. Какие вещества количественно определяют методом нитритометрии?
12. Какой рабочий раствор применяют в методе нитритометрии?
13. Какое установочное вещество используют в методе нитритометрии?
14. Перечислите индикаторы метода нитритометрии.
15. Как фиксируется точка эквивалентности в методе нитритометриипри титровании с тропеолином 00?
16. Как фиксируется точка эквивалентности при применении йодкрахмальной бумаги?
17. В какой среде проводят нитритометрические определения?
18. С какой целью применяют бромид калия?
ПЗ №16 ФГОС 2009 года – 4 –
Задания для внеаудиторной самостоятельной работы студентов:
В тетрадях по самоподготовке:
а) Напишитеуравнения реакций, лежащих в основе количественного определения стрептоцидаметодом нитритометрии. Титрование проводилось с внутренним индикатором.
Формула стрептоцида:
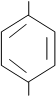 NH2
NH2
SO2NH2
б) Напишите уравнения реакций, лежащих в основе количественного определения стрептоцида методом нитритометрии. Титрование проводилось с внешним индикатором.
в) Решите задачу:
Рассчитайте титр рабочего раствора нитрита натрия с молярной концентрацией эквивалента 0,1 моль/л по стрептоциду.
Молярная масса стрептоцида 172,21 г/моль.
На занятии студенты должны:
I. Ответить на вопросы входного контроля.
II. Выполнить практическую работу
Поиск по сайту: