 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Применение первого начала термодинамики для вывода уравнения адиабатного процесса
Адиабатным называется процесс обмена теплом системой с внешней средой при условии 
Запишем первое начало термодинамики в виде
 (9.37)
(9.37)
Для одного моля получим уравнение
 (9.38)
(9.38)
Из уравнения Менделеева – Клапейрона для одного моля найдем давление
 (9.39)
(9.39)
Подставим полученное соотношение в (9.38):
 (9.40)
(9.40)
Разделим обе части уравнения на CVT, находим:
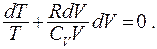
Мы получили
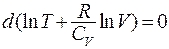 ,
,
откуда следует:
 (9.41)
(9.41)
Введем показатель адиабаты:
 (9.42)
(9.42)
Теплоемкость при постоянном объеме:
 (9.43)
(9.43)
Подставим (9.43) в (9.41):

отсюда следует

Уравнение адиабатного процесса в параметрах T,V:
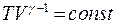 (9.44)
(9.44)
Из уравнения Менделеева – Клапейрона находим  подставим в (9.44) и получим уравнение адиабатного процесса в параметрах P,V:
подставим в (9.44) и получим уравнение адиабатного процесса в параметрах P,V:
 (9.45)
(9.45)
Докажем, что работа не является функцией состояния системы и зависит от вида процесса. При изменении объема системы от V1 до V2 совершается работа против внешних сил:
 (9.46)
(9.46)
1. При изохорном процессе A = 0, т.к. V= const.
2. При изобарном процессе (P = const)из (9.46) следует
 (9.47)
(9.47)
3. Работу при изотермическом процессе (T = const) найдем, подставив в уравнение (9.46) давление, полученное из уравнения Менделеева – Клапейрона: 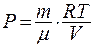 :
:
 (9.48)
(9.48)
4. В адиабатном процессе  , поэтому работа равна изменению внутренней энергии, взятому с отрицательным знаком:
, поэтому работа равна изменению внутренней энергии, взятому с отрицательным знаком:
 (9.49)
(9.49)
Из (9.45) найдем давление  подставим в (9.46) и запишем работу в виде:
подставим в (9.46) и запишем работу в виде:
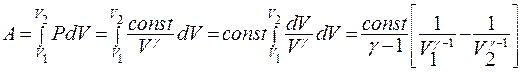 (9.50)
(9.50)
Находим работу при адиабатном процессе:
 (9.51)
(9.51)
Поиск по сайту: