 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Радиоактивность. Основной закон радиоактивного распада. Активность. Явление радиоактивности было открыто в 1896 г
Явление радиоактивности было открыто в 1896 г. А. Беккерелем, который наблюдал спонтанное испускание солями урана неизвестного излучения. Вскоре Э. Резерфорд и супруги Кюри установили, что при радиоактивном распаде испускаются ядра Не (a-частицы), электроны (b-частицы) и жёсткое электромагнитное излучение (g-лучи). В 1934 году был открыт распад с вылетом позитронов (b+-распад), а в 1940 году был открыт новый тип радиоактивности – спонтанное деление ядер: делящееся ядро разваливается на два осколка сравнимой массы с одновременным испусканием нейтронов и g-квантов. Протонная радиоактивность ядер наблюдалась в 1982 году.
Радиоактивность – способность некоторых атомных ядер самопроизвольно (спонтанно) превращаться в другие ядра с испусканием частиц.
Атомные ядра состоят из протонов и нейтронов, которые имеют обобщающее название – нуклоны. Количество протонов в ядре определяет химические свойства атома и обозначается Z (это порядковый номер химического элемента). Количество нуклонов в ядре называют массовым числом и обозначают А. Ядра с одинаковым порядковым номером и различными массовыми числами называются изотопами. Все изотопы одного химического элемента имеют одинаковые химические свойства. Физические свойства изотопов могут различаться весьма сильно. Для обозначения изотопов используют символ химического элемента с двумя индексами:  . Нижний индекс – порядковый номер, верхний – массовое число. Часто нижний индекс опускают, так как на него указывает сам символ элемента. Например, пишут 14С вместо
. Нижний индекс – порядковый номер, верхний – массовое число. Часто нижний индекс опускают, так как на него указывает сам символ элемента. Например, пишут 14С вместо 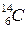 .
.
Способность ядра к распаду зависит от его состава. У одного и того же элемента могут быть и стабильный и радиоактивный изотопы. Например, изотоп углерода 12С – стабилен, а изотоп 14С – радиоактивен.
Радиоактивный распад – явление статистическое. Способность изотопа к распаду характеризует постоянная распада l.
Постоянная распада это вероятность того, что ядро данного изотопа распадется за единицу времени.
Вероятность распада ядра за малое время dt находится по формуле
Pdt = l·dt. (33.1)
Обозначим N – число ядер радиоактивного изотопа в момент времени t; dN' – число ядер распавшихся за время dt. Так как количество ядер в веществе – огромно, то выполняется закон больших чисел – частота равна вероятности:
dN'/N = Pdt.
Учитывая формулу (33.1), получим выражение, определяющее количество распавшихся ядер:
dN'/N = l· dt. (33.2)
Найдем закон, по которому убывает число ядер радиоактивного изотопа вследствие распада. Обозначим: N0 – число ядер в начальный момент времени (t = 0); N – число ядер в момент времени t; N' – число ядер распавшихся за время t. Очевидно, что
N' = N0 – N' и dN' = -dN.
Подставив выражение для dN' в (33.2), получим дифференциальное уравнение с разделяющимися переменными
l·dt = – dN/N.
Его решением этого является функция
N = Nо×exp (–l×t), (33.3)
где Nо – исходное число радиоактивных ядер, N - их число, оставшееся к моменту времени t, l - постоянная распада.
Формула (33.3) называется основным законом радиоактивного распада:
Число радиоактивных ядер убывает со временем по экспоненциальному закону.
На практике вместо постоянной распада l часто используют другую величину, называемую периодом полураспада.
Период полураспада (Т) – это время, в течение которого распадается половина радиоактивных ядер.
Закон радиоактивного распада с использованием периода полураспада записывается так:
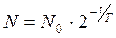 . (33.4)
. (33.4)
Характеристики распада Т и l связаны соотношением: Т = ln2/l = 0,693/l.
График зависимости (33.4) показан на рис. 33.1.
 |
Рис. 33.1. Убывание количества ядер исходного вещества при радиоактивном распаде
Период полураспада может быть как очень большим, так и очень маленьким (от долей секунды до многих миллиардов лет). В табл. 33.1 представлены периоды полураспада для некоторых элементов.
Таблица 33.1
Периоды полураспада для некоторых элементов
| Изотоп (доля в природном элементе) | Период полураспада (Т) |
| уран-238 (99,28%) | 4,50×109 лет |
| калий-40 (0,012%) | 1,3×109 лет |
| йод-131 нет йод-132 нет йод-125 нет | 8 дней 2,26 часа 60 дней |
| торий-232 (100%) | 1,4×1010 лет |
| радон-222 (–) | 3,8 дня |
| углерод-14 (–) | 5570 лет |
Для оценки степени радиоактивности изотопа используют специальную величину, называемую активностью.
Активность – число ядер радиоактивного препарата, распадающихся за единицу времени:
А = dN'/dt. (33.5)
Единица измерения активности в СИ – беккерель (Бк), что соответствует одному акту распада в секунду. На практике более употребительна внесистемная единица активности – кюри (Ки), равная активности 1 г 226Ra: 1 Ки = 3,7×1010 Бк.
С течением времени активность убывает так же, как убывает количество не распавшихся ядер:
 . (33.6)
. (33.6)
Из соотношения (33.2) получается формула для расчета активности:
А = l·N = 0,693N/T.
Число атомов радиоактивного изотопа (N) можно выразить через его массу m и молярную массу m:
N = m·NА/m,
где NА – постоянная Авогадро.
Тогда формула для расчета активности принимает вид:
А = l· m·NА/m = 0,693m·NА/(m·Т). (33.7)
В качестве характеристики изотопа используют его удельную активность (Ауд), которая равна активности единицы массы данного радиоактивного вещества.
Ауд = А/m, Ки/г. (33.8)
Удельная активность рассчитывается по формулам
Ауд = l·NА/m = 0,693NА/(m·Т). (33.9)
Поиск по сайту: