 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Внутриматочная патология
Внутриматочная патология включает гиперпластические процессы эндометрия; подслизистую миому матки; аденомиоз (внутренний эндометриоз); перегородки в матке; синехии; инородные тела. В структуре гинекологических заболеваний внутриматочная патология занимает значительное место.
Гиперпластические процессы эндометрия. Под гиперпластическими процессами эндометрия понимают патологическую диффузную или очаговую пролиферацию железистого и стромального компонентов слизистой оболочки матки с преимущественным поражением железистых структур.
Согласно принятой в 1994 г. классификации ВОЗ, выделяют эндоме-триальные полипы, эндометриальную гиперплазию - простую и сложную (комплексную), гиперплазию с клеточной атипией - простую и сложную.
В нашей стране термины "атипическая гиперплазия" и "аденоматоз" используются как синонимы, при этом атипическая гиперплазия подразделяется по степеням: легкая, среднетяжелая и тяжелая.
Гиперпластические процессы эндометрия возможны в любом возрасте, но их частота значительно возрастает в периоде перименопаузы.
Патогенез. Ведущее место в патогенезе гиперпластических процессов эндометрия отводится гормональным нарушениям в виде относительной или абсолютной гиперэстрогении при отсутствии антиэстрогенного влияния прогестерона или недостаточном его влиянии. Причины гиперэстроге-нии: ановуляция, обусловленная персистенцией или атрезией фолликулов; гормонопродуцирующие структуры яичников (стромальная гиперплазия, текоматоз, гранулезоклеточная опухоль, текаклеточные опухоли); нарушение гонадотропной функции гипофиза; гиперплазия коры надпочечников; неправильное использование гормональных препаратов (эстрогены, антиэстрогены). Известно, что у больных раком молочной железы прием та-моксифена увеличивает частоту гиперпластических процессов и рака эндометрия.
В патогенезе гиперпластических процессов эндометрия большое место занимают обменно-эндокринные нарушения: изменения жирового обмена, метаболизма половых гормонов при патологии гепатобилиарной системы и желудочно-кишечного тракта, иммунитета, функции щитовидной железы. В связи с этим у пациенток с гиперпластическими процессами эндометрия нередко отмечаются ожирение, гиперлипидемия, сахарный диабет, АГ, метаболический синдром.
Однако гиперпластические процессы эндометрия могут развиваться и при ненарушенных гормональных соотношениях. Немалую роль в развитии гиперпластических процессов эндометрия играют нарушения тканевой рецепции, инфекционно-воспалительные изменения в эндометрии, иммунные нарушения. Развитие железисто-фиброзных полипов эндометрия в 75% наблюдений происходит при ненарушенных гормональных соотношениях, при этом у 95,3% больных эндометрий инфицирован либо имеются признаки его хронического воспаления.
Развитие в последние годы молекулярной биологии, медицинской генетики, клинической иммунологии позволило выявить сложную систему факторов, участвующих в клеточной регуляции. Расширились представления о межклеточном взаимодействии и внутриклеточных процессах в гормонально зависимых тканях. Так, установлено, что в регуляции пролифера-тивной активности клеток эндометрия наряду с эстрогенами участвует ряд биологически активных соединений - таких, как факторы роста, цитоки-ны, метаболиты арахидоновой кислоты, а также система клеточного и гуморального иммунитета. Доказано, что в тканевом гомеостазе и патогенезе пролиферативных заболеваний важная роль принадлежит дисбалансу между процессами клеточной пролиферации и запрограммированной гибели клеток (апоптоз). Резистентность клеток эндометрия к апоптозу приводит к накоплению измененных и избыточно пролиферирующих клеток, что является характерной чертой неопластических изменений эндометрия.
Таким образом, патологическая трансформация эндометрия - сложный биологический процесс, затрагивающий все звенья нейрогуморальной системы организма женщины.
Гиперплазия эндометрия. Понятие "гиперплазия эндометрия" гистологическое; оно включает избыточный рост и структурные изменения желез эндометрия, отсутствие разделения на компактный и спонгиозный слои, нарушение правильного распределения желез в строме. Как правило, гиперпластическим изменениям подвергается функциональный слой слизистой оболочки тела матки, значительно реже - базальный слой.
Основные гистологические признаки железистой гиперплазии эндометрия сводятся к увеличению числа желез и изменению их формы (железы расширены), увеличению соотношения стромального и железистого компонентов при отсутствии цитологической атипии (рис. 15.1).
Простая гиперплазия эндометрия без атипии переходит в рак в 1% случаев, сложная без атипии - в 3 раза чаще.
Полипы эндометрия - наиболее распространенный вид гиперпластического процесса эндометрия; встречаются с частотой до 25%; малигнизиру-ются в 2-3% наблюдений. Наиболее часто полипы эндометрия выявляются в пре- и постменопаузе.
Полип эндометрия представляет собой доброкачественное образование, исходящее из базального слоя эндометрия. Патогномоничный анатомический признак полипа эндометрия - его основание (ножка) (рис. 15.2).
В зависимости от гистологического строения различают железистые (функционального или базального типа), железисто-фиброзные, фиброз-

Рис. 15.1. Простая железистая (железисто-кистозная) гиперплазия эндометрия. Окраска гематоксилином и эозином, × 200. Фото О.В. Зайратьянца

Рис. 15.2. Железисто-фиброзный полип эндометрия. Окраска гематоксилином и эозином, × 200. Фото О.В. Зайратьянца
ные и аденоматозные полипы эндометрия. Для аденоматозных полипов характерны интенсивная пролиферация желез и их эпителия с относительно высокой митотической активностью, атипия железистых клеток. Аденома-тозные полипы относят к предраковым состояниям слизистой оболочки матки.
Железистые полипы наиболее типичны для репродуктивного периода, железисто-фиброзные - для пре- и перименопаузы, фиброзно-железистые и фиброзные - для постменопаузы.
В репродуктивном и пременопаузальном периодах жизни женщины полипы эндометрия в качестве гистологически самостоятельной формы могут определяться как на фоне гиперплазии эндометрия, так и при нормальной слизистой оболочке различных фаз менструального цикла.
Полипы эндометрия в постменопаузе, как правило, бывают одиночными и могут возникать на фоне атрофичной слизистой оболочки. Иногда в этот период они достигают больших размеров и, выходя за пределы шейки матки, имитируют полип цервикального канала.
Особого внимания заслуживает рецидивирующая форма полипов эндометрия. Понятие "рецидив" неприемлемо, если ранее при удалении полипа эндометрия не использовался гистероскопический контроль, так как при выскабливании слизистой оболочки матки без гистероскопии возможно оставление патологически измененной ткани.
Предрак эндометрия. С морфологических позиций к предраку эндометрия относят гиперплазию с атипией (атипическая гиперплазия) и адено-матозные полипы.
К морфологическим признакам атипии эндометрия относят (рис. 15.3):
• увеличение числа желез, близко расположенных друг к другу, иногда с пальцеобразными выростами в направлении стромы;
• железистый цилиндрический эпителий в 2-4 ряда с формированием папиллярных выростов в направлении маточных желез, при выраженной атипии наблюдается потеря полярности;
• гиперхромные ядра с равномерным или (при большой атипии) с неравномерным распределением хроматина и глыбками его по периферии; высокую митотическую активность с увеличением спектра патологических митозов;
• базофильную цитоплазму при меньшей степени атипии, оксифиль-ную - при выраженной;
• наличие отечной стромы, с фибробластами и лимфоцитами;
• неравномерное распределение кровеносных сосудов с явлениями стаза и тромбоза.
Простая атипическая гиперплазия без лечения прогрессирует в рак у 8% больных, сложная атипическая гиперплазия - у 29%. Однако риск малиг-низации гиперпластических процессов эндометрия зависит не только от морфологической формы заболевания, но и от сопутствующей гинекологической и экстрагенитальной патологии (синдром поликистозных яичников, феминизирующие опухоли яичников, миома матки, ожирение, сахарный диабет или нарушение толерантности к глюкозе, гиперлипидемия, расстройства функции гепатобилиарной системы).
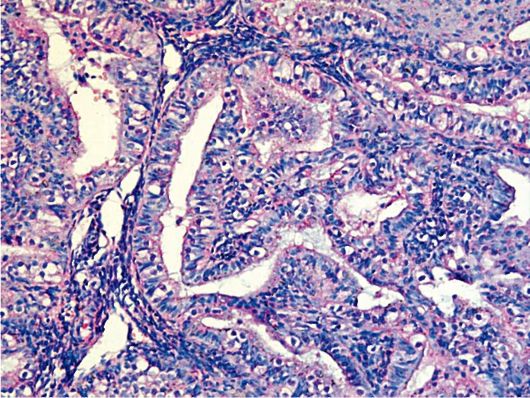
Рис. 15.3. Атипическая комплексная железистая гиперплазия эндометрия (аденома-тозная гиперплазия). Окраска гематоксилином и эозином, χ 400. Фото О.В. Зайратьянца
Клиническая симптоматика. Основные клинические проявления гиперпластических процессов эндометрия - маточные кровотечения, чаще ациклические в виде метроррагий, реже меноррагии. При больших полипах эндометрия могут наблюдаются схваткообразные боли внизу живота. Иногда полипы эндометрия остаются бессимптомными, особенно в постменопаузе.
Поскольку патогенетическую основу гиперпластических процессов эндометрия у больных репродуктивного возраста составляет ановуляция, одним из симптомов является бесплодие, чаще первичное.
Бессимптомное течение гиперпластических процессов эндометрия может наблюдаться у 10% менструирующих больных и у 40% в постменопаузе.
Диагностика гиперпластических процессов эндометрия. Скрининговыми методами диагностики гиперпластических процессов эндометрия являются трансвагинальное УЗИ, при неоднозначной эхографической картине возможно выполнение ГСГ, реже исследование аспирата из полости матки. Методами углубленного обследования являются гистероскопия и раздельное диагностическое выскабливание слизистой оболочки матки. Окончательно верифицировать диагноз можно только после гистологического исследования эндометрия.
Трансвагинальное УЗ-сканирование является высокоинформативным, не-инвазивным, безопасным методом диагностики гиперпластических процессов эндометрия. Информативность метода зависит от вида патологии эндометрия и возраста женщины; она повышается при сочетании с ГСГ. Диагностика гиперплазии эндометрия при УЗИ основывается на выявлении увеличенного в переднезаднем размере срединного маточного эха (М-эха) с неоднородной акустической плотностью. У менструирующих женщин толщину М-эха следует оценивать в соответствии с фазой менструального цикла. Лучше всего проводить исследование сразу после менструации, когда тонкое М-эхо соответствует полному отторжению функционального слоя эндометрия, а увеличение переднезаднего размера М-эха на всем протяжении либо локально должно расцениваться как патология. В большинстве
наблюдений отличить железистую гиперплазию эндометрия от атипической при УЗИ не удается.
Если период постменопаузы не превышает 5 лет, толщина М-эха до 5 мм может считаться нормальной, при постменопаузе более 5 лет она не должна превышать 4 мм (при однородной структуре).
Точность диагностики гиперплазии эндометрия при УЗИ составляет 6070%. ГСГ не позволяет значительно улучшить результаты диагностики.
Ультразвуковая картина полипов эндометрия показывает овоидные, реже округлые включения в полости матки повышенной эхоплотности (рис. 15.4). Диагностические затруднения возникают при железистых полипах эндометрия, которые повторяют конфигурацию полости матки, имеют листовидную, уплощенную форму и не приводят к утолщению М-эха. По звукопроводимости они близки к окружающему эндометрию. Регистрация цветовых эхо-сигналов при допплеровском исследовании в структуре включения дает возможность дифференцировать полипы с внутриматочными синехиями, а у менструирующих пациенток - со сгустками крови, но кровоток при ЦДК в полипах определяется лишь в 40% наблюдений. Информативность транс-

Рис. 15.4. Полип эндометрия. УЗИ
вагинального УЗИ при полипах эндометрия составляет 80-98%. Контрастирование полости матки при ГСГ позволяет повысить диагностические возможности УЗИ (рис. 15.5).
Цитологическое либо гистологическое исследование аспирата из полости матки может использоваться в качестве скрининга патологии эндометрия. Аспирационная биопсия эндометрия может использоваться как метод контроля эффективности гормональной терапии при гиперпластических процессах эндометрия. При раке эндометрия она позволяет поставить диагноз и избежать гистероскопии и диагностического выскабливания, которые не отвечают принципам абластики.
Гистероскопия. Информативность гистероскопии в диагностике гиперпластических процессов эндометрия составляет 63-97%. Гистероскопия необходима и перед выскабливанием слизистой оболочки матки - для уточнения характера патологии и его локализации, и после него - с целью контроля тщательности удаления ткани.

Рис. 15.5. Полипы эндометрия. ГСГ
При гиперплазии эндометрия и отсутствии кровяных выделений эндометрий, как правило, утолщен в виде складок различной высоты, бледно-розового цвета, отечный, в нем просматривается большое количество протоков желез (прозрачные точки; рис. 15.6). При изменении скорости потока жидкости в полость матки отмечается волнообразное движение эндометрия. Если гистероскопию проводят у пациентки с длительными кровяными выделениями, в дне матки и в области устьев маточных труб чаще определяются бахромчатые обрывки эндометрия бледно-розового цвета (на остальном протяжении эндометрий тонкий, бледный - рис. 15.7). Такую гистероскопическую картину трудно отличить от картины эндометрия в фазе ранней пролиферации. Окончательный диагноз возможен только при гистологическом исследовании соскоба слизистой оболочки матки.
При полиповидной форме гиперплазии эндометрия визуально полость матки на всем протяжении выполнена полиповидными разрастаниями эндометрия бледно-розового цвета, иногда с пузырьками по поверхности, множественными эндометриальными синехиями (рис. 15.8). Поверхность эндометрия при этом виде гиперплазии выглядит неровной, с ямками, кистами, бороздками различной величины. Как правило, в дне и по задней

Рис. 15.6. Гистероскопическая картина гиперплазии эндометрия (утолщенный эндометрий в виде складок)

Рис. 15.7. Эндометрий в виде обрывков в стадии отторжения. Гистероскопия

Рис. 15.8. Полиповидная гиперплазия эндометрия. Гистероскопия
стенке матки изменения более выражены. Полиповидную гиперплазию эндометрия, особенно при проведении гистероскопии накануне менструации, трудно отличить от эндометрия в фазе поздней секреции. В подобных случаях для установления диагноза необходимо сопоставить гистероскопическую картину с клинической картиной заболевания и днем менструального цикла.
Атипическая гиперплазия эндометрия не имеет характерных эндоскопических критериев, гистероскопическая картина напоминает обычную железисто-кистозную гиперплазию. При тяжелой форме атипической гиперплазии могут определяться железистые полиповидные разрастания тусклого желтоватого или сероватого цвета (рис. 15.9). Чаще они пестрые,

Рис. 15.9. Гистероскопическая картина атипической гиперплазии эндометрия

Рис. 15.10. Фиброзный полип эндометрия. Гистероскопия
желтовато-сероватые с белесым налетом. Как правило, окончательный диагноз устанавливают после гистологического исследования.
Фиброзные полипы эндометрия при гистероскопии определяются в виде единичных бледных образований округлой или овальной формы, чаще небольшого размера (от 0,5x1 до 0,5x1,5 см), обычно на ножке, плотной структуры, с гладкой поверхностью, маловаскуляризирован-ных (рис. 15.10). Иногда фиброзные полипы эндометрия достигают большого размера. При гистероскопии
может быть допущена диагностическая ошибка, когда одна из поверхностей полипа, который плотно прилегает к стенке матки, воспринимается как атрофичная слизистая оболочка и полип не диагностируется. При обнаружении полипа необходимо обследовать его со всех сторон, оценить величину, локализацию, место прикрепления, величину ножки. Фиброзные полипы напоминают подслизистые миоматозные узлы; при их дифферен-цировке часто возникают трудности.
Железисто-кистозные полипы эндометрия в отличие от фиброзных чаще бывают большого размера (до 5-6 см), определяются в виде единичных образований, хотя может быть одновременно несколько полипов. Форма полипов продолговатая, конусовидная, неправильная (с перемычками), поверхность гладкая, ровная, в некоторых случаях над ней выступают кистоз-ные образования с тонкой стенкой и прозрачным содержимым (рис. 15.11). Цвет полипов бледно-розовый, бледно-желтый, серовато-розовый. Нередко верхушка полипа бывает темно-багрового или синюшно-багрового цвета. На поверхности полипа видны сосуды в виде капиллярной сети (рис. 15.12).

Рис. 15.11. Желизисто-кистозный полип эндометрия. Гистероскопия

Рис. 15.12. Железисто-фиброзный полип эндометрия с сосудистым рисунком. Гистероскопия

Рис. 15.13. Аденоматозный полип эндометрия. Гистероскопия
Аденоматозные полипы эндометрия чаще локализуются ближе к устьям маточных труб и, как правило, бывают небольшого размера (0,5x1; 0,5x1,5 см), выглядят более тусклыми, серыми, рыхлыми (рис. 15.13), но могут визуально не отличаться от железисто-кистозных полипов; в этом случае характер полипа при эндоскопическом исследовании определить не удается.
Полипы эндометрия изменяют форму при изменении скорости подачи жидкости или газа в полость матки - они сплющиваются, увеличиваются в диаметре, при уменьшении давления вытягиваются в длину и совершают колебательные движения.
Гистологическое исследование соскобов слизистой оболочки матки -окончательный метод диагностики гиперпластических процессов эндометрия.
Лечение гиперпластических процессов эндометрия. Терапия у женщин разного возраста складывается из остановки кровотечения, восстановления менструальной функции в репродуктивном периоде или достижения атрофии и субатрофии эндометрия в более старшем возрасте, а также профилактики рецидива гиперпластического процесса.
Ведение пациенток репродуктивного возраста с гиперпластическими процессами эндометрия. Традиционным методом лечения гиперпластических процессов эндометрия является гормональная терапия, которую назначают после гистероскопии, раздельного диагностического выскабливания и гистологического исследования. Схемы гормонального лечения представлены в табл. 15.1.
Рецидив гиперпластического процесса эндометрия может свидетельствовать о гормонально-активных процессах в яичниках, что требует уточнения их состояния, включая визуальные методы диагностики (УЗИ, лапароскопия, биопсия яичников). Отсутствие морфологических изменений в яичниках позволяет продолжить гормональную терапию более высокими дозами препаратов либо использовать гестагенсодержащие ВМК. Необходимо учитывать инфекционный фактор как возможную причину заболевания и неэффективности гормонотерапии.
При неэффективности гормонотерапии, рецидиве гиперплазии эндометрия без атипии у женщин, выполнивших репродуктивную функцию и не заинтересованных в ее сохранении, целесообразна абляция (резекция) эндометрия, которая выполняется при нежелании женщины в дальнейшем беременеть, возрасте старше 35 лет, желании сохранить матку, величина которой не превышает 10 нед беременности. Миома матки и аденомиоз не являются абсолютными противопоказаниями для абляции при гиперплазии эндометрия, но они ухудшают результаты лечения.
Таблица 15.1. Гормональное лечение гиперпластических процессов эндометрия в репродуктивном возрасте

При неэффективности гормонотерапии и рецидиве атипической гиперплазии эндометрия или аденоматозных полипов целесообразно оперативное лечение, объем которого определяется индивидуально, возможно выполнение гистерэктомии, клиновидной резекции яичников (у больных с СПКЯ), аднексэктомии (при наличии гормонпродуцирующей опухоли яичника).
Лечение гиперпластических процессов эндометрия у пациенток в перимено-паузе. Первый этап лечения включает гистероскопию с раздельным диагностическим выскабливанием слизистой оболочки матки. Выбор дальнейшей терапии зависит от морфологической структуры эндометрия, сопутствующей гинекологической и экстрагенитальной патологии. Выбор гормонального препарата, схема и длительность лечения определяются также желанием женщины сохранить менструации.
Схемы гормональной терапии гиперпластических процессов эндометрия в пре- и перименопаузе представлены в табл. 15.2.
При рецидивирующей гиперплазии эндометрия без атипии, невозможности проведения гормонотерапии из-за сопутствующей экстрагенитальной патологии показана гистероскопическая операция - абляция эндометрия. Рецидив гиперпластических процессов эндометрия, а также сочетание этой патологии с миомой матки и (или) внутренним эндометриозом у больных в пре- и перименопаузе требуют расширения показаний к радикальному оперативному вмешательству (гистерэктомии).
Ведение пациенток с гиперплазией эндометрия в постменопаузе. Раздельное диагностическое выскабливание с гистероскопией показано пациенткам, у которых при скрининг-обследовании заподозрена патология эндометрия, либо имелись кровянистые выделения. При впервые выявленной гиперплазии эндометрия у женщин в постменопаузе целесообразно назначение гормональной терапии, при клинико-ультразвуковых признаках гормон-продуцирующей опухоли яичника показана гистерэктомия с придатками. Рецидив гиперплазии эндометрия в постменопаузе служит показанием к хирургическому вмешательству - экстирпации матки с придатками, что является методом выбора у данной категории больных. У пациенток с абсолютными противопоказаниями к абдоминальной гистерэктомии допустима гормонотерапия гестагенами до 12 мес, либо абляция эндометрия. Обязательным является динамическое наблюдение с эхографией, аспирационной биопсией эндометрия, при необходимости - с гистероскопией, раздельным диагностическим выскабливанием.
При атипической гиперплазии эндометрия в постменопаузе необходимо сразу решать вопрос о радикальной операции - пангистерэктомии. При выраженной экстрагенитальной патологии и повышенном риске оперативного лечения (пангистерэктомии) необходимо длительное лечение гестаге-нами.
Схемы гормональной терапии гиперплазии эндометрия у пациенток периода постменопаузы представлены в табл. 15.3.
С целью снижения риска осложнений гормонотерапии, назначаемой в любом возрасте по поводу гиперпластических процессов эндометрия, параллельно рекомендуют гепатопротекторы, антикоагулянты, антиагреганты.
Таблица 15. 2. Гормональная терапия гиперпластических процессов эндометрия в период пре- и перименопаузы

Таблица 15. 3. Гормональная терапия при гиперплазии эндометрия в постменопаузе

Лечение пациенток с полипами эндометрия. Основной метод лечения больных с полипом эндометрия - прицельная полипэктомия. Радикальное удаление полипа эндометрия (с базальным слоем эндометрия в месте локализации ножки полипа) возможно только под контролем гистероскопии с применением как механических эндоскопических инструментов, так и электрохирургических, а также лазерной технологии. Электрохирургическое иссечение полипа при гистероскопии рекомендуется при фиброзных и пристеночных полипах эндометрия, а также при рецидивирующих полипах эндометрия. У пациенток в период перименопаузы гистероскопическую полипэктомию целесообразно сочетать с абляцией эндометрия.
После удаления железистых и железисто-фиброзных полипов эндометрия назначают гормональную терапию, вид и длительность которой зависят от возраста пациентки, морфологического строения полипа, сопутствующей патологии. Схемы гормональной терапии пациенток с полипами эндометрия в постменопаузе представлены в табл. 15.4.
Схемы гормональной терапии при железистых полипах эндометрия в репродуктивном и перименопаузальном периодах соответствуют таковым при гиперплазии эндометрия без атипии.
Таблица 15.4. Гормональная терапия при полипах эндометрия в постменопаузе

Внутриматочные синехии. Внутриматочные синехии (сращения), подразумевают частичное или полное заращение полости матки (синдром Ашер-мана).
Патогенез. Существует несколько теорий возникновения внутриматоч-ных синехий: инфекционная, травматическая, нейровисцеральная. Основным фактором считается механическая травма базального слоя эндометрия после родов, аборта (раневая фаза) или грубого выскабливания; инфекция служит вторичным фактором. Возникновение внутриматочных сине-хий наиболее вероятно у пациенток с замершей беременностью, поскольку остатки плацентарной ткани могут вызывать активацию фибробластов и образование коллагена до регенерации эндометрия.
Внутриматочные синехии могут также возникнуть после оперативных вмешательств на матке: миомэктомии, метропластики или диагностического выскабливания слизистой оболочки, абляции эндометрия, а также после эндометрита. Данную патологию может также провоцировать ВМК.
Классификация. Наиболее удобна и часто используется классификация внутриматочных синехий по распространенности и степени облитерации полости матки:
I степень - вовлечено менее 1/4 объема полости матки, тонкие спайки, дно и устья труб свободны;
II степень - вовлечено от 1/4 до 3/4 объема полости матки, слипания стенок нет, есть только спайки, дно и устья труб частично закрыты;
III степень - вовлечено более 3/4 объема полости матки.
Клиническая симптоматика. В зависимости от степени заращения полости матки внутриматочные синехии проявляются гипоменструальным синдромом или аменореей. Следствием синехий становятся бесплодие или невынашивание беременности. В случае заращения нижней части полости матки с нормально функционирующим эндометрием в верхней части может развиться гематометра. Значительное заращение полости матки и недостаток нормально функционирующего эндометрия приводят к затруднению имплантации плодного яйца. Даже слабо выраженные внутриматочные си-нехии становятся одной из причин неэффективности ЭКО.
Диагностика. Для диагностики внутриматочных синехий применяют гистеросальпингографию, УЗИ, гистероскопию, наиболее информативна ГСГ.
Гистеросальпингография. Рентгенологическая картина при внутриматоч-ных синехиях зависит от характера последних и их распространенности. Обычно синехии проявляются в виде одиночных или множественных дефектов наполнения неправильной формы и различных размеров. Плотные множественные синехии могут разделять полость матки на большое количество камер различного размера, соединенных между собой мелкими протоками. Такую конфигурацию матки не удается определить при гистероскопии; она может дать информацию только о первых нескольких сантиметрах нижнего сегмента полости матки. При гистерографии текучее контрастное вещество может находить пути через сложные лабиринты и необлитериро-ванные пространства. При гистеросальпингографии часто получают ложно-положительные результаты из-за обрывков эндометрия, слизи, искривления полости матки.
УЗИ. Возможности эхографии в диагностике внутриматочных синехий ограничены. В некоторых случаях визуализируются неровные контуры эндометрия, прерывистое М-эхо, при гематометре определяется анэхогенное содержимое в полости матки. ГСГ позволяет выявить единичные внутри-маточные сращения, если нет полной обструкции в нижней части полости матки (рис. 15.14).
Гистероскопия. При гистероскопии синехии определяются как белесоватые бессосудистые тяжи - сращения между стенками матки различной, плотности и протяженности, нередко уменьшающие объем полости матки, а иногда полностью ее облитерирующие. Синехии могут располагаться также в цервикальном канале, вызывая его заращение и препятствуя доступу в полость матки и оттоку содержимого из нее. Нежные синехии выглядят как тяжи бледно-розового цвета в виде паутины, иногда видны проходящие

Рис. 15.14. Гидросонография (вну-триматочные синехии в виде дефекта наполнения)
в них сосуды. Более плотные синехии определяются как плотные белесоватые тяжи, располагающиеся, как правило, по боковым стенкам, реже - по центру полости матки (рис. 15.15, 15.16). Множественные поперечные синехии обусловливают частичное заращение полости матки с множеством полостей различной величины в виде углублений (отверстий). Иногда эти отверстия ошибочно принимают за устья маточных труб.
Лечение. В настоящее время единственным методом лечения внутрима-точных синехий является их рассечение под прямым визуальным гистероскопическим контролем, чтобы не травмировать оставшийся эндометрий - для восстановления нормального менструального цикла и фертильности. Характер операции, ее эффективность и отдаленные результаты зависят от вида внутриматочных синехий и степени окклюзии полости матки.
Расположенные центрально синехии можно разделить тупым путем с помощью корпуса гистероскопа. Используют также эндоскопические ножницы и щипцы, неодимовый ИАГ-лазер (на иттрий-алюминиевом гранате). Из электрохирургических инструментов наиболее удобен при разделении синехий электрод в виде иглы.

Рис. 15.15. Гистероскопическая картина плотных внутриматочных синехий (синдром Ашермана)

Рис. 15.16. Гистероскопическая картина плотных внутриматочных синехий
Для предотвращения возможной перфорации матки операцию проводят под контролем УЗИ, при значительном заращении полости матки - под лапароскопическим контролем.
Несмотря на высокую эффективность гистероскопического адгезиолизи-са внутриматочных синехий, рецидив заболевания не исключен, особенно при распространенных, плотных синехиях и у пациенток с туберкулезным поражением матки. Для предотвращения рецидива внутриматочных сращений практически все хирурги предлагают вводить в полость матки катетер Фолея (на 1 сут), ВМК типа петли Липпса не менее чем на 1 мес, специальный противоспаечный гель. В последующем назначают гормональную терапию (эстроген-гестагены в высоких дозах) с целью восстановления эндометрия в течение 3-6 мес.
Прогноз. Эффективность трансцервикального рассечения внутриматоч-ных синехий под контролем гистероскопа зависит от функционального состояния сохраненного эндометрия, распространенности и протяженности внутриматочных сращений: чем больше заращена полость матки, тем менее результативна операция. В плане восстановления менструальной и репродуктивной функций, а также возможности рецидива заболевания хуже всего прогноз при внутриматочных синехиях туберкулезной этиологии.
Беременные после рассечения распространенных внутриматочных сине-хий представляют группу риска по возникновению осложнений беременности, родов и послеродового периода. У 1/3 женщин с внутриматочными синехиями происходят самопроизвольные выкидыши, у1/3 - преждевременные роды и у 1/3 отмечается патология плаценты (плотное прикрепление, предлежание).
Профилактика. Необходимо помнить о возможности возникновения внутриматочных синехий у пациенток с осложненным течением раннего послеродового и послеабортного периода. При возникновении нарушений менструального цикла у этих женщин необходимо как можно раньше проводить гистероскопию с целью ранней диагностики синехий и их разрушения. У больных с подозрением на остатки плодного яйца или плаценты в матке целесообразно выполнять не просто выскабливание слизистой оболочки матки, а осуществлять гистероскопию для уточнения расположения патологического очага и его прицельного удаления без травмирования неизменного эндометрия.
Внутриматочная перегородка - порок развития, при котором полость матки разделена на две половины (гемиполости) перегородкой различной длины. Пациентки с внутриматочной перегородкой составляют 48-55% всех женщин с пороками развития половых органов. В общей популяции перегородка в матке встречается приблизительно у 2-3% женщин.
Клиническая картина. У женщин с перегородкой в матке в основном отмечается невынашивание беременности, реже - бесплодие. В I триместре беременности риск самопроизвольного выкидыша у пациенток с перегородкой в матке составляет 28-60%, во II триместре - приблизительно 5%. Для пациенток с внутриматочной перегородкой характерны преждевременные роды, нарушения сократительной способности матки в родах, отмечается
неправильное положение плода. Причины отрицательного влияния перегородки на течение беременности:
• недостаточный объем полости матки - перегородка мешает росту плода;
• истмико-цервикальная недостаточность, которая нередко сочетается с перегородкой матки;
• имплантация на бессосудистой перегородке, которая не способна поддерживать адекватное развитие эмбриона.
Чаще эти нарушения возникают при полной перегородке в матке.
У пациенток с перегородкой в матке часто встречаются дисменорея и патологические маточные кровотечения.
Примерно 50% женщин с внутриматочной перегородкой способны к зачатию и вынашиванию беременности, порок развития матки у них выявляется случайно, при обследовании по поводу другого заболевания.
Диагностика. Как правило, перегородка в матке диагностируется при обследовании пациентки с невынашиванием беременности (УЗИ, метро-сальпингография) либо при гистероскопии и выскабливании слизистой оболочки матки, при котором может возникнуть подозрение на аномалию развития. В клинической практике для диагностики внутриматочной перегородки используют различные методы исследования.
Гистеросальпингография позволяет определять только внутренние контуры полости матки; наружные контуры не видны, возможна ошибка в определении вида порока. При гистеросальпингографии сложно различить перегородку в матке и двурогую матку. Диагностическая точность гисте-росальпингографии в диагностике вида порока развития матки составляет
50%.
Эхография. Перегородка в матке выявляется не всегда и определяется на эхограмме как тонкостенная структура, идущая в переднезаднем направлении. Создается впечатление, что матка состоит из двух частей (рис. 15.17). По данным УЗИ отличить двурогую матку от полной или неполной перегородки в матке удается не всегда. УЗ-аппараты с трехмерным изображением позволяют с высокой точностью (91-95%) диагностировать внутриматоч-ную перегородку. Наибольшей информативностью обладает ГСГ: на фоне

Рис. 15.17. УЗИ внутриматоч-ной перегородки

Рис. 15.18. ГСГ внутриматочной перегородки
расширенной полости матки легко идентифицируется перегородка, можно определить ее толщину и протяженность (рис. 15.18).
При выполнении УЗИ матки у пациенток с подозрением на внутрима-точную перегородку необходимо обследование почек для исключения аномалий развития.
Эндоскопические методы исследования. Наиболее полную информацию о характере порока развития матки можно получить при сочетании гистероскопии, ГСГ и лапароскопии.
Параллельное обследование с применением двух эндоскопических методов необходимо в связи с тем, что гистероскопическая картина при двурогой матке и внутриматочной перегородке идентична. Лапароскопия позволяет не только уточнить вид порока развития матки (внешние контуры матки), оценить состояние придатков матки, тазовой брюшины, но и произвести коррекцию выявленных патологических процессов в брюшной полости. Кроме того, лапароскопия может быть методом контроля хода гистероскопической операции при рассечении внутриматочной перегородки.
У больных с внутриматочной перегородкой лапароскопическая картина может показать расширение матки в поперечнике или белесоватую полоску, проходящую в сагиттальном направлении, и небольшое втяжение в этой области; одна половина матки может быть больше другой, но иногда матка сохраняет обычные размеры и форму. Гистероскопия используется как для уточнения формы порока, так и для его хирургической коррекции.
При гистероскопии внутриматочная перегородка определяется в виде полоски ткани треугольной формы, различной толщины и длины, разделяющей полость матки на две гемиполости (рис. 15.19), причем в каждой из них определяется только одно устье маточной трубы. Перегородка может быть полной, доходящей до цервикального канала, и неполной (рис. 15.20). Чаще перегородка бывает продольной, длиной от 1 до 5-6 см, но могут встречаться и поперечные перегородки. Продольная перегородка может определяться в виде треугольника, основание которого утолщено и находится в дне матки. Редко встречаются перегородки в цервикальном канале. Уточнить вид порока развития матки, особенно при толстой и полной перегородке, можно при сочетании гистероскопии с ГСГ.

Рис. 15.19. Гистероскопическая картина внутриматочной перегородки, разделяющей полость матки на две гемиполости

Рис. 15.20. Неполная внутриматочная перегородка. Гистероскопия
Дополнительные методы исследования. Высокой информативностью в диагностике пороков развития матки обладают МРТ и спиральная КТ. Их применение целесообразно для уточнения диагноза в сложных случаях на этапе обследования; это позволяет избежать применения инвазивных методов диагностики. Однако вследствие дороговизны указанные методики не являются рутинными.
Лечение. Хирургическое лечение внутриматочной перегородки, по мнению многих авторов, должно проводиться только при выраженном нарушении репродуктивной функции. По мнению других, сразу же после выявления внутриматочной перегородки пациентке необходимо предложить метропластику, не дожидаясь возможных осложнений.
В настоящее время методом выбора при внутриматочной перегородке является ее рассечение под визуальным контролем трансцервикальным путем при гистероскопии. В зависимости от толщины перегородку можно рассекать с помощью эндоскопических ножниц (если она тонкая) либо ги-стерорезектоскопа (при толстой, широкой, васкуляризированной перегородке). Возможно применение лазера.
При полной перегородке матки, переходящей в цервикальный канал, рекомендуют сохранять цервикальную часть перегородки для предотвращения вторичной истмико-цервикальной недостаточности.
После рассечения широкой внутриматочной перегородки с целью уменьшения вероятности формирования синехий в месте рассечения перегородки и быстрой эпителизации большинство авторов назначают эстрогены (эстра-диол - по 2 мг ежедневно в 1-ю фазу) на 2-3 мес.
Прогноз. Гистероскопическое рассечение внутриматочной перегородки - щадящая и малотравматичная операция (в отличие от применявшейся ранее абдоминальной метропластики). Вследствие отсутствия рубца на матке после такой операции роды могут проводиться через естественные родовые пути. Частота нормальных родов, по данным разных авторов, после
гистероскопического рассечения внутриматочной перегородки составляет 70-85%. Однако в литературе есть упоминания о разрывах матки во время беременности после гистероскопической метропластики - как осложненной (перфорация матки), так и неосложненной метропластики.
Инородные тела в матке. К инородным телам в матке относятся внутри-маточные контрацептивы (ВМК) и их фрагменты, костные остатки, различные лигатуры.
Клиническая картина инородных тел в полости матки чаще проявляется различными нарушениями менструальной функции (меноррагии, меноме-троррагии, ациклические кровяные выделения). При длительном нахождении инородного тела в матке клиническая симптоматика может проявляться вторичным бесплодием, явлениями хронического эндометрита или пиометрой. Возможны бессимптомные инородные тела в полости матки (фрагменты ВМК).
Болевой синдром возникает при перфорации матки ВМК и дальнейшей миграции его к соседним органам с возможной их перфорацией. Не исключена миграция ВМК в сальник, ректосигмоидный угол толстой кишки, забрюшинное пространство, мочевой пузырь, в слепую кишку, к области червеобразного отростка, в тонкую кишку, к придаткам матки.
Костные фрагменты обычно становятся случайной находкой у пациенток с нарушениями менструального цикла, длительным эндометритом или выявляются при обследовании у женщин с вторичным бесплодием. В анамнезе можно выявить случаи прерывания беременности при большом сроке (13-14 нед и более), осложнявшиеся, как правило, длительным кровотечением, иногда с повторными выскабливаниями.
Лигатуры, как правило, шелковые или лавсановые, выявляются у больных хроническим эндометритом и пиометрой, с указанием на кесарево сечение или консервативную миомэктомию в анамнезе. Также пациентки жалуются на постоянные гнойные выделения из половых путей, не поддающиеся массивной антибактериальной терапии, и вторичное бесплодие.
Диагностика. Основной метод диагностики инородных тел в матке - гистероскопия, дополнительные методы (УЗИ, при необходимости гидросо-нография - ГсГ и лапароскопия).
УЗИ. Ультразвуковая картина при ВМК зависит от формы и типа контрацептива. Каждый тип ВМК дает характерное четкое эхогенное изображение, способное меняться в зависимости от локализации контрацептива в матке. Оптимально для контрацепции такое расположение ВМК, когда его дистальная часть локализуется в дне, а проксимальная - не достигает уровня внутреннего зева.
При смещении ВМК его проксимальная часть визуализируется в верхней трети цервикального канала. Наиболее серьезное осложнение ВМК - перфорация матки, которая может быть неполной (ВМК проникает в мио-метрий) или полной (ВМК частично или полностью выходит за пределы матки).
Фрагменты ВМК могут определяться как в полости матки, так и в толще миометрия в виде линейных включений повышенной эхогенности, различных размеров, дающих акустическую тень (рис. 15.21).
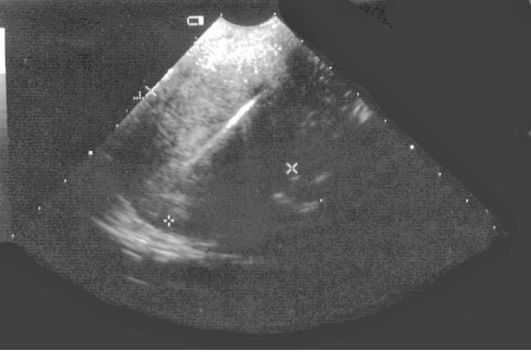
Рис. 15.21. УЗИ (фрагментарные остатки ВМК в миометрии и полости матки)
Точная ультразвуковая диагностика костных фрагментов затруднена. При УЗИ они могут определяться в виде разрозненных эхонасыщенных структур неправильной формы.
При лигатурах в полости матки УЗИ малоинформативно.
Гистероскопия. Эндоскопическая картина ВМК зависит от вида контрацептива и времени проведения исследования. Длительно находящийся в матке ВМК частично прикрывается синехиями и лоскутами эндометрия, кристаллами солей. При подозрении на фрагменты ВМК гистероскопию необходимо проводить в раннюю фазу пролиферации, тщательно осматривая все стенки матки. Фрагменты ВМК могут быть представлены раздробленной пластиковой частью, металлическими обломками, "усами" (рис. 15.22, 15.23); свободно находиться в полости матки или частично внедряться в ее стенку. При обнаружении перфорации матки ВМК гистероскопию проводят совместно с лапароскопией.

Рис. 15.22. Гистероскопическая картина ВМК, покрытого кристаллами солей

Рис. 15.23. Гистероскопическая картина ВМК с "усами"

Рис. 15.24. Гистероскопическая картина костных фрагментов
Гистероскопия показана, когда в полости матки остаются фрагменты ВМК вследствие неудачного его удаления и есть подозрение на перфорацию матки. При длительном пребывании контрацептива в полости матки иногда происходит его плотное прикрепление и даже врастание в толщу миометрия. Гистероскопия позволяет определить локализацию самого ВМК или его фрагментов и прицельно удалить эти инородные тела.
Гистероскопическая картина костных фрагментов зависит от длительности их
пребывания в матке. Если срок относительно небольшой, видны пластинчатые плотные белесоватые образования с острыми краями, внедрившиеся в стенку матки (рис. 15.24). Если костные фрагменты долго находились в полости матки (более 5 лет), они имеют характерное кристаллическое строение (коралловидную форму) и при попытке удаления щипцами рассыпаются, "как песок". Чаще всего костные фрагменты располагаются в области устьев маточных труб и в дне матки.
Лигатуры при гистероскопии определяются как белесоватые нити на фоне общей гиперемии слизистой оболочки матки в нижней ее трети по передней стенке (после кесарева сечения) или в различных участках стенок матки (после консервативной миомэктомии; рис. 15.25, 15.26).
Лечение. Инородные тела удаляют из матки при гистероскопии с помощью специальных эндоскопических инструментов. Не рекомендуется пытаться удалять ВМК без видимых "усов" вслепую, различными приспособлениями. Такие попытки обычно приводят к деформации ВМК, его фрагментации, а иногда - к перфорации матки. При подозрении на перфорацию матки ВМК проводят сочетанное исследование: гистероскопию и лапароскопию.

Рис. 15.25. Лигатуры в полости матки после кесарева сечения. Гистероскопия

Рис. 15.26. Лигатуры в полости матки после консервативной миомэктомии. Гистероскопия
Если по данным УЗИ в толще миометрия определяются фрагменты ВМК, а при гистероскопии и лапароскопии их определить не удается, не следует пытаться извлекать эти фрагменты из толщи стенки. Необходимо наблюдение за пациенткой.
В послеоперационном периоде после удаления инородного тела из матки рекомендуется антибактериальная терапия с учетом чувствительности микрофлоры к препарату.
Контрольные вопросы
1. Перечислите виды внутриматочной патологии.
2. Назовите современные методы диагностики видов внутриматочной патологии.
3. Приведите классификацию гиперпластических процессов эндометрия (ВОЗ, 1994).
4. Какова лечебная тактика у больных с полипами эндометрия, эндо-метриальной и атипической гиперплазией эндометрия в различные периоды жизни женщины?
5. Укажите типы субмукозной миомы матки (в зависимости от выраженности интрамурального компонента узла).
6. Назовите методы диагностики и лечения у больных с субмукозной миомой.
Поиск по сайту: