 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Обратимые и необратимые процессы
Пусть в результате некоторого процесса в изолированной системе тело переходит из состояния А в состояние В и затем возвращается в начальное состояние А. Процесс называется обратимым, если возможно осуществить обратный переход из В в А через те же промежуточные состояния, что и в прямом процессе, чтобы не осталось никаких изменений и в самом теле и в окружающих телах. Если же обратный процесс невозможен, или по окончании процесса в окружающих телах и в самом теле остались какие-либо изменения, то процесс является необратимым.
Любой процесс сопровождаемый трением, теплопередачей от нагретого тела к менее нагретому (теплопроводность), является необратимым. К необратимым процессам также относятся диффузия, вязкое течение. Все необратимые процессы являются неравновесными.
Равновесные – это такие процессы, которые представляют из себя последовательность равновесных состояний. Равновесное состояние – это такое состояние, в котором без внешних воздействий тело может находиться сколь угодно долго. (Строго говоря, равновесный процесс может быть только бесконечно медленным. Любые реальные процессы в природе протекают с конечной скоростью и сопровождаются рассеянием энергии. Обратимые процессы – идеализация, когда необратимыми процессами можно пренебречь).
Если тело из состояния А в состояние В переходит через одни промежуточные состояния, а возвращается в начальное состояние А через другие промежуточные состояния, то совершается круговой процесс, или цикл.
Круговой процесс является обратимым, если все его части обратимы. Различают прямой цикл, или цикл тепловой машины и обратный цикл, или цикл холодильной машины.
2. Цикл Карно и его КПД для идеального газа
Коэффициент полезного действия идеальной тепловой машины, работающей по циклу Карно. Эта величина равна отношению количества теплоты, превращённого в работу, к количеству теплоты, полученному от нагревателя.
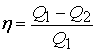
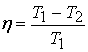
То есть КПД цикла Карно определяется только температурами нагревателя и холодильника.
Теорема Карно (без доказательства): КПД всех обратимых машин, работающих при одних и тех же температурах нагревателя и холодильника одинаков и определяется только температурами нагревателя и холодильника.
КПД реальной тепловой машины всегда ниже, чем КПД идеальной тепловой машины (в реальной машине существуют потери тепла, которые не учитываются при рассмотрении идеальной машины).
3. Принцип действия теплового двигателя и холодильной машины
Любой тепловой двигатель состоит из 3-х основных частей: рабочего тела, нагревателя и холодильника.
Рабочее тело получает некоторое количество теплоты Q1, от нагревателя. При сжатии газ передаёт некоторое количество теплоты Q2 холодильнику.
Полученная работа, совершаемая двигателем за цикл: 
Холодильная машина. От холодильной камеры поглощается тепло Q2.
Нагревателю рабочее тело передаёт некоторое количество теплоты Q1.
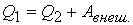
В результате цикла некоторое количество теплоты переходит от холодного тела к телу с более высокой температурой.
Реально рабочим телом в холодильной установке обычно служат пары легкокипящих жидкостей – аммиак, фреон и т. п.
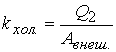 Эффективность холодильной установки оценивается по холодильному коэффициенту:
Эффективность холодильной установки оценивается по холодильному коэффициенту:
Тепловой насос. “Отопительный” коэффициент: 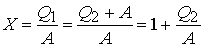
4. Энтропия. Закон возрастания энтропии
Энтропия: 
Физический смысл имеет не сама энтропия, а разность энтропий.
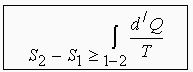
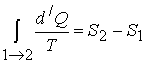
Закон возрастания энтропии:
Энтропия адиабатически изолированной системы не может убывать, она либо возрастает, либо остаётся постоянной. (Закон возрастания энтропии).
5. Статистический вес (термодинамическая вероятность).
Под термодинамической вероятностью понимается число микросостояний (микрораспределений, например, распределений молекул по пространству или энергии) которыми может определяться рассматриваемое макрораспределение.
Наибольшая термодинамическая вероятность у равномерного распределения, оно может осуществляться наибольшим числом способов.
Поиск по сайту: