 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Энтропия жидкости и пара
Как известно, из всей подведенной в круговом процессе теплоты Q 1 в полезную работу переводится только (Q 1 – Q 2) ккал, а Q 2 ккал передается в теплоприемник. Теплота Q 2 является прямой. Хотя и необходимой, потерей, которую следует стремиться уменьшить.
Выясним, от каких факторов она зависит. Допустим, что совершается равновесный цикл Карно (рис. 5.9).

Рис. 5.9. Система тел, участвующих в совершении
термодинамических циклов
Для этого цикла  =
=  или
или  .
.
Отсюда имеем
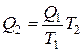 .
.
Как видим, величина Q 2 зависит от двух множителей: отношения  и температуры T 2. Если температуру считать величиной постоянной, то потеря теплоты Q, зависит практически только от величины отношения
и температуры T 2. Если температуру считать величиной постоянной, то потеря теплоты Q, зависит практически только от величины отношения  . Чем больше это отношение, тем больше потеря Q 2.
. Чем больше это отношение, тем больше потеря Q 2.
Учитывая большую роль отношения 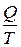 , в термодинамику введена особая величина, зависящая от этого отношения и названная э н т р о п и е й.
, в термодинамику введена особая величина, зависящая от этого отношения и названная э н т р о п и е й.
Если равновесный процесс подвода или отвода теплоты совершается при постоянной температуре, как в цикле Карно, то изменение энтропии в таких процессах для 1 кг тела будет
s 2 – s 1 =  = 2,3
= 2,3  lg
lg  кДж/кг∙град, (5.10)
кДж/кг∙град, (5.10)
где:
q – участвующая в процессе теплота;
Т – температура, при которой совершается процесс.
В приведенной формуле s 1 принимают равной нулю при Т 1 = 273 оС, теплоемкость воды принимается равной 4,19 кДж/кг∙град.
Под энтропией жидкости (воды) подразумевают увеличение энтропии 1 кг воды, имеющей температуру 0 оС, в процессе нагревания ее при постоянном давлении до кипения.
Если вода не доводится до кипения, то энтропия ее
s ж = 2,3 lg  ,
,
где Т – конечная температура воды.
Энтропия кипящей жидкости
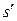 = 2,3 lg
= 2,3 lg  .
.
Энтропия сухого насыщенного пара 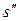 представляет собой увеличение энтропии 1 кг воды, взятой при 0 оС, в процессе превращения ее при постоянном давлении в сухой насыщенный пар.
представляет собой увеличение энтропии 1 кг воды, взятой при 0 оС, в процессе превращения ее при постоянном давлении в сухой насыщенный пар.
Процесс получения пара из кипящей воды происходит при постоянной температуре; поэтому изменение энтропии в этом процессе может быть найдено по уравнению
s 2 – s 1 =  .
.
В данном случае 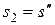 (энтропия сухого пара),
(энтропия сухого пара),  (энтропия жидкости); q = r – (теплота парообразования) и Т = Тs.
(энтропия жидкости); q = r – (теплота парообразования) и Т = Тs.
Таким образом
 ,
,
откуда

или
 .
.
Понятно, что энтропия влажного пара sх, для которого q = хr, будет равна:
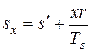 ,
,
или
 .
.
Энтропия перегретого пара s представляет собой увеличение энтропии 1 кг воды, взятой при 0 оС, в процессе превращения ее при постоянном давлении в перегретый пар.
В процессе перегрева при постоянном давлении температура пара повышается, поэтому изменение энтропии в процессе перегрева нужно подсчитать по уравнению
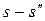 = 2,3
= 2,3  lg
lg  ,
,
где:
сpm – средняя изобарная теплоемкость перегретого пара,
Т – абсолютная температура перегретого пара.
Из этого уравнения получаем
 =
= 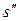 + 2,3
+ 2,3 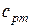 lg
lg 
или окончательно
 .
.
Поиск по сайту: