 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Стадии радикальной полимеризации. Инициирование (термическое, окислительно-восстановительное, фотохимическое)
Инициирование состоит из двух реакций. В начале, в результате гомолитического распада молекулы инициатора (I) или катализатора, образуется два радикала..
I  2 R·
2 R·
Затем, образовавшийся радикал присоединяется к молекуле мономера с образованием инициирующего центра растущей цепи.
R· + М 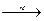 R-М
R-М  ·
· 
R· + CH 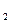 = CH
= CH 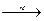 R– CH
R– CH 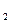 - CH·
- CH·
| |
X X
I. Термическое инициирование. Наиболее широко применяются термический, гомолитический распад инициаторов. В качестве инициаторов используется ограниченный круг соединений с энергией диссоциации связи 25 – 40 килокаллорий на моль, содержащие связи О- О, S–S, N–O. Наиболее широко используются перекиси и азосоединения.
1. Ацилпероксиды.
Распад пероксида бензоила:
(С  Н
Н  -СОО)
-СОО) 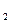
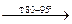 2С
2С  Н
Н  -СОО· → С
-СОО· → С  Н
Н  ∙ + СО
∙ + СО 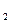 ↑
↑
Распад пероксида ацетила:
(СН  -СОО)
-СОО) 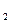
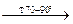 2СН
2СН  -СОО·→ СН
-СОО·→ СН  · + СО
· + СО 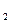 ↑
↑
2. Алкилпероксиды. Пероксид тетрабутила [(СН3)3СО]2; пероксид кумола [С6Н5(СН3)2СО]2.
Распад пероксида кумола:
СН  СН
СН  СН
СН 
׀ ׀ ׀
СН  – C – O – O – C – СН
– C – O – O – C – СН 
 2 СН
2 СН  – C – O∙
– C – O∙
׀ ׀ ׀
С  Н
Н  С
С  Н
Н  С
С  Н
Н 
Распад пероксида тетрабутила:
СН  СН
СН  СН
СН 
׀ ׀ ׀
СН  – C – O – O – C – СН
– C – O – O – C – СН 
 2 СН
2 СН  – C – O∙
– C – O∙
׀ ׀ ׀
СН3 СН3 СН3
3. Гидропероксиды: гидропероксид третбутила (СН  )
)  С –О– OH, гидропероксид кумола С
С –О– OH, гидропероксид кумола С  Н
Н  (СН
(СН  )
) 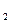 С–О– OH, гидропероксид ацетила СН
С–О– OH, гидропероксид ацетила СН  СО – O – OH.
СО – O – OH.
Распад гидропероксида кумола:
СН  СН
СН 
׀ ׀
СН  – С – О – OH
– С – О – OH 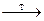 СН
СН  – С = О + ·OH + С
– С = О + ·OH + С  Н
Н  ∙
∙
׀ (СН  )
)
С  Н
Н 
(СН  )
)
Распад гидропероксида третбутила:
СН  СН
СН 
׀ ׀
СН  – С – О – OH
– С – О – OH 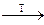 СН
СН  – С = О + ·OH + СН3∙
– С = О + ·OH + СН3∙
׀
СН3
Распад 2,2'- азобисизобутиронитрил (АИБН)
СН  СН
СН  СН
СН 
׀ ׀ ׀
NС – C –N = N– C – CN  2 NС – C· + N
2 NС – C· + N 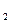
׀ ׀ ׀
СН  СН
СН  СН
СН 
Легкое разложение азосоединеий обусловлено образованием в процессе их распада молекул азота.
ΙΙ. Окислительно-восстановительное инициирование. Особенностью является очень низкая энергия активации (12 – 20 ккал./моль вместо 35 ккал./моль) при термическом инициировании, что позволяет проводить реакцию при низких температурах (от 0 до 50  С) и тем самым уменьшить возможность протекания побочных процессов.
С) и тем самым уменьшить возможность протекания побочных процессов.
Fe  + Н
+ Н 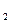 О
О 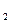 → Fe
→ Fe  + ОН
+ ОН 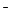 + ·ОН
+ ·ОН
Радикал ·ОН, присоединяясь к молекуле мономера, инициирует радикальную полимеризацию. Применяются также окислительно-восстановительные системы, растворимые в воде – персульфат натрия, тиосульфат натрия, а также растворимые в органических растворителях – органические пероксиды (амиды).
ΙΙΙ. Фотохимическое инициирование. В этом случае радикалы образуются в результате ультрафиолетового облучения чистого мономера, а также мономера, содержащего катализатор или фотосенсибилизатор. Мономер, поглощая квант света, переходит в возбужденное состояние.
М + hν → М 
квант
света
Возбужденные частицы, в результате гомолитического разрыва химических связей, распадаются на радикалы: М  → R· + R'·, которые способны инициировать полимеризацию.
→ R· + R'·, которые способны инициировать полимеризацию.
Сенсибилизатор С, поглощая квант света, переходит в возбужденное состояние, затем передает свою энергию мономеру М, который в возбужденном состоянии распадается на радикалы:
С + hν → С 
С  + М → С + М
+ М → С + М 
М  → R· + R'·
→ R· + R'·
ΙV. При радиохимическом инициировании радикальной полимеризации, образование радикалов происходит под действием ионизирующих излучений (гамма-лучей, альфа-частиц, нейтронов, быстрых электронов, бета-лучей). Под действием высоких энергий происходит ионизация соединений углерода с выбросом электронов по схеме:
С + излучение → С  +
+ 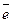
Радикал может также образоваться при диссоциации катиона: С + → А· + В 
Выброшенный электрон может присоединиться к катиону В  с образованием другого радикала, т.е. В
с образованием другого радикала, т.е. В  +
+ 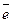 →В.
→В.
Поиск по сайту: