 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Горючее – индивидуальное химическое соединение
В случае индивидуального химического соединения объем и состав продуктов горения рассчитывается по уравнению реакции горения.
| Расчет объема и процентного состава продуктов горения индивидуального вещества | Пример 2.8. Определить объем и состав в объемных % продуктов горения, образовавшихся при сгорании 3 кг бензола С6Н6. Температура 200С, давление 770 мм рт.ст., коэффициент избытка воздуха a = 1,4. |
1. Записываем уравнение реакции горения
3 кг х1 м3 х2 м3 х3 м3 х4 м3
С6Н6 + 7,5(О2 + 3,76N2) = 6СО2 + 3Н2О + 7,5×3,76N2
М = 78 кг 7,5×4,76 × Vм = 6×Vм = 3×Vм = 7,5×3,76×Vм =
=7,5×4,76×23,7 м3 =6×23,7 м3 =3×23,7 м3 =7,5×3,76×23,7 м3
2. Рассчитаем, какой объем занимает 1 кмоль газообразных веществ при заданных температуре и давлении.
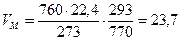 м3/кмоль
м3/кмоль

3. Теоретический объем продуктов горения (VПГ) определяем по уравнению реакции.
VПГ = 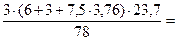 33,9 м3
33,9 м3
4. Горение протекает с коэффициентом избытка воздуха, следовательно, в состав продуктов горения войдет избыточный воздух DVв.
Для расчета избытка воздуха по уравнению реакции найдем теоретический объем воздуха, необходимый для полного сгорания бензола:
Vвтеор = х1 = 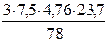 = 32,5 м3
= 32,5 м3
Избыток воздуха определим по формуле (3.4):
DVв= Vвтеор(a -1) = 32,5(1,4 – 1) = 13 м3
С учетом избытка воздуха практический объем продуктов горения составит:
VПГ* = VПГ + DVв = 33,9 + 13 = 46,9 м3
5. Иногда возникает необходимость рассчитать объем отдельных компонентов продуктов горения и их процентный состав.
В этом случае по уравнению реакции определяем объем СО2, Н2О и N2.
V(СО2) = х2 =  = 5,47 м3
= 5,47 м3
V(Н2О) = х3 = 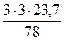 = 2,73 м3
= 2,73 м3
V(N2) = х4 = 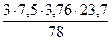 = 25,71 м3
= 25,71 м3
DVв= 13 м3 (рассчитано в п.4)
Объемная концентрация каждого компонента смеси рассчитывается следующим образом:
jоб (СО2) =  =
=  = 11,7 %
= 11,7 %
jоб (Н2О) =  =
= 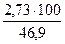 = 5,8 %
= 5,8 %
jоб (N2) = 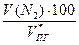 =
= 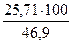 = 54,8 %
= 54,8 %
jоб (DVв) =  =
=  = 27,7 %
= 27,7 %
Обратите внимание, что более половины объема всех продуктов горения – это азот воздуха, израсходованного на горение. Если же горение протекает с коэффициентом избытка воздуха a > 1, то избыточный воздух также составляет значительную часть продуктов горения.
Поиск по сайту: