 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Горючее вещество – определенное химическое соединение. Если горючее вещество (твердое, жидкое или газообразное) представляет собой определенный химический элемент или соединение
Если горючее вещество (твердое, жидкое или газообразное) представляет собой определенный химический элемент или соединение, то для него можно записать уравнение химической реакции горения. В этом случае состав и содержание продуктов полного сгорания можно определить непосредственно по уравнению реакции горения.
Рассмотрим порядок расчета на примере горения этилацетата СН3–СОО–С2Н5 при нормальных условиях (Т =0°С, р =760 мм Hg)
· Запишем уравнение реакции горения:
СН3–СОО–С2Н5+5О2=4СО2–4Н2О.
· В это уравнение подставим значения молекулярных масс входящих в него элементов:

· Определим массу продуктов сгорания, образующихся при полном сгорании 1 кг этилацетата:
 кг;
кг;  кг.
кг.
· По известной плотности углекислого газа (r=1.977 кг/м3) и паров воды (r=0.804 кг/м3) при нормальных физических условиях, определим объем продуктов сгорания 1 кг этилацетата:
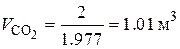 ;
;  .
.
Таким образом, при полном сгорании 1 кг этилацетата при нормальных физических условиях образуется 1.01 м3 углекислого газа и 1.02 м3 паров воды. В ряде случаев необходимо определить состав сухих продуктов сгорания, то есть без учета паров воды. В состав сухих продуктов сгорания этилацетата входит только углекислый газ СО2.
Поиск по сайту: