 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Горючее вещество – определенное химическое соединение
Если горючее вещество представляет собой определенный химический элемент или соединение, то для него можно записать уравнение химической реакции горения. В этом случае, независимо от агрегатного состояния вещества (твердое, жидкое или газообразное), необходимое для полного сгорания количество воздуха определяется непосредственно по уравнению реакции горения.
Для проведения расчетов необходимо знать относительные молекулярные массы основных веществ, участвующих в горении. В табл. 4.4 приведены значения М для основных компонентов органических и углеводородных топлив. Отметим, что азот воздуха не участвует в горении и является инертным веществом, так же как и входящие в состав воздуха инертные газы.
Таблица 4.4
Относительные молекулярные массы веществ
| Вещество | О2 | С | Н2 | S | Воздух | Fe | Al | N | Mg |
| М |
Рассмотрим порядок расчета на примере горения бензола С6Н6.
· Запишем уравнение реакции горения:
С6Н6+7.5О2=6СО2+3Н2О.
· В это уравнение подставим значения относительных молекулярных масс входящих в него элементов:
6×12+6×1+7.5(2∙16)=6(1∙12+2×16)+3(1×2+1∙16).
Поскольку молярная масса M (кг/кмоль) вещества численно совпадает с его относительной молекулярной массой, последнее соотношение можно записать в виде:

Таким образом, для сжигания 78 кг бензола C6H6 необходимо 240 кг кислорода.
· Определим массу кислорода mк, необходимую для сжигания 1 кг бензола:
 кг.
кг.
· По известной плотности кислорода при нормальных физических условиях (r н =1.429 кг/м3), взятой из табл. 4.1, определим объем кислорода Vк, необходимый для полного сгорания 1 кг бензола:
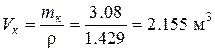 .
.
· Поскольку горение происходит в среде воздуха, расчет объема воздуха проведем с учетом объемного содержания кислорода в воздухе (21 %):
Vв =2.155∙4.762=10.262 м3.
Таким образом, для полного сгорания 1 кг бензола при нормальных физических условиях необходимо 10.262 м3 воздуха.
· Проведем расчет объема воздуха при заданных условиях (например, при Т =+20°С (293 К), р =750 мм Hg) с помощью формулы 4.6:
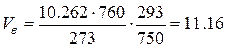 м3.
м3.
Таким образом, для полного сгорания 1 кг бензола при заданных условиях необходимый объем воздуха составляет Vв =11.16 м3.
Поиск по сайту: