 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
ОБЩАЯ ХАРАКТЕРИСТИКА АВТОНОМНОЙ НЕРВНОЙ СИСТЕМЫ
Автономная нервная система представляет часть общей нервной системы, состоит из центральных и периферических образований, осуществляет нервную регуляцию деятельности органов кровообращения, дыхания, пищеварения, выделения, размножения. Кроме того, она влияет на интенсивность обмена веществ в тканях и органах в соответствии с меняющимися условиями их функционирования, то есть выполняет адаптационно-трофическую функцию.
В настоящее время на основании структурных и функциональных признаков АНС подразделяется на симпатический, парасимпатический и метасимпатический отделы. Первые два имеют центральные и периферические части, а метасимпатический – только периферические образования. Центральными структурными элементами АНС являются ядра и диффузно расположенные нейроны спинного и головного мозга, а периферическими – автономные ганглии, сплетения, нервные проводники и окончания.
Функционально АНС существенно отличается от соматической (анимальной): последняя регулирует главным образом сложные произвольные движения, а функции АНС значительно разнообразнее.
В целом, оказывая регуляторное влияние на деятельность практически всех органов, она изменяет их функциональную активность в зависимости от физических и психических нагрузок в каждый данный момент, обеспечивает адекватную реакцию на все изменения, поддерживая при этом внутренний гомеостаз. Например, у спортсмена, начиная со старта, под действием импульсов симпатической нервной системы учащаются и усиливаются сокращения сердца, сужаются кровеносные сосуды кожи, желудочно-кишечного тракта, слюнных желез и других органов, а в скелетных мышцах они расширяются, тормозится двигательная активность желудка и кишечника, уменьшается выделение сока в желудке и поджелудочной железе, расширяются бронхи, расслабляется мочевой пузырь и задерживается его опорожнение, стимулируется потоотделение, увеличивается расщепление гликогена в печени и мышцах, а также нейтральных жиров в белых липоцитах, повышается содержание глюкозы и жирных кислот в крови, подавляется выделение инсулина и усиливается выработка глюкокортикоидов, гормонов щитовидной железы, расширяются зрачки, повышается восприимчивость органов чувств и работоспособность центральной нервной системы. После прекращения больших физических нагрузок под влиянием импульсов парасимпатической нервной системы происходят противоположные изменения, и функции всех систем организма возвращаются в исходное состояние.
Основу деятельности АНС, как и соматической, составляет трехчленная рефлекторная дуга. Вместе с тем в АНС все звенья рефлекторных дуг имеют свои особенности.
Чувствительное звено. В соматической нервной системе оно представлено только псевдоуниполярными нейронами спинномозговых узлов и аналогичных узлов черепномозговых нервов, а в АНС чувствительное звено включает три вида клеток:
1. Часть псевдоуниполярных нейронов спинальных и черепномозговых чувствительных узлов образует рецепторы в органах, иннервируемых АНС. Эти узлы достаточно описаны в общих учебниках гистологии.
2. Чувствительные клетки узлов блуждающих нервов, по строению близкие к нейронам спинномозговых узлов.
3. Клетки Догеля II типа, расположенные во многих узлах АНС. Их стуктурнофункциснальная характеристика приводится ниже.
Рецепторы в автономной нервной системе, как и в соматической, представлены свободными и несвободными нервными окончаниями, которые описаны во всех учебниках гистологии. У человека интероцепторы располагаются во всех висцеральных органах: сосудах, сердце, легких, почках, печени и др. В крупных вегетативных ганглиях также находятся свободные рецепторные окончания. Интероцепторы воспринимают механические, химические, температурные стимулы, а также изменение осмотического давления, параметров метаболизма, ток жидкости и т.д.
Информация, поступающая от висцеральных рецепторов, используется главным образом для вегетативных регуляторных процессов, управляющих кровообращением, дыханием, пищеварением, электролитным и водным балансом. Это в основном бессознательные функции, но в некоторой степени активность висцеральных афферентов воспринимается сознательно. Так, сильная потенциально вредная стимуляция внутренних органов воспринимается как боль. Ощущение голода, жажды, позывы на мочеиспускание и дефекацию – это также случаи сознательного восприятия афферентной висцеральной информации. Кроме этих конкретных сознательных восприятий и полностью бессознательных регуляторных реакций, сигналы рецепторов внутренних органов вызывают также неспецифические приятные и неприятные ощущения, в общем определяемые как самочувствие и обычно сильно влияющие на эмоциональное состояние.
В сердечно-сосудистой системе регулирование артериального давления (АД) и объема циркулирующей крови осуществляется с участием волюморецепторов дуги аорты, каротидного синуса, сонных артерий, предсердных и легочных вен. Активация волюморецепторов дуги аорты и каротидного синуса через сосудодвигательный центр продолговатого мозга ослабляет сопротивление периферических сосудов (снижает артериальное давление), рефлекторно усиливает выделение натрия почками и как следствие – уменьшает объем циркулирующей воды. Возбуждение волюморецепторов предсердий по афферентным волокнам блуждающих нервов передается в сосудодвигательный центр, который ослабляет тонус симпатических волокон почек, уменьшает выделение ренина, величину артериального давления и соответственно повышает скорость клубочковой фильтрации.
В дыхательной системе имеются разнообразные рецепторы, участвующие в регуляции ее функции. Это – хеморецепторы артериальных сосудов, возбуждающиеся при снижении содержания О2 и повышении концентрации СО2, а также механорецепторы, связанные с гладкими миоцитами воздухоносных путей, реагирующие на растяжение легких при вдохе. Кроме того, имеются поверхностные (ирритантные) рецепторы слизистых оболочек и юкстакапиллярные рецепторы альвеол. Первые реагируют на изменение объема легких при вдохе и выдохе, концентрации СО2, на асфиксию и содержание раздражающих паров, а юкстакапиллярные являются специфическими рецепторами спадения легких.
Как отмечено выше, в регулировании функции почек автономной нервной системой участвуют сигналы механо- и осморецепторов, расположенных в различных органах. Кроме того, в капсуле почек также имеются волюморецепторы. При увеличении интерстициального гидростатического давления (повышении содержания воды в почке) растяжение капсулы возбуждает эти рецепторы, что рефлекторно усиливает выделение натрия.
В печени имеется ряд популяций специфических рецепторов: волюмо-, осмо-, натрий- и калий чувствительных. Они имеют различные функциональные значения: участвуют в регулировании количества крови, протекающей через орган, общего объема циркулирующей крови, служат информационным звеном в осморегуляции.
В желудочно-кишечном тракте содержатся рецепторы, воспринимающие механические, химические, температурные стимулы и движение жидкости. Из механических здесь наиболее развиты рецепторы растяжения. Они участвуют в регулировании двигательной, секреторной функции желудка и тонкого кишечника, опорожнении толстой кишки. Стимуляция рецепторов растяжения в желудке вызывает чувство сытости, в кишечнике – чувство закупорки, в концевом участке подвздошной кишки – расслабление илеоцекального сфинктера и эвакуацию химуса в толстый кишечник. Сильное растяжение желудка и кишечника вызывает боль, которую пострадавшие иногда локализуют в зонах Геда на поверхности кожи. Боль от сильного растяжения возникает и в других органах (в желчном и мочевом пузыре, почечной лоханке и т.д.). Однако при этом болевая реакция возникает не от возбуждения рецепторов растяжения, а имеет собственные специализированные ноцицепторы. Поскольку боль является универсальной защитной реакцией, сигнализирующей о повреждении или потенциальной опасности повреждения тканей, рецепторы боли рассеяны в организме повсюду, и во внутренних органах они содержатся в значительных количествах. Гистологически они представляют собой неинкапсулированные нервные окончания, их ультраструктура и локализация изучены слабо. Предположительно они находятся в адвентициальной оболочке мелких кровеносных и лимфатических сосудов, в эндоневрии и других соединительнотканных промежутках. По некоторым данным, тонкие ветвления дендритов в многослойных эпителиях также являются ноцицепторами. Механизм возникновения потенциала в ноцицепторах сложнее, чем в других рецепторах. Здесь пусковым моментом служит появление повреждающих факторов (патогенных микроорганизмов, ишемии, сильных механических, химических и других воздействий), обусловливающих выделение активных веществ (простогландинов и брадикининов), которые вызывают раздражение ноцицепторов. Появление потенциала у ноцицепторов не регистрируется электрофизиологическими методами, потенциалы действия обнаруживаются только в соответствующих афферентных волокнах. Студентам-медикам и практикующим врачам полезно знать, что здоровая ткань содержит ноцицепторы, как правило, с высоким порогом возбуждения. Если же ткань патологически изменена, ноцицепторы сенситизируются, т.е. их пороги возбуждения могут снижаться настолько, что совершенно безвредные в норме воздействия будут вызывать острую боль.
Проводниками болевых сигналов являются только нервные волокна двух типов – тонкие миелинизированные (группа Аб) и безмиелиновые (группа С). Скорости проведения импульса у первых 2,5 – 20 м/с, у вторых - в среднем 1 м/с. В скелетных мышцах, суставах и других глубоких тканях импульсы от ноцицепторов отводятся волокнами группы Аб., а висцеральная боль – волокнами группы С.
Ассоциативное звено. В автономной рефлекторной дуге, в отличие от соматической, сигналы от афферентных клеток на эфферентные передаются не только на спинномозговом и супраспинальном уровнях, но и в ганглиях, являющихся низшими нервными центрами. В последних эта передача может проходить как через вставочные клетки, так и без них – путем непосредственной связи чувствительного нейрона с эфферентным (например, синапсы между клетками Догеля II и I типа).
В передаче сигналов на спинномозговом уровне также имеется отличие между автономной и соматической нервной системой. Так, если в соматической нервной системе существуют часто используемые в неврологической практике моносинаптические спинальные рефлексы с прямой передачей импульса от чувствительного нейрона на эфферентный (сухожильные или Т-рефлексы растяжения: коленный, подбородочный, локтевой и др.), в автономной нервной системе даже простейшие спинномозговые рефлексы не имеют прямых переключений с афферентных волокон на преганглионарные нейроны. Самый короткий путь между ними включает две передачи: 1) от афферентного волокна на ассоциотивный нейрон; 2) от ассоциативного нейрона на преганглионарный (Рис.1). Таким образом, в дуге спинального автономного рефлекса между афферентным и эфферентным нейроном имеется не менее трех синапсов, два из которых лежат в спином мозге, а один - в вегетативном ганглии (где расположен эфферентный нейрон).
Следует иметь в виду, что в спинном мозге в передаче сигнала от афферентного волокна на преганглионарный нейрон участвует не одна, а ряд ассоциативных клеток, причем каждая из них может иметь несколько афферентных входов. Среди этих вставочных клеток имеются нейроны, способные к суммации висцеральных и соматических влияний. В некоторых из них афферентные сигналы могут вызывать либо возбуждение, либо торможение, т.е. отдельные сигналы подавляются, чем облегчается прохождение других.
В образовании автономных рефлекторных дуг спинального уровня участвует лишь часть афферентных волокон, вступающих в спинной мозг. Остальные включаются в состав проприоспинальных и восходящих путей; последние завершаются проекцией висцеральных сигналов в коре мозга. По современным представлениям проекционные пути включают три нейрона. Первый из них – чувствительный – расположен в спинномозговом или вегетативном ганглии, а остальные – переключательные: один в клиновидном или тонком ядре продолговатого мозга, второй – в вентральном заднелатеральном ядре таламуса, аксон которого проецируется в соматосенсорную зону коры мозга. Несмотря на сложность многоступенчатой организации передачи афферентных сигналов, принципы межнейронного взаимодействия на всех уровнях одни и те же: конвергенция на центральных клетках висцеральных и соматических сигналов, их оценка аппаратом суммации и по ее результатам генерация нового сигнала. Висцеральная информация, поступающая в высшие центры, участвует вместе с соматической в возникновении эмоций, мотивации поступков и в формировании механизмов целенаправленного поведения. Для чувствительной и эфферентной вегетативной иннервации некоторых органов характерна сегментарная организация. Афферентные волокна от сердца, ЖКТ и выделительных органов переключаются в пределах сегментов спинного мозга на преганглионарные симпатические и парасимпатические нейроны, иннервирующие эти же органы (кишечно-кишечные, кардио-кардиальные, эвакуаторные рефлексы). Проявления этой сегментарной организации иннервации внутренних органов наблюдаются в клинике. При заболевании этих органов (холецистите, аппендиците), возникает напряжение мышц брюшной стенки в области локализации патологического процесса и покраснение кожи в участке (дерматоме), иннервируемом афферентами и эфферентами того же сегмента спинного мозга. Защитное сокращение мышц живота обусловлено возбуждающим действием чувствительных волокон от пораженного органа на мотонейроны, а покраснение кожи – тормозным действием афферентных волокон от этих органов на симпатические сосудосуживающие волокна того же сегмента. В связи с этими явлениями можно отметить, что раздражение терморецепторов кожи вызывает через симпатические нейроны
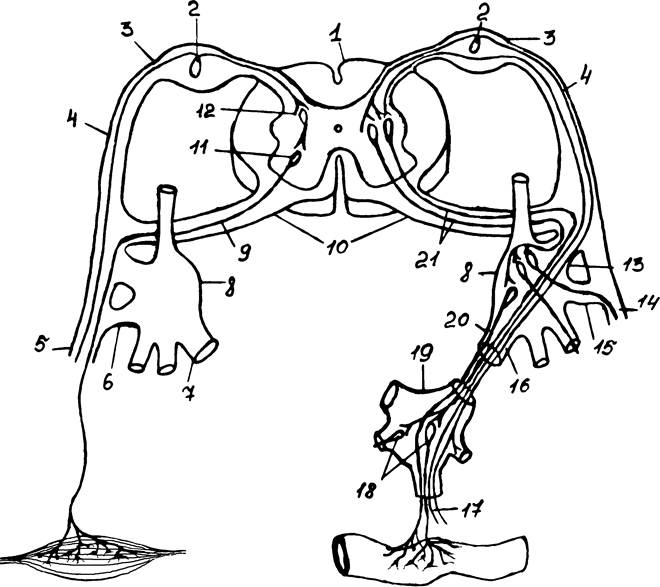
Рис. 1. Рефлекторные дуги спинномозгового уровня соматической и автономной нервных систем.
1 – спинной мозг; 2 – чувствительный нейрон; 3 – спинальный ганглий; 4 – дорсальный корешок; 5 – соматический нерв; 6 – серая соединительная ветвь; 7 – висцеральная ветвь; 8 – паравертебральный узел (узел пограничного симпатического ствола); 9 – двигательное соматическое волокно; 10 – вентральный корешок; 11 – двигательный нейрон соматической рефлекторной дуги; 12 – вставочный нейрон соматической рефлекторной дуги; 13 – белая соединительная ветвь; 14 – соматический нерв; 15 – серая соединительная ветвь; 16 – висцеральная ветвь; 17 – постганглионарное волокно; 18 – двигательный (постганглионарный) нейрон дуги автономного рефлекса; 19 – превертебральный узел (узел брыжеечного сплетения); 20 – постганглионарное волокно; 21 – преганглионарное волокно. [20]
торможение двигательной активности органов ЖКТ, иннервируемых из одноименных сегментов спинного мозга. Описанные выше факты представляют собой проявления взаимодействия вегетативной нервной системы с соматической в виде разнообразных висцеро-соматических и соматовисцеральных реакций.
Как известно, чувствительные волокна (афференты) – от кожи, мышц, суставов, внутренних органов – входят в спинной мозг по задним корешкам. Кожные афференты от каждого заднего корешка иннервируют ограниченную область кожи, называемую дерматомом. И соответственно висцеральные афференты каждого корешка иннервируют определенные внутренние органы. Как отмечено выше, в задних рогах спинного мозга на одном ассоциативном нейроне могут конвергировать афферентные волокна от внутренних органов и соматические, в том числе кожные. Поэтому отдельные внутренние органы связаны с определенными участками кожи, которые названы зонами Геда. Следовательно, зоны Геда соответствуют дерматомам, связанным с сегментами спинного мозга, иннервирующими тот или иной орган. Следует иметь в виду, что смежные дерматомы перекрываются, так как один периферический нерв содержит волокна нескольких соседних задних корешков, а один задний корешок – волокна разных нервов. Знание зон Геда довольно широко используется в практике. Многие больные, страдающие заболеваниями внутренних органов (ишемической болезнью сердца, холециститом, язвенной болезнью желудка и т.д.), жалуются на боли в этих зонах, что помогает диагностике.
Имеют место и случаи непосредственной связи висцеральной и кожной болевой чувствительности, являющиеся структурной основой отраженной боли: иногда ветви одного болевого афферентного волокна, иннервируют и кожу, и внутренние органы.
Эфферентное звено автономной нервной системы представлено эффекторными нейронами, расположенными в симпатических (пара- и превертебральных), парасимпатических и метасимпатических нервных узлах. Аксоны этих нейронов образуют постганглионарные безмиелиновые эфферентные волокна, которые в составе смешанных нервов направляются к своим мишеням. Они иннервируют большинство органов и тканей.
Эффекторный нейрон вегетативного узла получает ряд входных сигналов. Основной сигнал, возбуждающий, холинергический, поступает из центральных преганглионарных нейронов: симпатических, расположенных в спинном мозге, и парасимпатических, находящихся в стволе головного мозга; возбуждение самих преганглионарных волокон происходит в результате интегративных процессов в ЦНС. Остальные входные сигналы передаются эффекторному нейрону от чувствительных и вставочных нейронов самого узла (в том числе от МЦФ-клеток), а также от афферентных волокон, поступающих из других узлов. Наличие в вегетативных узлах афферентных окончаний, которые обычно локализуются в строме и вокруг тел нейронов, впервые было установлено отечественными исследователями. Обнаружение этого факта внесло существенные изменения в концепцию Ленгли о строении эфферентного звена АНС.
Эфферентным клеткам узлов АНС, как и нейронам ЦНС, свойственна интегративная деятельность: они обрабатывают, синтезируют все входные сигналы и в результате этого генерируют свой эффекторный импульс, передаваемый иннервируемым образованиям. Как правило, на каждом эффекторном нейроне находится множество синапсов. Среди них имеются аксодендритные, аксоаксональные, аксосоматические и дендродендритные десмосомоподобные контакты. Так как в нервных узлах концентрируется большое количество нервных волокон, образуется ганглионарный нейропиль, во многом не уступающий нейропилю в ЦНС. Вместе в тем синаптический аппарат эфферентных нейронов АНС устроен проще, чем у большинства клеток ЦНС. В некоторых узлах на каждом нейроне образует синапс только одно преганглионарное волокно. В узлах АНС отсутствуют аксошипиковые синапсы, и вообще шипиковый аппарат такого строения, как в ЦНС, у вегетативных нейронов не встречается. Тем не менее, аксодендритные и аксосоматические синапсы в этих узлах по основным структурным элементам аналогичны синапсам ЦНС: у них имеются пресинаптические плотные выступы и постсинаптическая «специализация» электронно-плотного материала (постсинаптическое уплотнение).
Эфферентное звено АНС существенно отличается от соматического строением терминальных отделов: аксоны вегетативных нейронов, в частности клеток Догеля I типа, не образуют прямых контактов с иннервируемыми тканями – непосредственно не соприкасаются с ними и не образуют специализированных окончаний на подобие моторных бляшек в скелетной мускулатуре. Терминальные части аксонов вегетативных нейронов образуют небольшие расширения – варикозности диаметром 0,5 – 2 мкм, которые регулярно располагаются по длине концевых ветвлений аксона на расстоянии 5-15 мкм друг от друга. Варикозности содержат митохондрии, синаптические и другие пузырьки, а межварикозные участки – преимущественно элементы цитоскелета. Именно из варикозностей периодически выделяются нейромедиаторы, которые диффундируют в окружающие ткани. Расширенные участки терминалей не имеют цельной глиальной оболочки, которая в межварикозных участках полностью окружает и изолирует терминаль. Взаимосвязи между терминалями аксонов эфферентных нейронов и клетками-мишенями наиболее изучены в гладкомышечной ткани внутренних органов, стенок сосудов и поперечнополосатой мускулатуре сердца.
Расстояния между варикозностями аксонных терминалей и мышечными клетками в тканях разных органов варьируют и составляют в среднем от 120 нм до 1 и более микрометров. Такая структурная особенность взаимосвязи аксонных терминалей и мышечной ткани приводит к тому, что выделяющиеся из варикозностей нейромедиаторы диффундируют в межклеточном пространстве и вследствие этого оказывают влияние на целые группы эффекторных клеток. Часть молекул медиатора взаимодействует с рецепторами мембран рабочих клеток, а оставшиеся захватываются нервными терминалями и используются при передаче последующих импульсов. Плотность расположения эфферентых терминалей в гладкой мышечной ткани в различных органах существенно отличается. По этому критерию выделяют 3 группы: А, В и С. В группе А каждая гладкомышечная клетка (ГМК) иннервирована индивидуально одним или несколькими плотными нейромышечными контактами с расстоянием между ГМК и варикозностями аксонов 20 нм. В данном случае обеспечивается возможность непосредственной активации каждой ГМК нервным импульсом и отсутствует межклеточное проведение возбуждения. Сюда относятся гладкие мышцы большинства сосудов и сфинктера зрачка. Даже внутри группы А количество нервно-мышечных контактов на одну ГМК варьирует в различных органах в широких пределах. В группе В от 20 до 50% ГМК имеет плотные нейромышечные контакты (20-50 нм), а остальные получают потенциал за счет электротонической связи с этими клетками. У человека к этой группе относится гладкая мускулатура семявыносящего протока. А в группе С нейромышечные контакты имеют только отдельные («ключевые») клетки. На часть других миоцитов потенциал передается через щелевые соединения, но большинство клеток этой группы активируется либо электрически, либо из варикозностей, расположенных на расстоянии более 100 нм. В эту группу входит мышечная ткань кишечника и матки.
Концевые аппараты аксонов эфферентных нейронов АНС большей частью являются адренергическими и холинергическими. Наряду с этим в метасимпатической системе в качестве медиатора передачи нервного импульса часто выступают АТФ и серотонин. Кроме того, имеются пептидергические нейроны, которые передают импульс клеткам-мишеням посредством вазоинтестинального пептида (ВИП) и нейропептида Y. В последнее время в числе кандидатов в медиаторы в АНС рассматриваются и другие вещества: соматостатин, холецистокинин, вещество Р, гистамин, глицин, гамма-аминомасляная кислота.
Таким образом, АНС, кроме ряда структурных особенностей рефлекторных дуг, отличается от соматической нервной системы значительным разнообразием нейронов эфферентного звена, использующих в качестве медиатора передачи импульсов широкий круг различных веществ.
Поиск по сайту: