 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
ДИАГРАММА «ЖЕЛЕЗО – УГЛЕРОД (ЦЕМЕНТИТ)»
5.1. Компоненты, фазы и структурные составляющие
железоуглеродистых сплавов
Железоуглеродистые сплавы – стали и чугуны – являются основными, наиболее распространенными материалами, используемыми в различных отраслях промышленности. Эти сплавы описываются диаграммой состояния «Железо – углерод (цементит)» («Fe – Fe3C») (рис. 5.1).
Основными компонентами диаграммы являются железо и углерод. Температура плавления железа 1539 °С. В твердом состоянии оно может находиться в двух модификациях: α (решетка ОЦК) и γ (решетка ГЦК). Модификация Feα существует при температурах до 911°С и от 1392 °С до 1539°С. Важной особенностью Feα является его ферромагнетизм ниже температуры 768°С (точка Кюри). Модификация Feγ существует в интервале температур 911°С–1392°С.
Железо с углеродом образует растворы внедрения. Растворимость углерода в железе зависит от температуры и от того, в какой кристаллической форме существует железо. Твердый раствор углерода в Feα называется ферритом, а в Feγ – аустенитом.
|

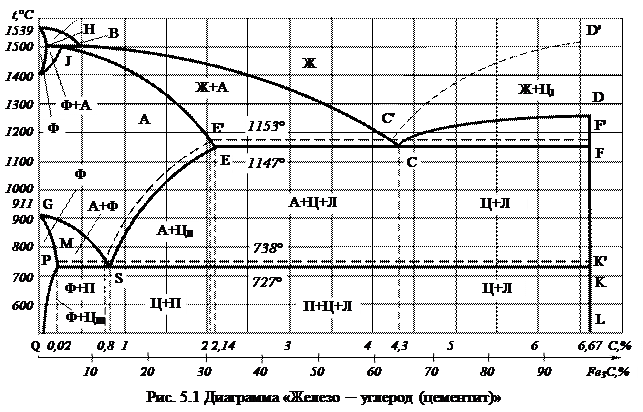

Содержание углерода в диаграмме «Железо – углерод» ограничивается 6,67%, т. к. при этой концентрации образуется химическое соединение Fe3C – цементит. Так как на практике применяют железоуглеродистые сплавы с содержанием углерода не более 5%, то цементит является вторым компонентом рассматриваемой диаграммы. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение для получения высокоуглеродистых сплавов – серых чугунов.
В сплавах «Fe – C» существуют две высокоуглеродистые фазы: метастабильная – цементит и стабильная – графит. Поэтому различают две диаграммы состояния (рис. 5.1) – метастабильную «Железо – цементит» и стабильную «Железо – графит» (на рисунке показана пунктирными линиями).
Координаты характерных точек диаграммы «Железо – цементит» приведены в таблице 5.1
Таблица 5.1.
Критические точки диаграммы «Железо – цементит»
| Обозначение точки | Т, °С | С,% | Обозначение точки | Т, °С | С,% |
| А | F | 6,67 | |||
| Н | 0,1 | G | |||
| I | 0,16 | P | 0,02 | ||
| B | 0,51 | S | 0,8 | ||
| N | K | 6,67 | |||
| D | 6,67 | Q | ≈ 600 | 0,01 | |
| E | 2,14 | L | ≈ 600 | 6,67 | |
| C | 4,3 |
Точка А определяет температуру плавления чистого железа, точка D – цементита. Точки N и G соответствуют температурам полиморфных превращений железа. Точки Н и P характеризуют предельную концентрацию углерода соответственно в высокотемпературном и низкотемпературном феррите. Точка Е определяет наибольшую концентрацию углерода в аустените.
Превращения в сплавах системы «Fe – Fe3C» происходят как при затвердевании жидкой фазы, так и в твердом состоянии.
Первичная кристаллизация идет в интервале температур, определяемых линиями ABCD (ликвидус) и AHIECF (солидус). Вторичная кристаллизация вызвана превращением железа одной модификации в другую и переменной растворимостью углерода в аустените и феррите, при понижении температуры растворимость уменьшается. Избыток углерода из твердых растворов выделяется в виде цементита. Линии ES и PQ характеризуют изменение концентрации углерода в аустените (ES) и феррите (PQ).
В системе «Fe – Fe3C» происходят три изотермических превращения:
при t = 1499 °С, линия HIB – перитектическое превращение:
ФН + ЖВ → АI;
при t = 1147 °С, линия ECF – эвтектическое превращение:
ЖС → АЕ + Ц;
при t = 727 °С, линия PSK – эвтектоидное превращение:
АS → ФР + Ц → П.
Структурными составляющими данной системы являются: феррит (Ф), аустенит (А), цементит (Ц), перлит (П), ледебурит (Л).
Феррит – твердый растворвнедрения углерода в Feα, – мягкая, пластичная фаза (σВ = 300 МПа, δ = 40%, ψ = 70%, 650–1000 HB). Различают низкотемпературный и высокотемпературный феррит. Предельная концентрация углерода в низкотемпературном феррите 0,02 % (P), в высокотемпературном – 0,1 % (H). Феррит магнитен до 768 ºС (линия МО).
Аустенит – твердый растворвнедрения углерода в Feγ, – более твердыйи пластичный (δ = 40–50%, 2000–2500 НВ), не магнитен. Предельная концентрация углерода достигает 2,14% (Е).
Цементит – химическое соединение Fe3C, – имеет сложную кристаллическую решетку. Температура плавления цементита около 1250 °С. Полиморфных превращений не испытывает, но при низких температурах слабоферромагнитен. Цементит имеет высокую твердость (8000 НВ), но практически нулевую пластичность.
Перлит – эвтектоидная смесь феррита и цементита, – чаще всего имеет пластичное строение, при котором кристаллы цементита перемежаются с кристаллами феррита,и является прочной структурной составляющей (σВ = 800–900 МПа, δ = 16%, 1800 HB).
Ледебурит – э втектическая смесь аустенита и цементита в интервале температур 1147 – 727°С, а ниже линии SK (727 °С) – смесь перлита и цементита. Ледебурит имеет высокую твердость > 6000 HB, но хрупок.
Железоуглеродистые сплавы подразделяют на техническое железо, стали и чугуны.
Техническое железо – сплавы железа с углеродом, содержащие до 0,02% С.
Стали – сплавы железа с углеродом, содержащие от 0,02 до 2,14% С.
Чугуны – сплавы железа с углеродом, содержащие свыше 2,14 % С.
Поиск по сайту: