 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Небелковые антигены загружаются на не-HLA-антигенпредстав- ляющие молекулы CD1
В целом макрофаги и В-клетки вовлечены, соответственно, в Т-клеточный или гуморальный иммунный ответ по пути, опосредованному HLA II, а дендритные клетки двух типов способны к перекрестной презентации. Дендритная клетка типа 1 осуществляет процессинг эндогенных антигенов по пути с HLA I для запуска Т-клеточного ответа, а дендритная клетка типа 2 процессирует экзогенные антигены по пути с HLA II и включает В-клеточный ответ.
Вторая стадия иммунного ответа (распознавание антигена) протекает в течение нескольких часов. Однако при нарушениях клеточной миграции и межклеточных взаимодействий она может быть более длительной. Возможно, это приводит к замедлению всего иммунного ответа на патоген. Клиническими проявлениями этой стадии являются повышение температуры тела, мышечная слабость, снижение аппетита и сонливость. По большей части они обусловлены системными эффектами цитокинов (см. ниже).
Для того чтобы мог стартовать специфический иммунный ответ на конкретный антиген, необходимо, чтобы Т- и В-лимфоциты соответствующего клона встретились с антигенпредставляющей клеткой. Некоторые антигены бактерий (T-независимые антигены) распознаются с помощью BCR B-клеток и не требуют помощи со стороны Т-хелперов. Большинство нативных антигенов (так называемых T-зависимых антигенов) полностью распознаются «наивными» CD4+ Th1 и CD8+ T-клетками (для включения Т-клеточного ответа или пути Th1), а также «нaивными» CD4+ Th2 (для включения гуморального ответа или пути Th2). Интересно, что для прайминга CD8+ Т-клеток необходимо участие CD4+ Th1.
Третья стадия (сигнальная трансдукция и активация лимфоцитов). Во время распознавания лимфоциты воспринимают три типа обязательных сигналов, один специфический и два неспецифических:
1. Aнтигенный пептид/HLA I или антигенный пептид/HLA II.
2. Цитокины.
3. Костимулирующие молекулы.
Антигенный пептид, загружаемый на HLA I или HLA II в результате процессинга, служит специфическим сигналом. Это одновременное «двойное» распознавание «своего» (белков HLA) и «несвоего» (антигена) было открыто нобелевскими лауреатами (1996) P.C. Doherty (Австралия, США) и R.M. Zinkernagel (Швейцария) и оказалось довольно универсальным явлением. Секретируемые цитокины и экспрессируемые костимулирующие молекулы являются двумя обязательными неспецифическими сигналами. Более того, для обеспечения надежного физического контакта клеток необходимо также взаимодействие таких адгезивных молекул, как LFA-1, ICAM-1, ICAM-2, ICAM-3.
Цитокины играют одну из ключевых ролей в неспецифической регуляции иммунного ответа. Т- и В-лимфоциты получают цитокиновые сигналы от антигенпредставляющих клеток, NK-клеток,
тучных клеток и др. Обратный сигнал от лимфоцитов, например секретируемый IFN-γ, способствует реэкспрессии HLA I/HLA II на антигенпредставляющих клетках. Цитокины, действующие на ранних стадиях иммунного ответа, могут быть разделены на две группы в зависимости от его направления:
1. Th1-цитокины: IL-2, IL-12, IL-18, IFN-γ, TNF-α/β (для пути Т-хелперов типа 1).
2. Th2-цитокины: IL-4, IL-13 (для пути Т-хелперов типа 2). Однако на следующих стадиях иммунного ответа (клональная
экспансия, созревание эффекторов, переключение синтеза изотипов антител) в процесс вовлекаются другие цитокины.
Костимулирующие молекулы также играют важную роль в неспецифической регуляции иммунного ответа (табл. 7-2).
Таблица 7-2. Костимулирующие молекулы при иммунном ответе
| Клетка | Молекула | Функция |
| Антигенпредставляющие клетки | B7.1, B7.2 | Лиганды для CD28, CTLA-4 |
| Т-хелпер 1 | CD28 CTLA-4 (CD152) | Активационный сигнал Ингибирующий сигнал |
| Т-хелпер 2 | CD28 CTLA-4 (CD152) | Ингибирующий сигнал Активационный сигнал |
| В-лимфоцит | CD40 CD22 | Активационный сигнал на переключение синтеза различных классов антител Ингибирующий сигнал |
Активация клеток является результатом сигнальной трансдукции, которая осуществляется серией сложных внутриклеточных реакций. После распознавания первоначально происходит активация связанных с корецепторами и молекулами CD3 (на Т-клетках) или CD79 (на В-клетках) тирозинкиназ нескольких семейств (Lck, Fyn, Blk, Btk, Lyn, Zap70, Syk и др.), затем через посредничество адаптерных белков включаются сигнальные пути. Один из них связан с активацией фосфолипазы Cγ, образованием инозитолтрифосфата и диацилглицерола, активацией протеинкиназы С и мобилизацией внутриклеточного Ca2+, с транскрипцией гена IL-2. Данный цитокин является ключевым ростовым фактором для лимфоцитов в иммунном ответе. Второй сигнальный путь связан
с обменом арахидоновой кислоты и приводит к транскрипции генов структурных белков, необходимых для осуществления митозов клеток.
Четвертая (клональная экспансия лимфоцитов) и пятая (созревание эффекторных лимфоцитов и клеток памяти) стадии иммунного ответа. Клональная экспансия представляет собой пролиферацию активированных лимфоцитов, которая протекает в периферических органах иммунной системы. Пролиферирующие В-лимфоциты образуют вторичные фолликулы в лимфатических узлах (центробластная стадия), при этом размножение клеток регулируется рядом цитокинов: IL-2, IL-4, IL-5, IL-6, IL-10, IL-13, IL-14, IFN-γ, TNF и др. В последующем центробласты начинают превращаться в центроциты, которые мигрируют на периферию фолликулов (центроцитарная стадия). В этот момент клетки вступают в период соматических гипермутаций, который является своеобразным способом селекции нужной специфичности BCR. Происходит позитивный отбор клеток с высокоспецифичным BCR и негативный отбор В-лимфоцитов с низкоспецифичным рецептором. В процессе созревания В-клетки претерпевают морфологические изменения (плазмобласт (иммунобласт) - проплазмоцит (лимфоплазмоидная клетка) - плазмоцит) и мигрируют в костный мозг и MALT для синтеза антител различных классов. Синтез ранних антител (IgM) регистрируется уже к концу первых суток клинического инфекционного эпизода, а высокоспецифических IgG - на 5-7 сутки.
Клональная экспансия и созревание Т-клеток протекают в паракортикальных зонах лимфатических узлов и периартериолярных пространствах селезенки. Распознавшие антиген клетки вступают в пролиферацию и превращаются в лимфобласты. Клоны CD8+ T-клеток нарастают быстро, а клоны CD4+ Т-лимфоцитов - более медленно. В целом, клональная экспансия и дифференцировка регулируются разными цитокинами (IL-2, IL-7, IL-9, IL-12, IL-15, IFN-γ, TNF и др.) и адгезивными молекулами. В процессе дифференцировки значительно изменяется фенотип Т-лимфоцитов, но, в отличие от В-лимфоцитов, они не меняются морфологически.
Характерным клиническим эквивалентом стадий клональной экспансии и дифференцировки является увеличение периферических лимфатических узлов, миндалин, видимых лимфатических фолликулов и селезенки. Можно наблюдать эти симптомы при респираторной, урогенитальной или значительной системной инфекциях.
В процессе иммунного ответа наряду с эффекторными клетками формируются Т- и В-клетки памяти. В отличие от эффекторных лимфоцитов с небольшими сроками жизни, клетки памяти остаются жизнеспособными в течение длительного времени (пожизненно). Существуют CD4+ и CD8+ T-клетки памяти, В-клетки памяти и долгоживущие плазматические клетки. В отличие от наивных Т-лимфоцитов Т-клетки памяти характеризуются фенотипом CD45RO+, CD44hi, быстрым HLA-независимым циклом и способностью секретировать большие количества цитокинов. Долгоживущие плазматические клетки обеспечивают дополнительный механизм поддержания синтеза иммуноглобулинов без дополнительной антигенной стимуляции в течение 1,5 лет.
Вторичный иммунный ответ протекает в ускоренном режиме за счет клеток памяти (рис. 7-3). Появление IgM в сыворотке крови часто указывает на «свежую» инфекцию или реактивацию персистирующего патогена, а синтез IgG соответствует наличию иммунной памяти к однажды перенесенной инфекции. При таком ускоренном синтезе IgG клинические проявления инфекционной болезни обычно отсутствуют.
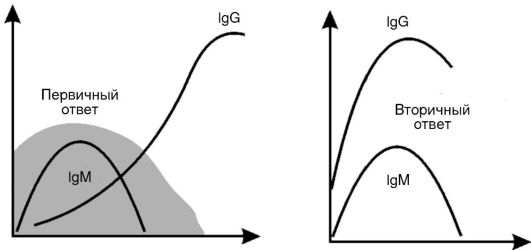 Рис. 7-3. Первичный и вторичный гуморальный ответ. В первом случае нарастание IgG отстает от нарастания IgM, при этом, поскольку IgM является низкоспецифичным по отношению к патогену, отмечаются все симптомы инфекционного заболевания (выделено серым). При вторичном ответе патоген связывается сразу высокоспецифичными антителами класса IgG, поэтому клинических проявлений болезни нет. По горизонтали - время (сутки); по вертикали - содержание иммуноглобулинов (г/л)
Рис. 7-3. Первичный и вторичный гуморальный ответ. В первом случае нарастание IgG отстает от нарастания IgM, при этом, поскольку IgM является низкоспецифичным по отношению к патогену, отмечаются все симптомы инфекционного заболевания (выделено серым). При вторичном ответе патоген связывается сразу высокоспецифичными антителами класса IgG, поэтому клинических проявлений болезни нет. По горизонтали - время (сутки); по вертикали - содержание иммуноглобулинов (г/л)
Шестая стадия иммунного ответа (эффекторная активность). Конечной стадией как гуморального, так и клеточного иммунного ответа является деструкция антигена, которая осуществляется с привлечением неспецифических факторов врожденного иммунитета. Известны следующие эффекторные механизмы деструкции антигена.
При иммунном ответе гуморального типа:
1. Простая нейтрализация антигена антителами при образовании иммунных комплексов «антиген + антитело» (АГ+АТ).
2. Комплементзависимый лизис антигена, связанного с антителом. Иммунные комплексы АГ+АТ, фиксированные на поверхности клеток-мишеней, присоединяют и активируют комплемент по классическому пути.
3. Фагоцитоз растворимых иммунных комплексов АГ+АТ с последующим их расщеплением в лизосомах фагоцитов.
4. Антителозависимая клеточная цитотоксичность (АЗКЦ). Реализуется путем разрушения клетками-киллерами (К-клетками) покрытых антителами (IgG) клеток-мишеней через присоединение к Fc-фрагменту IgG. Такими К-киллерами могут быть гранулоциты, макрофаги, тромбоциты, NK-клетки (натуральные киллеры).
При иммунном ответе клеточного типа:
1. Цитолиз и апоптоз клеток-мишеней. Цитотоксические Т-лимфоциты лизируют клетки-мишени с помощью белков - перфоринов. Перфорины - мономерные белки, способные встраивать в клеточную мембрану клетки-мишени и при полимеризации в присутствии Са2+ образовывать в ней каналы (поры), повышая тем самым ее проницаемость для Na+ и воды. В результате клетка-мишень набухает, происходит разрыв ее мембраны и гибель (осмотический лизис). Наряду с этим через поры, образованные перфоринами, в клетку-мишень поступают секретируемые цитотоксическими лимфоцитами TNF-β (лимфотоксин) и гранзимы (сериновые протеазы), запускающие механизм естественной клеточной гибели (перфорин-гранзимовый путь апоптоза). При этом сами цитотоксические Т-лимфоциты за счет синтеза специфических эндогенных ингибиторов сериновых протеаз нечувствительны к воздействию гранзимов. Реализация цитотоксичности Т-лимфоцитов может быть связана также с синтезом IFN-γ (ингибирует репликацию вирусов, активирует экспрессию HLA I/II и процесс распознавания вирусов и вирусинфицированных клеток Т-лимфоцитами) и индукцией рецепторзависимого апоптоза. Его развитие обусловливается лиганд-
рецепторным взаимодействием между Fas-рецептором (CD95), экспрессируемым клеткой-мишенью, и Fas-лигандом (Fas-L) Т-киллера либо посредством секреции Т-киллером TNF-α, активирующего TNF-R-ассоциированный домен смерти (TRADD - TNF-R-associated death domain) при связывании со специфическим рецептором TNF-R1 на клетке-мишени. Кроме того, проапоптотическое действие цитотоксических лимфоцитов может быть опосредовано увеличением проницаемости митохондриальных мембран клеток-мишеней, снижением трансмембранного потенциала митохондрий и выходом в цитоплазму клеток различных апоптогенных факторов, например цитохрома С и апоптозиндуцирующего фактора (AIF - apoptosis induced factor), активирующих каспазы (цистеиновые протеазы). Процедура апоптоза включает фрагментацию ДНК, конденсацию хроматина, блеббинг (образование вздутий - пузырей) мембраны, сокращение клетки, ее дезорганизацию и упаковку в апоптотические тельца. На поверхности апоптотирующих клеток экспрессируются молекулы, распознаваемые фагоцитами (фосфосерин, тромбоспондин, десиалированные мембранные гликоконъюгаты). За счет этого апоптотические клетки и тельца подвергаются фагоцитозу и разрушению лизосомальными факторами фагоцитов.
2. CD4+ Т-лимфоциты, ответственные за гиперчувствительность замедленного типа, с помощью секретируемых цитокинов (прежде всего IFN-γ) инициируют миграцию макрофагов и нейтрофилов в очаг иммунного воспаления и их активацию в очаге. Активированные макрофаги и нейтрофилы разрушают клетки-мишени путем фагоцитоза.
Поиск по сайту: