 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
ОПРЕДЕЛЕНИЕ ТЕПЛОЕМКОСТИ ВОЗДУХА
Цель работы: познакомиться с процессом изобарического нагревания воздуха, определить молярную теплоемкость воздуха при изобарическом нагревании.
Оборудование: нагреватель, компрессор, термопара с мультиметром, блок питания, амперметр и вольтметр.
ТЕОРЕТИЧЕСКОЕ ВВЕДЕНИЕ
Теплоемкость – это теплофизический параметр веществ, определяемый как количество теплоты, необходимое для нагревания некоторой массы вещества на один Кельвин. Если масса вещества равна одному килограмму, то теплоемкость называется удельной теплоемкостью, если масса равна одному моль, то – молярной теплоемкостью. По определению молярная теплоемкость равна
 . (1)
. (1)
Здесь ν = 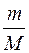 – количество вещества в моль, m – масса, M – масса одного моль, dQ – количество теплоты, достаточной для повышения температуры на dT. Для газов, в отличие от твердых и жидких тел, теплоемкость зависит от вида происходящего с газом термодинамического процесса нагревания. Это связано с тем, что, согласно первому началу термодинамики
– количество вещества в моль, m – масса, M – масса одного моль, dQ – количество теплоты, достаточной для повышения температуры на dT. Для газов, в отличие от твердых и жидких тел, теплоемкость зависит от вида происходящего с газом термодинамического процесса нагревания. Это связано с тем, что, согласно первому началу термодинамики
 , (2)
, (2)
теплота расходуется не только на повышение внутренней энергии dU, то есть на повышение температуры, но и на работу изменения объема газа. В отличие от твердых и жидких тел изменение объема может быть сравнительно большим и зависит от вида термодинамического процесса. Поэтому величина работы сил давления и количество теплоты, необходимое для нагревания газа, также зависит от вида процесса.
Рассмотрим нагревание идеального газа. Идеальный газ – это газ, собственный объем молекул которого ничтожно мал по сравнению с объемом сосуда, и потенциальная энергия взаимодействия молекул отсутствует. Воздух при нормальных условиях можно считать идеальным газом.
Приизохорическом нагревании газа изменения объема нет, работы нет, и теплота идет только на повышение внутренней энергии, dQ = dU. Для идеального газа, согласно молекулярно-кинетической теории, внутренняя энергия – это кинетическая энергия молекул  . Откуда молярная теплоемкость при изохорическом нагревании идеального газа равна
. Откуда молярная теплоемкость при изохорическом нагревании идеального газа равна  .
.
Приизобарическом нагревании газа в условиях постоянного давления дополнительно часть теплоты расходуется на работу изменения объема  . Поэтому полученное количество теплоты (dQ = dU + dA) будет равно
. Поэтому полученное количество теплоты (dQ = dU + dA) будет равно 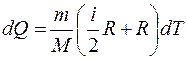 . Сравнивая с формулой (1), получим, что молярная теплоемкость при изобарическом нагревании
. Сравнивая с формулой (1), получим, что молярная теплоемкость при изобарическом нагревании
В формулах теплоемкости R – универсальная газовая постоянная, i – число степеней свободы молекулы газа. Это число независимых координат, необходимых для определения положения молекулы в пространстве. Или это число компонент энергии, которыми обладает молекула. Например, для одноатомной молекулы это составляющие кинетической энергии при поступательном движении относительно трех координатных осей, i = 3. Для двухатомной молекулы добавляются еще кинетические энергии вращательного движения относительно двух осей, так как относительно третьей, проходящей через оба атома, момент инерции и энергия отсутствуют. В итоге двухатомная молекула имеет 5 степеней свободы. Точно так же и для воздуха, состоящего в основном из двухатомных молекул кислорода и азота.
Экспериментальноеизмерение молярной теплоемкости воздуха производится с помощью калориметра. В калориметре воздух нагревается при постоянном давлении, равном атмосферному. Измерение температуры при нагреве производится с помощью термопары, подсоединенной к мультиметру. Для повышения точности измерений следует нагревать большую массу воздуха. Поэтому с помощью компрессора воздух непрерывной струей пропускается через калориметр (рис. 1).
 |
Нагреватель калориметра подключен к блоку питания. Потребляемая мощность определяется по показаниям вольтметра и амперметра N = J U. Когда после включения установки наступит тепловое равновесие и температура воздуха, выходящего из калориметра, перестанет изменяться, подводимая от электронагревателя тепловая мощность N расходуется на нагрев поступающего в калориметр воздуха и частично на теплопередачу q через стенки калориметра. Поэтому уравнение теплового баланса имеет вид
 . (3)
. (3)
Здесь m – секундный расход воздуха через калориметр, D T – повышение температуры воздуха после прохождения через калориметр.
Для исключения неизвестной мощности тепловых потерь q нужно провести опыты при разном расходе воздуха, но при одинаковом повышении температуры. При этом мощность тепловых потерь будет одинакова, потому что теплопередача через стенки пропорциональна перепаду температур. Согласно уравнению (3), подводимая к калориметру тепловая мощность, при постоянном повышении температуры воздуха Δ Т, зависит от секундного расхода воздуха линейно, и поэтому график – прямая линия. Угловой коэффициент линии равен  . Его можно определить экспериментально по графику как отношение катетов прямоугольного треугольника, построенного на экспериментальной линии, по координатам его вершин А и В. Откуда получим
. Его можно определить экспериментально по графику как отношение катетов прямоугольного треугольника, построенного на экспериментальной линии, по координатам его вершин А и В. Откуда получим
 . (4)
. (4)
ВЫПОЛНЕНИЕ РАБОТЫ
1. Измерить температуру воздуха в лаборатории термометром. Включить калориметр в сеть 220 В, установить переменным резистором компрессора сравнительно большой расход воздуха.
2. Установить переменным резистором нагревателя такую мощность, чтобы после установления теплового равновесия (3 мин) температура воздуха выходящего из калориметра повысилась бы на 30–50 К. Измерить температуру воздуха, определить по шкале резистора компрессора расход воздуха. Записать в таблицы повышение температуры, расход воздуха, показания амперметра и вольтметра.
3. Уменьшить расход воздуха примерно на одну пятую часть от начального и синхронно уменьшить мощность нагревателя так, чтобы температура воздуха на выходе из калориметра оставалась одинаковой. Эта часть работы требует терпения, плавности регулировки. Результаты измерений расхода воздуха, силы тока и напряжения записать в таблицу. Опыт провести не менее пяти раз во всем диапазоне расхода воздуха.
| Повышение температуры D Т, К | ||||||
| Расход воздуха m, г/с | ||||||
| Сила тока I, А | ||||||
| Напряжение U, В | ||||||
| Мощность N=IU, Вт |
Выключить питание мультиметров. Выключить установку.
4. Произвести расчеты. Определить мощность, потребляемую электронагревателем, N= I U. Записать в таблицу.
5. Построить график зависимости потребляемой мощности от расхода воздуха N (m). Размер графика не менее половины страницы. На осях координат нанести равномерный масштаб. Около точек провести прямую линию так, чтобы сумма отклонений точек была минимальной.
6. Построить на экспериментальной линии как на гипотенузе прямоугольный треугольник (рис. 2). Определить координаты вершин А и В треугольника. По формуле (4) рассчитать среднее значение молярной теплоемкости < CP >. Принять значение массы моля воздуха равным 28,9 10-3 кг/моль.
7. Оценить графическим методом случайную погрешность измерения молярной теплоемкости. Для этого провести на графике параллельно экспериментальной прямой две близкие линии так, чтобы все точки кроме промахов были между ними. Определить расстояние между линиями σN. Произвести расчет по формуле
 . (5)
. (5)
8. Записать результат в виде СР = <CP> ± d CP, P = 90%. Сравнить с теоретическим значением, рассчитанным по формуле (3), при R = 8,31 Дж/моль К, i = 5.
Сделать выводы.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Дайте определение молярной теплоемкости вещества.
2. Сформулируйте первое начало термодинамики. Запишите формулы для теплоты, работы, внутренней энергии идеального газа.
3. Выведите формулы для молярной теплоемкости идеального газа при изохорическом и изобарическом нагревании.
4. Запишите уравнение теплового баланса для калориметра.
5. Объясните, почему тепловые потери через стенки калориметра не влияют на измерение теплоемкости.
6. Объясните, почему в установке воздух должен непрерывной струей проходить через калориметр.
Работа 16
Поиск по сайту: