 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
КИНЕТИКА ТВЕРДОФАЗНЫХ РЕАКЦИЙ
Твердофазные гетерогенные взаимодействия, как правило, представляют собой многостадийные процессы, включающие доставку реагирующих компонентов в зону реакции, собственно химическое взаимодействие, отвод продуктов реакции, происходящий обычно по диффузионному механизму. Результирующая скорость поцесса определяется скоростью самой медленной стадии, и если это диффузия, то говорят, что процесс лимитируется диффузией и кинетика процесса - диффузионная. Если наиболее медленной стадией является химическая реакция, процесс лежит в кинетической области и кинетика, соответственно, - химическая. В некоторых случаях лимитирующей стадией оказывается стадия образования новой фазы – зародышеобразование.
Типичным примером твердофазных реакций являются процессы термического разложения твердых тел (термолиз). Поскольку фононы имеют существенно меньшую энергию, чем фотоны, используемые в процессах фотолиза, термолиз оказывается более локализованным на дефектных местах кристалла, чем фотолиз, и тем более, чем радиолиз. В случае термолиза генерация электронно-дырочных пар не играет той роли, которую она играет при фотолизе. Более того, если в химическом соединении анион или катион является сложным, то возбуждение может сосредоточиться внутри соответствующей анионной либо катионной подрешетки:
2MnO4- → MnO42- + MnO4o (10.1)
|→ MnO2 + O2 .
В ряде случаев оказываются более выгодными не электронные переходы, а протонные:
NH4ClO4 → NH3 + HClO4. (10.2)
В целом, процессы термолиза преимущественно обусловлены локальными переходами электронов из валентной зоны на примесные уровни с последующим химическим актом. Таким образом, три элементарных стадии – возбуждение, миграция и локализация при термолизе объединены в один. Эти обстоятельства резко повышают роль дефектной подсистемы.
Как процессы термолиза, так и многие другие твердофазные реакции характеризуются рядом общих особенностей, и в первую очередь тем, что определяющее значение играет пространственное расположение реагирующих молекул, процессы массопереноса, состояние дефектной подсистемы, предыстория образца. В совокупности эти особенности позволили объединить такого рода процессы под общим названием «топохимические» процессы. Термин «топохимия» предполагает, что реакция контролируется структурой кристаллической решетки, может идти в каждой точке объема кристалла и при этом вступающие в реакцию молекулы испытывают минимальные атомные или молекулярные перемещения (по крайней мере на начальных этапах процесса).
На начальной стадии твердофазного взаимодействия важное значение имеет процесс образования зародышей новой фазы. Во многих случаях на этой стадии имеет место автокаталитический рост скорости, затем размер зародышей продолжает возрастать и они начинают соприкасаться, и, постепенно скорость процесса снижается. Типичная зависимость степени превращения и скорости превращения (dα/dt) от времени (рис. 10.1) характеризуется так называемой s-образной (или «сигмоидной») кривой, изображенной на рис. 10.1.
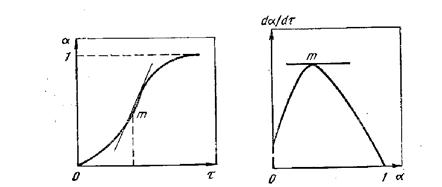
Рис. 10.1. Зависимости степени превращения от времени (а) и скорости превращения от степени превращения (б)
Для оценки скорости твердофазного взаимодействия обычно используется величину, называемую степенью превращения:
α = (xo-x) / xo, (10.3)
где хo - начальное количество вещества, x - количество вещества в момент времени τ.
Как упоминалось выше, важнейшей составляющей твердофазных процессов является процесс диффузии. В простейшем случае роль диффузии можно проиллюстрировать хорошо известными экспериментами, в которых исследовалось взаимодействие пластинок из серебра, меди и свинца со свободными галогенами в изотермических условиях. Было установлено, что скорость роста слоя галогенида металла описывается уравнением:
dx/dt = kx-1, (10.4)
где x – толщина слоя продукта, t - время, k - константа, зависящая от природы металла и галогена, а также от условий реакции, причем впоследствии было показано, что k = krD, где kr – константа, D - коэффициент диффузии. Объединяя это выражение с уравнением (10.4), интегрируя с учетом граничных условий x = 0 при t = 0, находим:
x2 = 2krDt = kpt, либо x = (kp)1/2t1/2, (10.5)
где kp - константа скорости параболического роста продуктов.
С учетом этой простейшей зависимости скорости процесса от времени в диффузионно-контролируемых условиях Яндером была предложена модель для описания кинетики реакций в порошкообразных системах. Принималось, что порошкообразный компонент A состоит из одинаковых по размеру сферических частиц с начальным радиусом Ro. Компонент B быстро образует непрерывный слой продукта C на поверхности частиц A по реакции
Aтв + Bтв = Cтв + Dг, (10.6)
причем реакция лимитирована объемной диффузией компонента B через слой продукта к компоненту A, а коэффициент диффузии не зависит от времени. Примером такой реакции может быть взаимодействие диоксида кремния с карбонатом бария:
SiO2 + BaCO3 = BaSiO3 + CO2. (10.7)
Исходя из геометрических аспектов данной задачи, для сферических частиц можно записать:
 . (10.8)
. (10.8)
 . (10.9)
. (10.9)
Объединяя выражения (10.9) и (10.5), получаем известное уравнение Яндера:
 , (10.10)
, (10.10)
иллюстрирующее временную зависимость степени превращения в ходе протекания твердофазной реакции, лимитированной диффузией.
Поиск по сайту: