 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Методы определения порядка химических реакций
Метод подстановки. Суть метода в том, что пробуют подставлять опытные данные в кинетические уравнения разных порядков и наблюдают, какое из них дает более постоянную величину константы скорости. Это наиболее простой метод, но и самый ненадежный.
Метод изоляции (избытка). Заключается в выделении частного порядка данной реакции по каждому веществу отдельно: общий порядок реакции находится суммированием частных порядков реакции.
Графический метод. Экспериментальные значения концентраций реагирующих веществ наносятся на график, отражающий изменение концентрации в зависимости от времени. При этом выбираются такие координатные оси, чтобы график представлял собой прямую линию. Если экспериментальные точки легли на прямую, то координатные оси выбраны удачно и соответствуют порядку реакции.
Метод периода полураспада. Период полураспада реакций различного порядка по-разному зависит от С0. На основании характера влияния С0 на  (см. уравнения 10.7, 10.12, 10.15 и 10.17) делается заключение о порядке реакции. Этот метод может быть реализован и в графическом варианте.
(см. уравнения 10.7, 10.12, 10.15 и 10.17) делается заключение о порядке реакции. Этот метод может быть реализован и в графическом варианте.
Метод Вант - Гоффа.
Пусть v = k 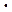 Cn, где n - порядок реакции. Тогда для двух различных концентраций
Cn, где n - порядок реакции. Тогда для двух различных концентраций
 и
и  .
.
Далее
 и
и  ,
,
поэтому
 .
.
Существует и графический вариант метода. После логарифмирования уравнения v =k 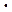 Cn:
Cn:
ln v = lnk + nlnC.
В координатах ln v - lnC получается прямая, тангенс угла наклона которой к оси абсцисс равен порядку реакции n.
Поиск по сайту: