 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Вычисление энтропии
В качестве отправной точки необходимо воспользоваться соотношением (4.21).
Тогда для изотермического процесса (Т = const):
 ,
,
где dq = dU + pdV, а dU = 0,
поэтому
 . (4.39)
. (4.39)
Из уравнения состояния идеального газа:
 , (4.40)
, (4.40)
если n = 1 моль, следовательно:
 . (4.41)
. (4.41)
После интегрирования:
 . (4.42)
. (4.42)
Для случая P = const:
 ,
,
где dqP = CPdT, поэтому
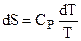
и после интегрирования:
 . (4.43)
. (4.43)
Если СР = const, то
 . (4.44)
. (4.44)
По аналогии для случая V = const:
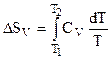 . (4.45)
. (4.45)
и если СV = const, то
 . (4.46)
. (4.46)
Если изотермическое превращение является фазовым - плавление, испарение, сублимация или полиморфный переход, то:
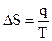 , (4.47)
, (4.47)
где q - энергетический эффект фазового перехода;
Т - температура фазового перехода.
Таким образом, рассмотрены некоторые уравнения, позволяющие вычислять изменение энтропии, если известны изменения параметров системы и ее теплоемкость. Существуют и другие методы определения изменения энтропии, например по измерениям электродвижущих сил гальванических элементов, о чем речь пойдет в главе “Электрохимия”.
Поиск по сайту: