 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Электропроводность растворов электролитов
Способность вещества проводить электричество называется электропровоностью или, наоборот, электросопротивлением:
 , (8.14)
, (8.14)
где  - электропроводность, Ом-1 или См (сименс);
- электропроводность, Ом-1 или См (сименс);
R - электросопротивление, Ом.
Электросопротивление проводника определяется его геометрией и природой:

|
 , (8.15)
, (8.15)
где l - длина проводника, м;
S - сечение проводника, м2;
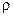 - удельное электросопротивление, Ом
- удельное электросопротивление, Ом 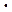 м.
м.
Удельная электропроводность.
В электрохимии вместо удельного электросопротивления принято пользоваться величиной удельной электропроводности, определяемой из выражения:
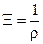 , (8.16)
, (8.16)
где  - удельная электропроводность, Ом-1
- удельная электропроводность, Ом-1 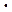 м-1.
м-1.
| Рис. 8.1. Схема концентрационной зависимости удельной электропроводности водных растворов. |
Удельная электропроводность - электропроводность электролита данной концентрации, помещенного между двумя электродами, находящимися на расстоянии 1 м друг от друга и с площадью пластин равной 1 м2.
Так как перенос электричества в растворе электролита осуществляется движением ионов, то удельная электропроводность тем выше, чем больше их концентрация в электролите и скорость их миграции.
Обычно зависимость удельной электропроводности водных растворов электролитов выражается кривой с максимумом (рис. 8.1). Ход кривой объясняется следующим образом: чистая вода - хороший диэлектрик; электрическая проводимость возникает при введении в воду первых порций электролита и увеличивается по мере добавления новых порций электролита; при достаточно большой концентрации проявляется взаимное влияние ионов и электропроводность уменьшается.
С ростом температуры электропроводность растворов электролитов увеличивается: при повышении температуры на 1 К  увеличивается на 2
увеличивается на 2 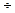 3 %.
3 %.
Эквивалентная электропроводность.
Изучение электрохимии упрощается, если сравнивать электропроводности растворов электролитов независимо от случайного выбора их концентраций. Для этого удельную электропроводность  относят к одной и той же концентрации С, выраженной в моль-экв/м3[4]:
относят к одной и той же концентрации С, выраженной в моль-экв/м3[4]:
 , (8.17)
, (8.17)
где  - эквивалентная электропроводность, Ом-1
- эквивалентная электропроводность, Ом-1 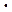 м2
м2 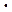 моль-экв-1;
моль-экв-1;
V - разбавление (разведение) электролита, м3/моль.
В размерности эквивалентной электропроводности последний сомножитель часто не указывается.

|
Эквивалентная электропроводность - электропроводность такого объема раствора данной концентрации, которое содержит 1 моль-экв растворенного вещества и которое помещается между электродами, находящимися на расстоянии 1 м.
Согласно (8.17) с увеличением концентрации электролита эквивалентная электропроводность уменьшается (рис. 8.2).
Из рис. 8.2 следует, что в зависимости от характера изменения  = f (С) растворы электролитов делятся на сильные и слабые электролиты: в растворах сильных электролитов
= f (С) растворы электролитов делятся на сильные и слабые электролиты: в растворах сильных электролитов  сохраняет высокие значения и при высоких концентрациях растворов.
сохраняет высокие значения и при высоких концентрациях растворов.
| Рис. 8.2. Схема концентрационной зависимости эквивалентной электропроводности водных растворов. |
В растворах слабых электролитов электропроводность падает очень быстро и даже в сильно разбавленных растворах она уже весьма мала. Такой характер кривой  = f (С) объясняется, главным образом, уменьшением степени электролитической диссоциации при повышении концентрации.
= f (С) объясняется, главным образом, уменьшением степени электролитической диссоциации при повышении концентрации.
Когда растворы обоих типов электролитов приближаются к бесконечно разбавленным, деление электролитов на слабые и сильные становится весьма условным.
Зависимость эквивалентной электропроводности разбавленных растворов слабых электролитов выражается уравнением закона разбавления Оствальда:
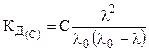 , (8.18)
, (8.18)
где  - эквивалентная электропроводность при бесконечном разбавлении раствора.
- эквивалентная электропроводность при бесконечном разбавлении раствора.
Закон разбавления Оствальда получен на основе закона действующих масс и выражения:
 .
.
Линеаризация закона разбавления приводит к выражению вида:
 . (8.18)
. (8.18)
Зависимость эквивалентной электропроводности разбавленных растворов сильных электролитов от концентрации хорошо передается широко оправдавшей себя формулой Кольрауша (1900 г.):
 , (8.19)
, (8.19)
где а - постоянная величина.
Поиск по сайту: