 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Эффект Джоуля-Томсона – положительный и интегральный
Положительный, если газ в процессе дросселирования охлаждается.
Интегр. эффект – эффект, при кот. давление измен. в широких пределах, сопровожд. значит. измен. темпер.
73. Понятие фазовых переходов. Фазовая диаграмма. Нормальные и аномальные вещества. Фазовые переходы 1-го рода. Уравнение Клайперона-Клаузиуса.
Фаз. переход – переход ве-ва из одной ТД фазы в другую при измен. внешних условий.
Фазовая диаграмма – графич. отображ. равновесного сост. бесконечной физико-химич. системы при условиях, отвечающих координатам рассм. точки на диаграмме.
Фаз. переходы 1-го рода сопровожд. поглощением теплоты фаз. перехода (кипение, плавление, возгонка) или выделением теплоты фаз. перехода (конденсация, кристаллизация, сублимация), при этом измен. молярные объёмы и энтропии ве-ва.
Ур. Клап.-Клаузиуса:
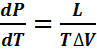 L- удельная теплота фазового перехода, △V – измен. удельного объёма тела при фаз. переходе
L- удельная теплота фазового перехода, △V – измен. удельного объёма тела при фаз. переходе
74. Фаза. Фазовый переход. Правило фаз Гиббса. Фазовый переход 2-го рода. Фазовая диаграмма гелия
Фаза -термодинамически равновесное состояние в-ва, отличающееся по физическим свойствам от других возможных равновесных состояний того же в-ва. Под фазой можно понимать агрегатное состояние. Фазовый переход - переход в-ва из одной фазы в другую, всегда связан с качественными изменениями св-в в-ва.
Правило фаз Гиббса: определяет число фаз, которые могут одновременно существовать в равновесии в ТД-системе. N<=K+2, где К- число компонентов смеси. Одновременно в равновесии м/б фаз: в чистом в-ве(К=1) N<=3; в бинарном(К=2)N<=4; в тройном(К=3) N<=5.если N<К+2, то f=K+2-N- число ТД-степеней свободы системы.
Фазовые переходы 2-ого рода: не требуют теплоты фаз перехода, не изменяют объём и энтропию; скачкообразное изменение теплоемкости; происходит незначительное перемещение атомов без большого затрачивания энергии. Пример: появление сверхпроводимости в металлах, превращение обыкновенного жидкого гелия в другую жидкую модификацию, обладающую св-вами сверхтекучести.
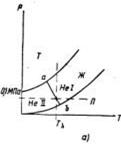
Фазовая диаграмма гелия: гелий после своего сжижения остаётся жидким при всех Т, вплоть до абсолютного 0. Кривые испарения и плавления не пересекаются, нет тройной точки. Кривая плавления пересекает ось давления при р= 2,5 МПа. Для отвердевания гелия необходимы понижение температур и повышение давления. Эти явления связаны с квантовыми процессами, движение атомов не прекращается при Т=0. Только при низких температурах гелий является квантовой жидкостью, которая не обязательно переходит в твердое состояние.
Поиск по сайту: