 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Занятие 4. Моль. Молярная масса
На занятии проводится тестовый контроль по теме «Основные понятия химии».
Вариант билета
1. В каком из случаев кислород выступает как химический элемент:
1) поддерживает дыхание и горение
2) является одним из составных компонентов воздуха
3) входит в состав воды и оксида углерода(IV)
4) взаимодействует со многими простыми и сложными веществами
2. Какая из записей обозначает наибольшее число молекул кислорода?
1) О2 2) О3 3) 2О2 4) 3О
3. Масса (в граммах) порции сульфата меди(II), в которой содержится 1,204×1023 атомов кислорода, равна:
1) 8 2) 32 3) 64 4) 128
4. Массовая доля брома наибольшая в соединении:
1) CH3Br 2) CH2Br2 3) CHBr3 4) CBr4
5. При разложении 21 г карбоната двухвалентного металла выделилось 5,6 л оксида углерода(IV) (н.у.). Этот металл:
1) ВаСО3 2) СаСО3 3) MgCO3 4) SrCO3
& Вопросы для самостоятельной подготовки
1. Моль – единица количества вещества.
2. Молярная масса, единицы измерения.
3. Число Авогадро.
 |

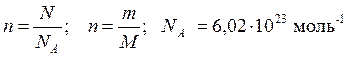
Упражнения и задачи для самостоятельного решения.
1. Вычислите молярные массы: гидроксида алюминия, сульфата железа(III).
2. В 7,20 г вещества содержится 5,42×1022 молекул. Чему равна молярная масса этого вещества? (Ответ: 80 г/моль)
3. Определите молярную массу неизвестного вещества, если масса одной его молекулы составляет 5,33×10-23 г. (Ответ: 32 г/моль)
4. Сколько моль и молекул составляют: 1 кг азотистой кислоты; 19,6 г фосфорной кислоты; 26,1 г оксида марганца(IV)?
(Ответ: 21,2 моль; 1,28×1025; 0,2 моль; 1,204×1023; 0,3 моль; 1,806×1023)
5. Какова масса: а) 18,06×1023 молекул оксида азота(IV); б) 1,204×1024 молекул озона? (Ответ: 138 г; 96 г)
6. Определите число атомов каждого элемента в воде массой 36 г.
(Ответ: 2,408×1024; 1,204×1024)
7. В каком количестве вещества хлороводорода содержится такое же количество атомов водорода, что и в серной кислоте массой 19,6 г?
(Ответ: 0,4 моль)
8. Сколько молекул воды содержится в стакане воды (200 мл)?
(Ответ: 6,7×1024)
 Дополнительные задания
Дополнительные задания
1. Определите абсолютную молекулярную массу гормона инсулина, если относительная молекулярная масса этого гормона равна 5734.
(Ответ: 9,52×10–21 г)
2. Рассчитайте молярную массу хлорофилла, если абсолютная молекулярная масса его составляет 1,485×10–18 мг. (Ответ: 894 г/моль)
3. В образце ортофосфорной кислоты содержится 1,5 г атомов водорода. Чему равно количество вещества ортофосфорной кислоты?
(Ответ: 0,5 моль)
4. Какое количество атомов водорода содержится в 25,5 г аммиака?
(Ответ: 4,5 моль)
5. В какой массе алюмокалиевых квасцов KАl(SO4)2×12H2O содержится: а) 2,7 г алюминия; б) 0,06 моль воды; в) 0,1 моль атомов кислорода? (Ответ: а) 47,4 г; б) 2,37 г; в) 2,37г)
6. Имеется 0,25 моль образца ортофосфата магния. Вычислите количество вещества в этом образце: а) атомов магния; б) атомов кислорода;
в) атомов фосфора; г) фосфат ионов; д) электронов.
(Ответ: 0,75; 0,5; 2,0; 0,5; 32,5 моль)
Поиск по сайту: