 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Задача № 1. При взаимодействии 10 г оксида натрия с водой выделяется 36,46 кДж теплоты
При взаимодействии 10 г оксида натрия с водой выделяется 36,46 кДж теплоты. Какое количество теплоты (кДж) выделилось, если в результате реакции образовалось 200 г гидроксида натрия?
Решение:
1. Запишем термохимическое уравнение реакции:
Na2O + H2O = 2NaOH + Q
2. Определяем количество оксида натрия:
 ;
;  моль.
моль.
3. Определяем количество гидроксида натрия, образовавшегося при растворении 10 г Na2O: n (Na2O): n (NaOН) = 1: 2 (по уравнению),
следовательно, n (NaOН) = 2 n (Na2O); n (NaOН) = 2×0,16 = 0,32 моль.
4. Определяем количество гидроксида натрия, соответствующего 200 г NaOH: 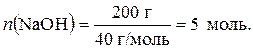
5. Определяем количество теплоты, выделившейся при образовании
5 моль NaOH:
при образовании 0,32 моль NaOH выделится 36,46 кДж,
а при образовании 5 моль NaOH выделится х кДж, что составляет:
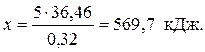
Ответ: 569,7 кДж
Поиск по сайту: