 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Задача № 1. Для гидролизующихся веществ написать уравнения реакций гидролиза:
Для гидролизующихся веществ написать уравнения реакций гидролиза:
CuCl2, Na2CO3, CrS, Cr2S3, NaCl, тристеарид, глицилглицин, этилэтаноат.
Решение:
а) CuCl2 – соль, растворимая в воде, образована катионом слабого основания и анионом сильной кислоты, подвергается гидролизу. Гидролиз протекает по катиону слабого основания:
CuCl2 = Cu2+ + 2Cl–
Cu2+ + HOH (CuOH)+ + H+ I ступень, pH<7
CuCl2 + HOH (CuOH)Cl + HCl
CuOHCl ® (CuOH)+ + Cl 
(CuOH)+ + HOH Cu(OH)2 + H+ II ступень
CuOHCl + HOH Cu(OH)2 + HCl
При обычных условиях гидролиз протекает только по I ступени.
б) Na2CO3 – соль, растворимая в воде, образована катионом сильного основания и анионом слабой кислоты, подвергается гидролизу.
Гидролиз протекает по аниону слабой кислоты:
Na2CO3 = 2Na+ + CO 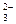
CO 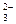 + HOH HCO
+ HOH HCO 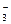 + OH
+ OH  I ступень, pH>7
I ступень, pH>7
Na2CO3 + HOH NaHCO3 + NaOH
NaHCO3 = Na+ + HCO 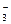
HCO 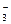 + HOH H2CO3 + OH
+ HOH H2CO3 + OH  II ступень
II ступень
NaHCO3 + HOH H2CO3 + NaOH
в) CrS – труднорастворимая соль, не гидролизуется из-за низкой концентрации ионов в водном растворе.
г) Cr2S3 – соль, образована слабым нерастворимым в воде основанием и слабой, летучей кислотой. В водном растворе соль не существует, так как подвергается полному гидролизу: Cr2S3 + 6HOH 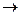 2Cr(OH)3
2Cr(OH)3 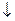 + 3H2S
+ 3H2S 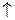 .
.
д) NaCl – соль растворима в воде, образована катионом сильного основания и анионом сильной кислоты. Гидролизу не подвергается.
Поиск по сайту: