 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Закон постоянства состава. Химические формулы
& Вопросы для самостоятельной подготовки
1. Что называют химическим явлением или реакцией? Чем химическое явление отличается от физического? Приведите примеры
2. Химическое соединение и смесь с точки зрения атомно-молекулярного учения. Укажите признаки, по которым смеси отличаются от химических соединений.
3. Что называют химической формулой? Виды химических формул: эмпирические, молекулярные, графические. Какую информацию несет химическая формула?
4. Как рассчитать массовую долю элемента в соединении?
5. Закон постоянства состава.
 |



Типовые задачи с решениями
Задача № 1
Вычислите массовые доли углерода, водорода и кислорода в уксусной кислоте.
Решение:
1. Определяем молярную массу уксусной кислоты:
М (СН3СООН) = 60 г/моль;
2. По формуле 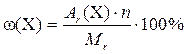 рассчитываем массовую долю элементов в соединении:
рассчитываем массовую долю элементов в соединении:
w(С) =  40,0%; w(Н) =
40,0%; w(Н) =  = 6,67%;
= 6,67%;
w(О) = 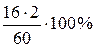 = 53,33%.
= 53,33%.
Ответ: 40,0%; 6,67%; 53,33%.
Задача № 2
Массовая доля кислорода в оксиде трехвалентного металла составляет 47,06%. Определите металл.
Решение:
1. Запишем формулу оксида в виде Ме2О3 и определим его молярную массу, пользуясь формулой:  ;
;
Мr =  ; М (Ме2О3) =
; М (Ме2О3) =  = 102 г/моль.
= 102 г/моль.
2. Рассчитаем молярную массу металла:
М (Ме) = 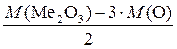 ; М (Ме) =
; М (Ме) =  г/моль.
г/моль.
Следовательно, металл – алюминий.
Ответ: Al.
Упражнения и задачи для самостоятельного решения.
1. К каким явлениям – физическим или химическим – относятся: а) кипение воды; б) хлорирование металла; в) таяние ледников; г) пожелтение травы; д) ржавление гвоздя; е) испарение воды; ж) образование озона в атмосфере во время грозы; з) перегонка нефти; и) скисание молока;
к) плавление соли; л) окисление металла?
2. Какие из перечисленных веществ являются химическими соединениями и какие смесями: а) воздух; б) мел; в) мрамор; г) водяной пар;
д) морская вода; е) почва?
3. Что означают формулы: Н2SO4, КОН, Al2(SO4)3, NaCl?
4. Дать названия и составить графические формулы следующих веществ: Fe2O3; Mg3P2; Li3N; Cl2O7; Ca(OH)2; H2SO4; K2SO4; Cr2O3; SiO2.
5. Рассчитать массовую долю металла в следующих соединениях: FeO, Fe2O3, Fe3O4.
6. Массовая доля кислорода в оксиде трехвалентного элемента составляет 0,173. Вычислить относительную атомную массу элемента.
(Ответ: 114,7)
7. При сгорании трехвалентного металла массой 11,2 г образовался оксид массой 16 г. Какой был взят металл? (Ответ: железо)
 Дополнительные задания
Дополнительные задания
1. Абсолютная молекулярная масса серы равна 4,25×10-22 г. Из какого числа атомов состоит молекула серы? (Ответ: 8 атомов)
2. Общее число атомов в образце оксида металла II-А группы, в котором массовая доля кислорода больше массовой доли металла, равна 3,01×1021. Вычислите массу образца оксида. (Ответ: 0,0625 г ВеО)
3. Массовая доля кислорода в кристаллогидрате сульфата железа(II) равна 0,633. Установите формулу кристаллогидрата.
(Ответ: FeSO4×7H2O)
Поиск по сайту: