 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Основные формулы для решения задач
| Величина и ее размерность | Соотношение |
| Атомная масса элемента Х (относительная) |  
|
| Порядковый номер элемента | Z = N (е –)= N (р +) |
| Массовая доля элемента Э в веществе Х, в долях единицы, в %) |  
|
| Количество вещества Х, моль | 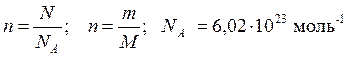
|
| Количество вещества газа, моль |  Vm = 22,4 л/моль (н.у.)
н.у. – р = 101 325 Па, Т = 273 К Vm = 22,4 л/моль (н.у.)
н.у. – р = 101 325 Па, Т = 273 К
|
| Молярная масса вещества Х, г/моль, кг/моль | 
|
| Масса вещества X, г, кг | m (X) = n (X)× M (X) |
| Молярный объем газа, л/моль, м3/моль | Vm = 22,4 л/моль при н.у. |
| Объем газа, м3 | V = Vm × n |
| Выход продукта |   
|
| Плотность вещества Х, г/л, г/мл, кг/м3 | 
|
| Плотность газообразного вещества Х по водороду | 
|
| Плотность газообразного вещества Х по воздуху |  М (воздуха) = 29 г/моль
М (воздуха) = 29 г/моль
|
| Объединенный газовый закон | 
|
| Уравнение Менделеева-Клапейрона | PV = nRT, R = 8,314 Дж/моль×К |
| Объемная доля газообразного вещества в смеси газов, в долях единицы или в % | 
|
| Молярная масса смеси газов | 
|
| Молярная доля вещества (Х) в смеси | 
|
| Количество теплоты, Дж, кДж | Q = n (X)× Q (X) |
| Тепловой эффект реакции | Q =– D H |
| Теплота образования вещества Х, Дж/моль, кДж/моль | 
|
| Скорость химической реакции (моль/л×сек) | 

|
| Закон действия масс (для простой реакции) | a A + в B = с С + d D u = k×с a (A)× с в (B) |
| Правило Вант-Гоффа | 
|
| Растворимость вещества (Х) (г/100 г растворителя) | 
|
| Массовая доля вещества Х в смеси А + Х, в долях единицы, в % | 
|
| Масса раствора, г, кг | m (р-р) = m (X) + m (H2O) m (р-р) = V (р-р)× r (р-р) |
| Массовая доля растворенного вещества в растворе, в долях единицы, в % | 
|
| Плотность раствора | 
|
| Объем раствора, см3, л, м3 | 
|
| Молярная концентрация, моль/л | 
|
| Степень диссоциации электролита (Х), в долях единицы или % | 
|
| Ионное произведение воды | K (H2O) = [H+][OH–] |
| Водородный показатель | рН = –lg[H+] |
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
Основная:
Кузнецова Н.Е. и др. Химия. 8 кл-10 кл.. – М.: Вентана-Граф, 2005-2007.
Кузнецова Н.Е., Литвинова Т.Н., Левкин А.Н. Химия.11 класс в 2-х частях, 2005-2007 гг.
Егоров А.С. Химия. Новое учебное пособие для подготовки в вузы. Ростов н/Д: Феникс, 2004.– 640 с.
Егоров А.С. Химия: современный курс для подготовки к ЕГЭ. Ростов н/Д: Феникс, 2011. (2012)– 699 с.
Егоров А.С. Самоучитель по решению химических задач. – Ростов-на-Дону: Феникс, 2000.– 352 с.
Химия/пособие-репетитор для поступающих в вузы. Ростов-н/Д, Феникс, 2005– 536 с.
Хомченко Г.П.,Хомченко И.Г. Задачи по химии для поступающих в вузы. М.: Высшая школа. 2007.–302с.
Дополнительная:
Врублевский А.И. Учебно-тренировочные материалы для подготовки к централизованному тестированию по химии/ А.И. Врублевский –Мн.: ООО «Юнипресс», 2004.– 368 с.
Врублевский А.И. 1000 задач по химии с цепочками превращений и контрольными тестами для школьников и абитуриентов.– Мн.: ООО «Юнипресс», 2003.– 400 с.
Егоров А.С. Все типы расчетных задач по химии для подготовки к ЕГЭ.–Ростов н/Д: Феникс, 2003.–320с.
Егоров А.С., Аминова Г.Х. Типовые задания и упражнения для подготовки к экзамену по химии. – Ростов н/Д: Феникс, 2005.– 448 с.
Единый государственный экзамен 2007. Химия. Учебно-тренировочные материалы для подготовки учащихся/ФИПИ – М.: Интеллект-Центр, 2007.– 272 с.
ЕГЭ-2011. Химия. Учебно-тренировочный комплект под ред. А.А. Кавериной.– М.: Национальное образование, 2011.
Единственные реальные варианты заданий для подготовки к единому государственному экзамену. ЕГЭ.2007. Химия/В.Ю. Мишина, Е.Н. Стрельникова. М.: Федеральный центр тестирования, 2007.–151с.
Каверина А.А. Оптимальный банк заданий для подготовки учащихся. Единый государственный экзамен 2012.Химия. Учебное пособие./ А.А. Каверина, Д.Ю. Добротин, Ю.Н. Медведев, М.Г. Снастина.– М.: Интеллект-Центр, 2012.– 256 с.
Литвинова Т.Н., Выскубова Н.К., Ажипа Л.Т., Соловьева М.В. Тестовые задания в дополнение к контрольным работам для слушателей 10-месячных заочных подготовительных курсов (методические указания). Краснодар, 2004. – С. 18 – 70.
Литвинова Т.Н. Химия. ЕГЭ-2011. Тренировочные тесты. Ростов н/Д: Феникс, 2011.– 349 с.
Литвинова Т.Н. Химия. Тесты к ЕГЭ. Ростов н/Д.: Феникс, 2012. - 284 с.
Литвинова Т.Н. Химия. Законы, свойства элементов и их соединений. Ростов н/Д.: Феникс, 2012. - 156 с.
Литвинова Т.Н., Мельникова Е.Д., Соловьева М.В., Ажипа Л.Т., Выскубова Н.К. Химия в задачах для поступающих в вузы.– М.: ООО «Изд-во Оникс»: ООО «Изд-во «Мир и образование», 2009.– 832 с.
Учебно-методический комплекс по химии для учащихся медико-биологических классов под ред. Т.Н.Литвиновой.– Краснодар.: КГМУ, – 2008.
Химия. ЕГЭ–2008. Вступительные испытания, учебно-методическое пособие / под ред. В.Н. Доронькина. – Ростов н/Д: Легион, 2008.– 271 с
Список сайтов по химии:
1. Alhimik. http://www.alhimik.ru
2. Химия для всех. Электронный справочник за полный курс химии.
http://www.informika.ru/text/database/chemy/START.html
3. Школьная химия – справочник. http://www.schoolchemistry.by.ru
4. Репетитор по химии. http://www. chemistry.nm.ru
Поиск по сайту: