 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Тест тапсырмалары 7 страница
| Энергетикалық деңгейлер | 
| 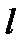
| ò |
| Ê | 0 s | ||
| L | 0 s 1 p | +1, 0, -1 | |
| M | 0 s 1 p 2 d | +1, 0, -1 +2, +1, 0, -1, -2 | |
| N | 0 s 1 p 2 d 3 f | +1, 0, -1 +2, +1, 0, -1, -2 +3, +2, +1, 0, -1, -2, -3 |
Àòîìнûң ýëåêòðîí қàóûçдарûí òîëòûðó åðåæåëåði. Ïàóëè ïðèíöèïi. Êëå÷êîâñêèé, Ãóíä åðåæåëåði.
Ýëåêòðîíäàðäûң äåңãåéëåðäå îðíàëàñóû îëàðäûң ýíåðãèÿñûíà áàéëàíûñòû. Ýëåêòðîí ÿäðîғà æàқñû òàðòûëûï, ýíåðãèÿñû íåғұðëûì аз äåңãåéäå îðíàëàñóғà òûðûñàäû. Ýëåêòðîíäàðäûң äåңãåéëåðäå îðíàëàñó ðåòi îñû åðåæåëåðãå áàғûíàäû:
Ïàóëè ïðèíöèï i: àòîìäà òөðò êâàíò ñàíäàðûíûң ìәíäåði áiðäåé áîëàòûí åêi ýëåêòðîí áîëìàéäû.
Гóíä åðåæåñi: ýëåêòðîíäàð àòîìäàðäà ñïèí ñàíäàðûның қîñûíäûñû ìàêñèìàë áîëàòûíäàé îðíàëàñàäû
Êëå÷êîâñêèé åðåæåñi: ýëåìåíòòåðäiң ðåòòiê íөìiði àðòқàí ñàéûí àòîìäàðäûң ýëåêòðîíäûқ äåңãåéëåði n+l қîñûíäûñû ìәíiнің өñói áîéûíøà ýëåêòðîíғà òîëàäû, åãåð n+l қîñûíäûñû òåң áîëñà, онда ýëåêòðîí l-ң ìәíi æîғàðû болатын îðáèòàëғà îðíàëàñàäû.
Ìûñàëы: 1) Êàëèé ýëåìåíòiíiң ñîңғû îí òîғûçûíøû ýëåêòðîíû үøií 3d æәíå 4ð îðáèòàëäàðû áîñ. Åãåð ýëåêòðîí 3d-îðáèòàëғà áàðàäû äåñåê, îë үøií n+l – äiң ìәíi 3+2 = 5, àë 4s îðáèòàëi үøií n+l = 4+0 = 4 áîëàäû. Äåìåê, êàëèéäiң ñîңғû ýëåêòðîíû 4s îðáèòàëiíå îðíàëàñàäû: 1s22s22ð63s23ð64s1.
2) Åíäi îñû åðåæåíi ïàéäàëàíûï ñêàíäèé ýëåìåíòiíiң ñîңғû ýëåêòðîíû 3d íåмесе 4ð îðáèòàëäàðûíûң қàéñûñûíà îðíàëàñàòûíûí åñåïòåï êөðåëiê. Ñêàíäèé үøií 3d = n+l = 3+2 = 5, àë 4ð = n+l = 4+1= 5 áîëàäû åêåí. Äåìåê, áұë æàғäàéäà, ÿғíè n+l – äiң қîñûíäûñû òåң áîëғàíäà, l – äiң ìәíi æîғàðû îðáèòàëғà ýëåêòðîíның îðíàëàñóы òèiс: l – äiң ìәíi жоғары болады 3d (l =2) орбиталда. Ñîíûìåí, ñêàíäèé ýëåìåíòiíiң ýëåêòðîíäûқ êîíôèãóðàöèÿñû ìûíàäàé áîëàäû: 1s22s22ð63s23ð63d14s2.
Îñû ìûñàëäàðғà қàðàé àòîìäàғû ýëåêòðîíäàðäûң äåңãåéëåð ìåí äåңãåéøåëåðäå ìûíàäàé ðåòïåí îðíàëàñàòûíûí êөðóãå áîëàäû:
 <
<  <
<  <
<  <
<  <
<  <
<  <
<  <
<  <
< 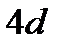 <
<  <
<  <
< 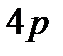 <
<  <
<  <
<  <
<  <
< 
4. Бақылау сұрақтары:
1. Атомқұрылысының мәні қандай?
2. Кванттық сандардың мәні қандай?
3. Калий, күкірт, қалайының электрондық және электронды-графикалық формуласын құрастырыңыз.
3. Изотоптар дегеніміз не?
4. Неліктен 3d-топшасы 4s-топшасынан кей3н толтырылады?
5. Тест тапсырмалары:
1. Атом ядросы қандай бөлшектерден тұрады?
1. тек протоннан
2) протон және электроннан
3) электрон және нейтроннан
4) нуклон және протоннан
5) протон және нейтроннан
2. Протонның заряды:
1) +2
2) -1
3) 0
4) заряды жоқ
5) +1
3. Атомдағы нейтрондар санын қалай анықтайды?
1) атомның массалық санынан протондар санын алады
2) атомның массалық санына протондар санын қосады
3) протондар санына нуклон санын қосады
4) массалық санға нуклон санын қосады
5) массалық санннан нуклон санын алады
4. Күкірт атомындағы нейтрондар саны нешеге тең?
1) 32
2) 15
3) 16
4) 8
5) 64
5. 8 нейтроны бар азот атомының массалық санын анықтаңыз:
1) 17
2) 14
3) 13
4) 3
5) 15.
6. Күкірт атомының ядро заряды нешеге тең?
1) + 6
2) + 8
3) + 32
4) + 16
5) + 10
7. Бір изотопының массалық саны 31-ге тең, ал нейтрон саны 16 болатын элементтің реттік номерін көрсетіңіз:
1) 47
2) 15
3) 33
4) 39
5) 8
8. 4-ші периодта 5-ші қосымша топшада орналасқан элемент атомының құрамында неше электрон және неше протон бар?
1) 28
2) 51
3) 23
4) 30
5) 74
9. Массалық саны 31-ге тең, ал нейтрон саны 16 болатын элементтің реттік номері қандай?
1) 15
2) 47
3) 21
4) 32
5) 8
10. Кеңістіктегі электрон бұлтының бағытын қай квант саны сипаттайды?
1) орбиталь квант саны (l))
2) магнит квант саны (m)
3) спин квант саны (s)
4) бас квант саны (n)
5) магнит және бас квант сандары (m және n)
11.Энергетикалық деңгейдегі орбитальдардың жалпы саны қандай формуламен анықталады?
1) Ν = n2 + 2
2) Ν = 2n2
3) Ν = 3n2
4) Ν = n3
5) Ν = n2
12. Энергетикалық деңгейдегі максималды электрондар санын қандай формуламен анықтауға болады?
1) Ν = 3n2
2) Ν = n2
3) Ν = n3
4) Ν = n2 + 1
5) Ν = 2n2
13. Үшінші периодтағы қай элемент атомының сыртқы энергетикалық деңгейінде 3 электрон (е-) бар?
1) Р
2) В
3) Аl
4) Аs
5) Ν
14. Төртінші энергетикалық деңгейге максималды қанша электронды орналастыруға болады?
1) 32
2) 16
3) 8
4) 18
5) 36
15. Реттік номері 35 болатын элементтің атомында қанша энергетикалық деңгей бар?
1) 7
2) 4
3) 6
4) 5
5) 3
16. Егер р – орбитальда 4 электрон болса, онда қанша электронның дара болғандығы?
1) 0
2) 3
3) 1
4) 4
5) 2
17. Берілген конфигурациялар бойынша электрондарға толған деңгейшелер санын көрсетіңіз: а) 4s1 ә) 2s2 б) 2р5 в) 4d2 г) 3р6 д) 5f14 е) 3d8 ж) 5р6
1) 5
2) 4
3) 2
4) 3
5) 6
18. Екінші энергетикалық деңгейдегі р – орбитальда 3 дара электрон бар. Бұл қай элемент атомының электрондық формуласы?
1) фосфор
2) азот
3) көміртек
4) оттек
5) бор
19. Электрондық формулалары төменде келтірілген элементтерді атаңыз:
а) 1s2 2s1ә) 1s2 2s2 2р5 б ) 1s2 2s2 2р6 3s1 в) 3s2 3р5 г ) 3s2 3р6 4s2 3d2
1) литий, фтор, натрий, хлор титан
2) литий, азот, натрий, фосфор, мырыш
3) фтор, хлор, иод, титан, бор
4) литий, натрий, фосфор, мырыш, титан
5) хлор, бром, литий, бор, титан
20. Y-ден (иттрийден) Сd-ге (кадмийге) дейінгі элементтердің атомдарында қай орбитальда электрондар саны артады?
1) р
2) s
3) d
4) f
5) d және f
21. Атом құрылысының үлгісі мен графикалық формулалары берілген элементтерді атаңыз:
| +3 |
1S2
2 1
| +9 |
2S2
2 7 1S2
1) фтор, литий
2) литий, азот
3) литий, хлор
4) фосфор, литий
5) литий, фтор
22. Натрий катионындағы электрондар саны қанша?
1) 9
2) 11
3) 12
4) 10
5) 8
23. 3рдеңгейшеде 3 электроны бар элементті атаңыз:
1) алюминий
2) фосфор
3) кальций
4) бор
5) күміс
24. Екінші энергетикалық деңгейдегі р – орбитальда 3 дара электрон бар. Бұл қай элемент атомына сәйкес келеді?
1) оттек
2) азот
3) көміртек
4) кремний
5) фтор
25. Сыртқы қабаттың электрондық конфигурациясы...4s24p5 болатын элементті атаңыз?
1) ванадий
2) хлор
3) фтор
4) мышьяк
5) бром
26. Орбиталь квант (l) санының мәні 1-ге тең болғанда магнит квант (m) санының мәні қандай болады?
1) -1, 0, +1
2) 0, +1, +2
3) +1, +2
4) 0, 1, 2
5) -2, -1, 0, +1, +2
27. Бас квант саны 3-ке (n = 3), ал орбиталь квант саны 0-ге (l = 0) тең болғанда деңгейшені қалай белгілейді?
1) 3d
2) 3р
3) 3s
4) 3f
5) 3q
28. Орбиталь квант саны 1- ге (l = 1) тең болатын электрондар қалай аталады?
1) f – электрондар
2) s– электрондар
3) d – электрондар
4) р – электрондар
5) q – электрондар
29. S – электрондардың орбиталь квант сандарының мәні қандай болады?
1) 0
2) 1
3) 2
4) 3
5) -1
30. Орбиталь квант саны 2- ге (l = 2) тең болатын электрондарды қалай атайды?
1) s – электрондар
2) р – электрондар
3) d – электрондар
4) f – электрондар
5) q – электрондар
№ 4 дәріс. Химиялық элементтердің (Д.И.Менделеевтің) периодтық жүйесі
1. Дәрістің мақсаты:
Химиялық элементтердің периодтық жүйесін қарастыру және периодтық жүйені пайдалана отырып әрбір элементке сипаттама беруді студентке үйрету. Д. И. Менделеевтіѕ периодтыќ заѕының маңызын көрсету.
2. Дәрістің жоспары:
1.Ýëåìåíòòåðäiң ïåðèîäòûқ æүéåñi æәíå àòîì құðûëûñû. Àòîìäàғû ýëåêòðîíäàð êүéi. Үëêåí æәíå êiøi ïåðèîäòàð. Òîïòàð æәíå òîïøàëàð.
2. Ýëåêòðîí қàóûçû құðûëûñûíûң ïåðèîäòûëûғû. Ïåðèîäòûқ æүéåäå òîï æәíå òîïøàëàð áîéûíøà ýëåìåíòòåðäiң ìàңûçäû қàñèåòòåðiíiң өçãåðói.
3. Элементтердің электртерістілігі
4.Õèìèÿëûқ ýëåìåíòòåðäiң ïåðèîäòûқ æүéåäåãi îðíû және àòîì құðûëûñû òұðғûñûíàí ýëåìåíòòiң æәíå îíûң қîñûëûñòàðûíûң ñèïàòòàìàñû.
5. Ä. È. Ìåíäåëååâòiң ïåðèîäòûқ çàңûíûң ìàңûçû
3. Дәрістің мазмұны:
Ýëåìåíòòåðäiң ïåðèîäòûқ æүéåñi æәíå àòîì құðûëûñû. Àòîìäàғû ýëåêòðîíäàð êүéi. Үëêåí æәíå êiøi ïåðèîäòàð. Òîïòàð æәíå òîïøàëàð.
ÕIÕ Ғàñûðäûң åêiíøi æàðòûñûíäà àëïûñòàí аса õèìèÿëûқ ýëåìåíòòåð àøûëûï, îëàðäûң қàñèåòòåði æәíå îë ýëåìåíòòåðäiң қîñûëûñòàðûíûң қàñèåòòåði çåðòòåëäi. Îñûíäàé òîëûï æàòқàí ìàòåðèàëäàðäû áið æүéåãå êåëòiðó қàæåò áîëäû. Êөïòåãåí ғàëûìäàð ýëåìåíòòåðäi æүéåãå êåëòiðóãå òûðûñòû. Ìûñàëû, íåìiñ ғаëûìû È. Äåáåðåéíåð қàñèåòòåði ұқñàñ үø ýëåìåíòòiң àòîìäûқ ìàññàëàðûíûң îðòàøà àðèôìåòèêàëûқ ìөëøåðiíå òåң åêåíií àéòòû. Àғûëøûí ғàëûìû Ä. Íüþëåíäñ ýëåìåíòòåðäi àòîìäûқ ìàññàëàðûíûң өñó ðåòiìåí îðíàëàñòûðғàíäà æåòi ýëåìåíòòåí ñîң ñåãiçiíøiäåí áàñòàï õèìèÿëûқ қàñèåòòåði қàéòà қàéòàëàíàòûíûí áàéқàï, îíû îêòàâà çàңû äåï àòàäû. Íåìiñ ғàëûìû Ë.Ìåéåð ýëåìåíòòåðäi àòîìäûқ ìàññàëàðûíûң өñó ðåòiìåí îðíàëàñòûðûï ұқñàñ ýëåìåíòòåðäiң àëòû òîáûí æàñàäû. Áiðàқ àòàëғàí ғàëûìäàð ýëåìåíòòåðäiң ұқñàñ òîïòàðûí áið-áiðiíåí æåêå қàðàï, îëàðäûң àðàñûíäàғû iøêi áàéëàíûñòû àøà àëìàäû. Ñîíäûқòàí îëàð ұқñàñ æәíå ұқñàñ åìåñ ýëåìåíòòåðäiң òîïòàðûí ñèïàòòàéòûí òåîðèÿëûқ øîëó æàñàé àëìàäû.
Ýëåìåíòòåðäi æүéåãå êåëòiðó ìәñåëåñií îðûñòûң ұëû ғàëûìû Ä.È.Ìåíäåëååâ (1834-1907æ.) øåøòi. Îë 1869 æûëû ïåðèîäòûқ çàңäû àøûï, 1871 æûëû àíûқòàìàñûí áåðäi æәíå ñîë çàңíûң íåãiçiíäå ýëåìåíòòåðäiң ïåðèîäûқ æүéåñií æàñàäû. Ýëåìåíòòåðäi æүéåãå êåëòiðóäiң íåãiçi åòiï îëàðäûң àòîìäûқ ìàññàëàðûí àëäû.
Поиск по сайту: