 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Тест тапсырмалары 31 страница
Ýëåêòðîëèç êåçiíäå ýëåêòð ýíåðãèÿñû õèìèÿëûқ ðåàêöèÿ ýíåðãèÿñûíà, àòàï àéòқàíäà òîòûғó æәíå òîòûқñûçäàíó ðåàêöèÿëàðûíûң ýíåðãèÿñûíà àéíàëàäû.
4. Бақылау сұрақтары:
1.Тотығу дәрежесі қалай анықталады?
2.Тотығу-тотықсыздану реакцияларының қандай түрлерін білесіздер?
3.Негізгі тотықтырғыштар мен тотықсыздандырғыштарды атаңыздар.
5. Тест тапсырмалары:
1. Қандай реакция тотығу-тотықсыздану реакциясына жатады?
1) элемент атомдарының тотығу дәрежесі өзгермей жүретін реакция
2) элемент атомдарының тотығу дәрежесі өзгеріп жүретін реакция
3) реакцияға қатысқан заттар құрам бөліктерімен алмаса жүретін реакция
4) бір мезгілде екі бағытта жүретін реакция
5) ерітіндінің сутектік көрсеткішінің мәні өзгеріп жүретін реакция
2. Жәй заттардың тотығу дәрежесі нешеге тең болады?
1) < 1
2) +1
3) -1
4) > 1
5) 0
3. Молекула құрамына кіретін барлық атомдардың тотығу дәрежелерінің қосындысы қандай мәнге ие болады?
1) +1
2) 0
3) -1
4) > 1
5) < 1
4. Тотықсыздану процесі дегеніміз:
1) катионның электронды беруі
2) атом немесе ионның электронды беруі
3) атом немесе ионның электронды қосып алуы
4) анионның электронды беруі
5) атомның электронды беруі
5. Калий перманганатындағы марганецтің тотығу дәрежесі нешеге тең болады?
1) + 7
2) + 2
3) + 1
4) + 6
5) + 5
6. КСr(SO4)2 қосылысындағы хромның тотығу дәрежесін анықтаңыз:
1) + 2
2) + 6
3) + 4
4) + 5
5) + 3
7. Күкірт тотығу S-2 → S+6 барысында неше электрон береді?
1) 4
2) 6
3) 5
4) 8
5) 2
8. Күкірттің қандай қосылысы әрі тотықтырғыш, әрі тотықсыздандырғыш қасиет көрсетеді?
1) Н2SО4
2) Н2SО3
3) Н2S
4) SО3
5) К2SО4
9. Көміртек тотығу С-4 → С+4 кезінде қанша электронын береді?
1) 5
2) 0
3) 8
4) 6
5) 2
10. Азоттың қай қосылысы тек тотықтырғыш қасиет көрсетеді?
1) НNО2
2) НNО3
3) N2
4) NО2
5) NH3
11. Азоттың қай қосылысы тек тотықсыздандырғыш қасиет көрсетеді?
1) НNО2
2) НNО3
3) NH3
4) N2
5) NО2
12. Қай реакция тотығу-тотықсыздану реакциясына жатады?
1) KNО2 + КМnO4 →
2) NaCl + AgNO3 →
3) KOH + H2SO4 →
4) Na2CO3 + HCl →
5) Ba(NO3)2 + K2SO4 →
13. Cu + HNO3 → Cu(NO3)2 + NO2 + H2O тотығу-тотықсыздану реакциясындағы барлық коэффициенттердің қосындысы нешеге тең болады?
1) 7
2) 8
3) 5
4) 6
5) 10
14. Cu + HNO3 → Cu(NO3)2 + NO2 + H2O тотығу-тотықсыздану реакциясында тотықтырғыштың неше молі тотықсызданады?
1) 8
2) 3
3) 5
4) 4
5) 6
15. NН4NО3 қосылысындағы азот атомдарының тотығу дәрежелерін анықтаңыз:
1) -4, +5
2) -3, +4
3) +3, +5
4) +3, +3
5) -3, +5
16. Тотығу үрдісін көрсетіңіз:
1) N+5 → N+4
2) S-2 → S+6
3) Zn+2 → Zn0
4) 2Н+1 → Н20
5) S+4 → S-2
17. Тотықсыздану үрдісін көрсетіңіз:
1) S-2 → S+6
2) S+4 → S-2
3) N-3 → N+5
4) Zn0 → Zn+2
5) N+2 → N+4
18. Диспропорционирлену тотығу-тотықсыздану реакциясын көрсетіңіз:
1) 4KClO3 → 3KClO4 + KCl
2) Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
3) Zn + H2SO4 → ZnSO4 + H2
4) 4NН3 + 5О2 → 4NO + 6H2О
5) SO2 + 2H2S → 3S + 2H2О
19. Қай реакция молекулааралық тотығу-тотықсыздану реакциясына жатады?
1) Cl2 + H2O → НClО + HCl
2) 4KClO3 → 3KClO4 + KCl
3) Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
4) 2Co(NO3)2 → 2CoO + 4NO2 + O2
5) 2СаSO4 → 2СаО + 2SO2 + O2
20. Берілген реакцияда 2FeCl3 + H2S→ 2FeCl2 + S+ 2HCl қай элементтің атомы тотығады?
1) темір мен күкірттің
2) сутектің
3) темірдің
4) хлордың
5) күкірттің
21. Калий перманганаты қышқыл ортада тотықсызданғанда түзілетін қосылыс құрамындағы марганецтің тотығу дәрежесі қандай болады?
1) + 7
2) + 2
3) + 1
4) - 2
5) + 4
22. Қай қосылыс тек қана тотықтырғыш бола алады:
1) Н2SО4
2) NН3
3) Fe
4) FeSO4
5) КNО2
23. Қай қосылыс тек қана тотықсыздандырғыш бола алады:
1) KMnO4
2) NН3
3) K2Cr2O7
4) F2
5) НNО3
24. Берілген иондардағы MnO4- , MnO4 2- марганецтің тотығу дәрежесін анықтаңыз:
1) + 1, + 2
2) + 4, + 8
3) + 3, + 2
4) + 5, + 6
5) + 7, + 6
25. Бұл MnO4- → MnO4 2- қандай үрдіс?
1) қайта топтасу
2) тотығу
3) тотықсыздану
4) тотығу-тотықсыздану
5) изомерлену
26. Бұл Cl- → ClO3- қандай үрдіс?
1) қайта топтасу
2) тотықсыздану
3) тотығу
4) тотығу-тотықсыздану
5) инверсия
27. Берілген иондардағы NO2-, NO3- азоттың тотығу дәрежесін көрсетіңіз:
1) + 5, + 6
2) + 1, + 2
3) - 3, + 2
4) + 3, + 5
5) + 1, - 1
28. Калий перманганаты бейтарап ортада тотықсызданғанда түзілетін қосылыс құрамындағы марганецтің тотығу дәрежесі қандай болады?
1) + 7
2) + 4
3) + 1
4) - 2
5) + 2
29. Берілген реакцияда FeCl3 + H2S→ FeCl2 + S + HCl тотығу үрдісіне неше электрон қатысады?
1) 4
2) 1
3) 3
4) 5
5) 2
30. Берілген тотығу – тотықсыздану 2Н2 + О2 → 2Н2О реакциясындағы тотықтырғыштың 2 молімен әрекеттесетін тотықсыздандырғыштың массасын табыңыз:
1) 8
2) 6
3) 10
4) 32
5) 16
№ 13 дәріс. Сулы ерітінділердегі тотығу-тотықсыздану реакциялары. Электрохимиялық үрдістер
1. Дәрістің мақсаты:
Электр энергиясының химиялық қайнар көзінің жұмыс істеу принципіне сүйеніп әртүрлі аккумуляторлардың жұмыс істеуін қамтамасыз ететін химиялық реакциялармен студенттерді таныстыру.
2. Дәрістің жоспары:
1. ýëåêòðîäòûқ ïîòåíöèàëäàð òóðàëû òүñiíiê æәíå îëàðäûң ïàéäà áîëó ìåõàíèçìi
2. Ñòàíäàðòòû ñóòåêòiê ýëåêòðîä. Íåðíñò òåңäåói. Ýëåêòðîäòû үрдіñòåðäiң êèíåòèêàñû. Ýëåêòðîõèìèÿëûқ æәíå êîíöåíòðàöèÿëûқ ïîëÿðëåíó
3. Ãàëüâàíèêàëûқ ýëåìåíòòåð. Ýëåêòð қîçғàóøû êүø (ÝҚК) æәíå îíûң өëøåìi.
4.Áàòàðåÿëàð ìåí àêêóìóëÿòîðëàð
3. Дәрістің мазмұны:
ýëåêòðîäòûқ ïîòåíöèàëäàð òóðàëû òүñiíiê æәíå îëàðäûң ïàéäà áîëó ìåõàíèçìi
Әð òүðëi ìåòàëäàðäû áið-áiðiíå òүéiñòiðãåíäå ýëåêòð òîãûíûң ïàéäà áîëóû îíäàғû åðêií ýëåêòðîíäàð ñàíûíûң òåңåñóiíåí áîëàäû.
Ìåòàëë ïëàñòèíêàëàðäû ñóғà áàòûðғàí êåçäå қàíäàé құáûëûñ áîëàòûíûí қàðàñòûðàéûқ. Ìûñàëû, ñóғà ìûðûøòàí æàñàëғàí ïëàñòèíêàíû áàòûðñàқ, îíäà ïîëþñòi ñó ìîëåêóëàëàðû әñåðiíåí ìåòàëë èîíäàðû ïëàñòèíêà áåòiíåí åðiòiíäiãå ãèäðàòòàëғàí èîíäàð òүðiíäå áөëiíiï øûғàäû. Ìұíûң íәòèæåñiíäå åðiòiíäi îң çàðÿäòàëàäû, àë ìåòàëë ïëàñòèíêàäà åðêií ýëåêòðîíäàð ñàíû àðòûï, îë òåðiñ çàðÿäòàëàäû. Ìiíå, îñûëàéøà ìåòàëë ïëàñòèíêà ìåí åðiòiíäi øåêàðàñûíäà қ îñ ýëåêòðëiê қàáàò òүçiëåäi. Áұë ïàéäà áîëғàí қîñ ýëåêòðëiê қàáàò ìåòàëë èîíäàðûíûң ìåòàëäàí îäàí әði áөëiíóií òåæåéäi. Àқûðûíäà ìåòàëë ìåí åðiòiíäi àðàñûíäà òåïå-òåңäiê îðíàéäû:
Ме + т Н2О ↔ Ме(Н2О) п + т + п 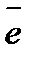
Ìұíûң íåãiçiíäå ìåòàëë ìåí åðiòiíäi øåêàðàñûíäà (æàңàñó бетіíäå) ïîòåíöèàëäàð àéûðûìû áîëàäû, ìұíû êөáiíåñå òåïå-òåңäiê æàғäàéäàғû ýëåêòðîä ïîòåíöèàëû äåï àòàéäû. Åíäi ìåòàëäû ñóғà åìåñ, îñû ìåòàëë òұçûíûң åðiòіíäiñiíå áàòûðñàқ, îíäà áұë åðiòiíäi құðàìûíäà ãèäðàòòàëғàí (ñó ìîëåêóëàñûìåí қîðøàëғàí) èîíäàð áîëғàíäûқòàí òåïå-òåңäiê ñîëғà қàðàé ûғûñàäû, îñûíûң íәòèæåñiíäå ïîòåíöèàë àéûðìàñû àçàÿäû. Àë åðiãåí òұç êîíöåíòðàöèÿñû íåғұðëûì êөáiðåê áîëñà, ïîòåíöèàë àéûðìàñû ñîғұðëûì àç áîëàäû.
Åíäi áåëñåíäiëiãi òөìåí ìåòàëäû, мысалы ìûñòû îñû ìåòàëë èîíû êөï åðiòiíäiãå áàòûðñàқ, îíäà åðiòiíäiãå ìûñ ïëàñòèíêàсы èîíäàð áåðìåéäi, êåðiñiíøå, êàòèîíäàðäûң áið áөëiãiíå өçäåðiíiң ãèäðàòòû қàáûқøàëàðûí áұçûï, åðiòiíäiíi òàñòàï, ìåòàëäûң êðèñòàëäûқ òîðûí æàñàқòàéäû. Ìұíûң íәòèæåñiíäå îëàð ìåòàëäû îң çàðÿäòàï, åðiòiíäiäåãi àíèîíäàðäûң ïàéäà áîëóû íәòèæåñiíäå òåðiñ çàðÿä áåðåäi. Áұë æàғäàéäà äà ñó ìåí ìåòàëë øåêòåñêåí æåðiíäå қîñ ýëåêòðëiê қàáàò ïàéäà áîëûï, ïîòåíöèàëäàð àéûðûìû áîëàäû.
Ñòàíäàðòòû ñóòåêòiê ýëåêòðîä. Íåðíñò òåңäåói. Ýëåêòðîäòû үрдіñòåðäiң êèíåòèêàñû. Ýëåêòðîõèìèÿëûқ æәíå êîíöåíòðàöèÿëûқ ïîëÿðëåíó
Áàéқàëàòûí ïîòåíöèàëäàð àéûðûìûí өëøåéòií òiêåëåé әäiñ æîқ. Әðáið ìåòàëäûң òóғûçàòûí ïîòåíöèàëäàð àéûðûìûí ñóòåê ýëåêòðîäû êөìåãiìåí àíûқòàéäû. Áұë íұñқà áîéûíøà, құðàìûíäà ïðîòîíû áàð åðiòiíäiãå ïëàòèíà ïëàñòèíêàíû îðíàëàñòûðûï, îғàí ñóòåê ãàçûí æiáåðñå, îíäà îíûң áåòiíäå ñóòåê ãàçû àäñîðáöèÿëàíàäû. Îñû àäñîðáöèÿëàíғàí ñóòåê ìîëåêóëàñû ìåí Í- àðàñûíäà ìûíàäàé òåïå-òåңäiê қàëûïòàñàäû:
Н2 ↔2Н++2 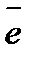
Îñû æүéåíi ñûììåí ìûðûø ñóëüôàò åðiòiíäiñiíå áàòûðûëғàí ìûðûø ïëàñòèíêàсыìåí æàëғàñòûðñàқ, îíäà ýëåêòðîíäàð ìûðûøòàí ñóòåê ýëåêòðîäûíà өòåäi, өéòêåíi ìûðûø ñóòåê ýëåêòðîäûíà қàðàғàíäà òåðiñ çàðÿäòàëғàí. Ñóòåê ýëåêòðîäûның ïîòåíöèàëû 0-ãå òåң äåï àëынàäû. Ýëåêòðîä ïîòåíöèàëûның øàìàñû òåìïåðàòóðàғà, òұçäàðäûң êîíöåíòðàöèÿñûíà, қûñûìғà òәóåëäi болады, ñîíäûқòàí îëàðäû ñòàíäàðòòû æàғäàéäà àíûқòàéäû. Îñû æàғäàéäà àíûқòàëғàí ýëåêòðîä ïîòåíöèàëû ñòàíäàðòòû æàғäàéäàғû ýëåêòðîä ïîòåíöèàëû(Å0) äåï àòàëàäû.
Поиск по сайту: