 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Тест тапсырмалары 25 страница
Åðiòiíäiëåðäiң қàòó òåìïåðàòóðàñûí өëøåóäi êðèîñêîïèÿ, àë қàéíàó òåìïåðàòóðàñûí өëøåóäi ýáóëëèîñêîïèÿ äåéäi.
Áұë әäiñòåðìåí åðiãåí çàòòûң ìîëåêóëàëûқ ìàññàñûí îңàé åñåïòåóãå áîëàäû. Îë үøií Ðàóëü çàңûíûң ìàòåìàòèêàëûқ òүðäå берілген òåңäåóëåðіндегі молялäiê êîíöåíòðàöèÿíûң (Ñ) îðíûíà g/Mr ìәíií қîю керек (Ñ = g/Mr). Ñîíäà æîғàðûäàғû òåңäåуëåð áûëàé æàçûëàäû:
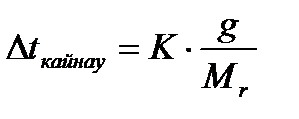
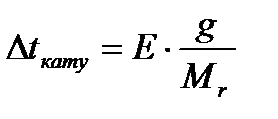
мұíäàғы g – 1000 ã åðiòêiøòå åðiãåí çàòтың ìөëøåði Ìr – еріген заттың ìîëåêóëàëûқ ìàññàсы. Áұë òåңäåóëåðäåí ìîëåêóëàëûқ ìàññàны анықтайды:
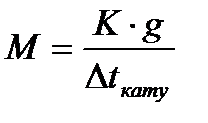
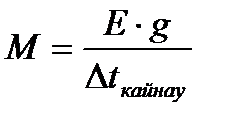
Мîëåêóëàëûқ ìàññàны àíûқòàó үøií òåê қàòó òåìïåðàòóðàñûíûң êåìóií íåìåñå қàéíàó òåìïåðàòóðàñûíûң æîғàðûëàóûí àíûқòàñà áîëғàíû.
4. Бақылау сұрақтары:
1. Осмос дегеніміз не?
2. Диффузия дегеніміз не?
3. Неліктен кейбір заттар ерігенде жылу бөлінеді, ал кейбіреулері ерігенде жылу сіңіріледі?
5. Тест тапсырмалары:
1. Сольваттар дегеніміз не?
1) еріген зат бөлшектерінің еріткіш молекулаларымен араласу қүбылысы
2) еріген заттың еріткішпен әрекеттесуінен түзілген құрамы тұрақты болатын қосылыс
3) еріген зат молекулаларының еріткіш молекулаларына қарай бір бағытта қозғалуы
4) еріген зат бөлшектерінің еріткіш молекулаларымен әрекеттесуінен түзілген құрамы ауыспалы болатын қосылыс
5) еріген зат бөлшектерінің ассоциациялануы,
2. Қандай құбылыс гидраттану деп аталады?
1) тұз иондары мен су бөлшектерінің әрекеттесуі
2) еріген зат бөлшектерінің ерітінді молекулаларымен әрекеттесуі
3) тұз иондарының су молекулаларымен әрекеттесуі
4) еріген зат бөлшектерінің су молекулаларымен әрекеттесуі
5) су молекулаларының бір-бірімен әрекеттесуі
3. Қандай заттар кристаллогидраттар деп аталады?
1) сумен әрекеттесе алатын заттар
2) еріген зат бөлшектерінің еріткіш молекулаларымен әрекеттесуінен түзілген қосылыс
3) еріген зат бөлшектерінің су молекулаларымен әрекеттесуінен түзілген гидраттар
4) тұз иондарының су молекулаларымен әрекеттесуінен түзілген заттар
5) құрамында су молекулалары болатын қатты заттар
4. Заттың еру жылуы дегеніміз не?
1) кез-келген зат ерігенде сіңірілетін жылу мөлшері
2) 1 моль зат ерігенде бөлінетін жылу мөлшері
3) заттың еруі кезінде бөлініп шығатын немесе сіңірілетін жылу мөлшері
4) зат еріген кезде кристалдық торды бұзуға жұмсалатын жылу мөлшері
5) гидраттану кезінде бөлінетін жылу мөлшері
5. Еру кезінде байқалатын жалпы жылу мөлшерін қандай формуламен өрнектейді?
1) ΔН = ΣΔНөнім + ΣΔНбаст.заттар
2) ΔН = ΔG + TΔS
3) ΔН = ΔН2 - ΔН1
4) ΔН = - Q
5) ΔНE = ΔНГ + ΔНК
6. Қаныққан бу деп қандай буды айтады?
1) конденсациялану жылдамдығы булану жылдамдығынан көп болған кездегі бу
2) булану жылдамдығы конденсациялану жылдамдығынан көп болған кездегі бу
3) Еріткіш молекулаларының булану жылдамдығы конденсациялану жылдамдығына теңескен жағдайдағы бу
4) ерітіндінің булану жылдамдығы конденсациялану жылдамдығына тең болған жағдайдағы бу
5) 1000 С температурада қайнаған еріткіш буы
7. Ерітінді бетіндегі еріткіштің қаныққан бу қысымының төмендеуін қалай белгілейді?
1) 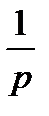
2) 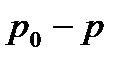
3) 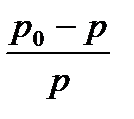
4) С = k·p
5) 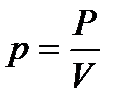
8. Не себебтен калий гидроксиді суда ерігенде жылу бөлінеді?
1) гидраттану жылуы мен кристал торды бұзуға арналған жылудың қосындысы нөльге тең болады
2) гидраттану кезінде бөлінетін жылу мөлшері кристалды бұзуға жұмсалатын жылудан аз болады
3) гидраттану кезінде бөлінетін жылу мөлшері кристалды бұзуға жұмсалатын жылуға тең болады
4) кристалды бұзуға жұмсалатын жылудан гидраттану кезінде бөлінетін жылу мөлшері көп болады
5) гидраттану жылуы мен кристал торды бұзуға арналған жылудың қосындысы нөльден үлкен болады
9. Аммоний нитратын суда еріткенде жылу:
1) бөлінбейді
2) бөлінеді
3) сіңіріледі
4) жұтылмайды
5) алдымен жұтылып кейін бөлінеді
10. Ерітінді бетіндегі еріткіштің қаныққан бу қысымының салыстырмалы төмендеуін қалай белгілейді?
1) 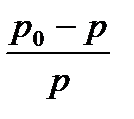
2) 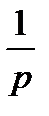
3) 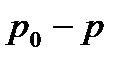
4) С = k·p
5) 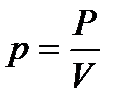
11. Раульдің 1-ші заңының математикалық өрнектелуі:
1) Δtқайнау = ЕС
2) С = k·p
3) 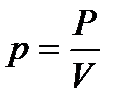
4) Δtқайнау = t1қайнау - tқайнау
5) 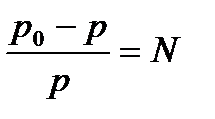
12. Ерітіндінің қайнау температурасының жоғарылауы қай формуламен өрнектеледі?
1) Δtқайнау = t1қайнау + tқайнау
2) Δtқайнау = t1қайнау − tқайнау
3) Δtқайнау = ЕС
4) Δtқайнау = КС
5) Δtқайнау = КС + ЕС
13. Ерітіндінің қату температурасының төмендеуі қай формуламен өрнектеледі?
1) Δtқату = КС
2) Δtқату = t1қату + tқату
3) Δtқату = ЕС
4) Δtқату = t1қату - tқату
5) Δtқату = КС + ЕС
14. Криоскопия дегеніміз не?
1) ерітіндінің қату температурасының температурасына теңелуін
2) ерітіндінің қайнау температурасын өлшеу
3) ерітіндінің қату температурасының төмендеуі
4) ерітіндінің қайнау температурасының жоғарылауы
5) ерітіндінің қату температурасын өлшеу
15. Эбулиоскопия деп нені айтады?
1) ерітіндінің қату температурасын өлшеуді
2) ерітіндінің қайнау температурасын өлшеуді
3) ерітіндінің қату температурасының төмендеуін
4) ерітіндінің қайнау температурасының жоғарылауын
5) ерітіндінің қайнау температурасының қату температурасына теңелуін
16. Эбулиоскопиялық және криоскопиялық тұрақтылар неге тәуелді болады?
1) еріткіштің тегіне
2) ерітіндінің табиғатына
3) еріген заттың табиғатына
4) еріген заттың құрамына
5) ерітіндінің концентрациясына
17. Қандай су кристалдық су деп аталады?
1) кристаллогидратты ерітетін су
2) қатты (кристалдық) затты қайта кристалдауға жұмсалатын су
3) кристаллогидрат құрамындағы су
4) еріген зат бөлшектерін гидраттайтын су
5) тұз иондарын гидролиздейтін су
18. Қай қосылыс кристаллогидратқа жатады?
1) CO2·5H2O
2) Na2SO4+H2O
3) CuSO4·5H2O
4) NH3·3H2O
5) NH3 +3H2O
19. Газдардың еріткіштегі ерігіштігі температура өскен сайын?
1) артады
2) кемиді
3) алдымен артады одан кейін кемиді
4) алдымен кемиді одан кейін артады
5) өзгермейді
20. Қандай құбылыс осмос деп аталады?
1) еріген зат бөлшектерінің су молекулаларымен әрекеттесуі
2) еріген зат молекулаларының ерітінді бойына біртекті таралуы
3) жартылай өткізгіш арқылы өтетін біржақты диффузия
4) ерітінді бетіндегі қаныққан бу қысымының салыстырмалы төмендеуі
5) қаныққан бу қысымының еріген заттың мольдік үлесіне тәуелділігі
21. Қандай құбылысты диффузия деп атайды?
1) қаныққан бу қысымының еріген заттың мольдік үлесіне тәуелділігі
2) жартылай өткізгіш арқылы өтетін біржақты диффузия
3) еріген зат бөлшектерінің су молекулаларымен әрекеттесуі
4) ерітінді бетіндегі қаныққан бу қысымының салыстырмалы төмендеуі
5) еріген зат молекулаларының еріткіш молекулаларының арасына біркелкі таралуы
22. Газдардың еріткіштегі ерігіштігі қысым өскен сайын?
1) өзгермейді
2) алдымен артады одан кейін кемиді
3) кемиді
4) алдымен кемиді одан кейін артады
5) артады
23. Еріген заттың молярлық үлесін қай формуламен анықтайды?
1) 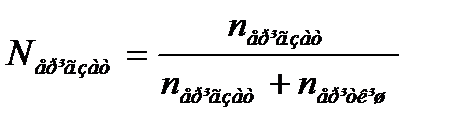
2) 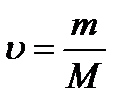
3) 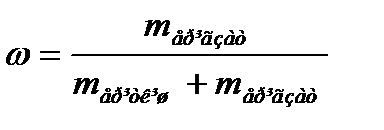
4) 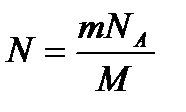
5) N = υNA
24. Генри заңының математикалық өрнегі:
1) N = υNA
2) C = kp
3) 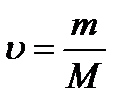
4) Δtқату = t1қату + tқату
5) Δtқату = КС
25. Диффузия:
1) қайтымды процесс
2) өздігінен жүрмейтін құбылыс
3) жоғары температураның әсерінен жүретін құбылыс
4) өздігінен жүретін құбылыс
5) қысымды арттырғанда жүретін құбылыс
26. Раульдің 2-ші заңының математикалық өрнегі:
1) Δtқату = КС Δtқайнау = ЕС
2) С = kp Δp = p0 – p
3) 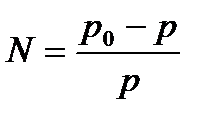
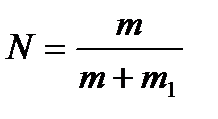
4) Δtқату = t1қату + tқату Δtқайнау = t1қайнау + tқайнау
5) 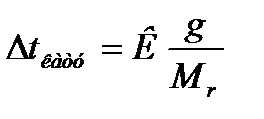
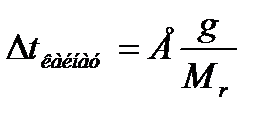
27. Кристалдық торды бұзуға жұмсалатын энергия қалай өрнектеледі?
1) ΔН298
2) ΔНГ
3) ΔНЕ
4) ΔНК
5) ΔН
28. Осмос құбылысы қай уақытта тоқтайды?
1) ерітіндідегі екі жақтың концентрацияларының айырмашылығы артқанда
2) біржақты диффузия құбылысы аяқталғанда
3) ерітіндідегі екі жақтың концентрациялары теңескенде
4) диффузия құбылысы тоқтағанда
5) ерітіндідегі еріген заттың концентрациясы азайғанда
29. Диффузия дегеніміз:
1) молекула аралық байланысты күшейтетін құбылыс
2) ерітіндідегі еріген заттың концентрациясын азайтатын құбылыс
3) ерітіндідегі екі жақтың концентрацияларының айырмашылығын арттыратын құбылыс
4) броундық қозғалысқа кедергі жасайтын құбылыс
5) концентрацияларын теңестіруге әкеп соғатын заттардың өздігінен жүретін қозғалысы, яғни орын ауыстыруы
30. 2,5 г глицеринді 100 г суда еріткенде ерітіндінің қату температурасы 0,506 градусқа төмендеді. Судың криоскопиялық тұрақтысының мәні 1,86. Глицериннің молекулалық массасын табыңыз:
1) 95
2) 92
3) 76
4) 96
5) 90
№ 11 дәріс. Ерітінділердің жалпы қасиеттері. Электролит ерітінділері
1. Дәрістің мақсаты:
Студенттердің электролиттік диссоциация механизмін және тұздар гидролизін терең меңгеруін қалыптастыру
2. Дәрістің жоспары:
1. Åðiãåí çàòòàðäûң ýëåêòðîëèòòiê äèññîöèàöèÿñû. Дèññîöèàöèÿ òұðàқòûñû æәíå äèññîöèàöèÿëàíó äәðåæåñi
2. Êүøòi ýëåêòðîëèòòåð òåîðèÿñû. Èîíäûқ àòìîñôåðà. Áåëñåíäiëiê
3. Ãèäðîëèç
4. Ñóäûң ýëåêòðîëèòòiê äèññîöèàöèÿñû. Ñóòåêòiê êөðñåòêiø (ðÍ)
3. Дәрістің мазмұны:
Áàðëûқ çàòòàð ýëåêòðîëèòòåð æәíå áåéýëåêòðîëèòòåð болып åêi òîïқà áөëiíåäi. Áåéýëåêòðîëèòòåð ñóлû åðiòiíäiëåðäå òåê ìîëåêóëàëàðғà äåéií áөëøåêòåíåäi, àë ìîëåêóëàëàð ýëåêòðîíåéòðàë (бейтарап) áîëғàíäûқòàí ìұíäàé åðiòiíäiëåð ýëåêòð òîãûí өòêiçáåéäi. Áåéýëåêòðîëèòòåðãå қàíò, ãëþêîçà åðiòiíäiëåði ìûñàë áîëà àëàäû. Íåãiçiíåí êîâàëåíòòi áàéëàíûñ àðқûëû òүçiëåòií ìîëåêóëàëàðäàí òұðàòûí çàòòàð áåéýëåêòðîëèòòåðãå æàòàäû.
Ýëåêòðîëèòòåðãå æàòàòûí çàòòàð åðiãåí íåìåñå áàëқûғàí êүéäå ýëåêòð òîãûí өòêiçåäi. Ýëåêòðîëèòòåðãå ìîëåêóëàëàðû ïîëþñòi íåìåñå èîíäû áîëàòûí íåãiçäåð, қûøқûëäàð æәíå òұçäàð æàòàäû.
Ýëåêòðîëèòòåðäiң òàáèғàòûíà æәíå îëàðäûң ìîëåêóëàëàðûíäàғû àòîìäàð àðàñûíäàғû õèìèÿëûқ áàéëàíûñòûң áåðiêòiãiíå áàéëàíûñòû ýëåêòðîëèòòåð әð òүðëi äәðåæåäå èîíäàðғà ûäûðàéäû. Õèìèÿëûқ áàéëàíûñ íåғұðëûì әëñiç áîëñà, ñîғұðëûì ýëåêòðîëèò êөáiðåê èîíäàðғà ûäûðàéäû.
Êүøòi ýëåòðîëèòòåðãå åðiãåí êåçäå èîíäàðғà òîëûғûìåí ûäûðàéòûí çàòòàð æàòàäû: ÍÑ1, HNO3, H2SÎ4, HCIO4, HI, KOH, NaOH æәíå áàðëûқ åðèòií òұçäàð. Әëñiç ýëåêòðîëèòòåðãå èîíäàðғà íàøàð ûäûðàéòûí çàòòàð æàòàäû: Í3ÂÎ3, ÑÍ3ÑÎÎÍ, HCN, Í2S және ò.á. Әëñiç ýëåêòðîëèòòåð åðiãåí кезде олардûң áiðàç бөлігі иондарға ыдырамай ìîëåêóëà êүéiíäå қàëàäû. Êүøòåði îðòàøà ýëåêòðîëèòòåð áîëûï ìûíà çàòòàð ñàíàëàäû: Í2SÎ3, H3PO4 және ò.á.
Åðiãåí çàòòàðäûң ýëåêòðîëèòòiê äèññîöèàöèÿñû. Дèññîöèàöèÿ òұðàқòûñû æәíå äèññîöèàöèÿëàíó äәðåæåñi
Ýëåêòðîëèòòåðäiң қàñèåòòåðií òүñiíäiðó үøií øâåöèÿ ғàëûìû Ñ.Àððåíèóñ 1887 æûëû өçiíiң ýëåêòðîëèòтiê äèññîöèàöèÿ òåîðèÿñûí ұñûíäû. Áұë òåîðèÿ ìûíàäàé íåãiçãi қàғèäàëàðäàí òұðàäû:
1. Ýëåêòðîëèòòåðäiң áàëқûғàí íåìåñå åðiãåí êåçäå èîíäàðғà ûäûðàóû ýëåêòðîëèòòiê äèññîöèàöèÿ äåï àòàëàäû.
2. Ýëåêòðîëèòòåð ñóäà åðiãåíäå îң çàðÿäòàëғàí èîíäàðғà - êàòèîíäàðғà æәíå òåðiñ çàðÿäòàëғàí èîíäàðғà – àíèîíäàðғà ûäûðàéäû.
Поиск по сайту: