 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Принцип Паули
Хорошо известная из курса химии формулировка принципа Паули говорит о том, что в данном атоме или молекуле не может быть двух электронов с четырьмя одинаковыми квантовыми числами. Рассмотрим другую формулировку этого знаменитого принципа, используя некоторые положения квантовой механики. Пусть  – оператор перестановки k-го и j-го электронов, то есть в результате действия такого оператора данные два электрона меняются местами. Так как электроны неразличимы, то
– оператор перестановки k-го и j-го электронов, то есть в результате действия такого оператора данные два электрона меняются местами. Так как электроны неразличимы, то
 (II.110)
(II.110)
поскольку  коммутирует с гамильтонианом, то
коммутирует с гамильтонианом, то  соответствует постоянной движения и
соответствует постоянной движения и  и гамильтониан имеют общие собственные функции. Введем краткое обозначение
и гамильтониан имеют общие собственные функции. Введем краткое обозначение  .
.
Тогда
 , (II.111)
, (II.111)
где 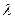 – действительное число, поскольку оператор
– действительное число, поскольку оператор  – эрмитов. Подействуем оператором перестановки два раза подряд на волновую функцию
– эрмитов. Подействуем оператором перестановки два раза подряд на волновую функцию  :
:
 (II.112)
(II.112)
То есть при перестановке двух одинаковых частиц решение стационарного уравнения Шредингера может либо изменять знак, либо нет. Состояния, при которых  меняет, знак называются антисимметричными. Согласно принципу Паули волновые функции систем, состоящих из электронов, являются антисимметричными. В этом и заключается его смысл в квантовой механике.
меняет, знак называются антисимметричными. Согласно принципу Паули волновые функции систем, состоящих из электронов, являются антисимметричными. В этом и заключается его смысл в квантовой механике.
Поиск по сайту: