 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Атомно-молекулярное учение
Атом - наименьшая электронейтральная частица химического элемента, являющаяся носителем его химических свойств и состоящая из положительно заряженного ядра и электронной оболочки.
Бертоллиды – вещества переменного состава.
Валентность – мера способности атома присоединять или замещать другие атомы или группы атомов при образовании химических связей. За единицу принята валентность атома водорода.
Дальтониды – вещества постоянного состава.
Закон Авогадро: в равных объемах различных газов при одинаковых температуре и давлении содержится одинаковое число молекул.
Закон постоянства состава: индивидуальное химическое вещество молекулярного строения имеет постоянный качественный и количественный состав, не зависящий от способа его получения.
Закон сохранения массы вещества: сумма масс продуктов реакции равна сумме масс веществ, вступивших во взаимодействие.
Закон эквивалентов: массы реагирующих веществ прямопропорциональны их эквивалентным массам.
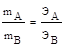
Молекулярная частица - наименьшая устойчивая совокупность взаимосвязанных атомных частиц, являющаяся носителем химических свойств вещества.
Относительная атомная масса - отношение массы атома к 1/12 массы атома углерода изотопа 12С.
Относительная молекулярная масса - отношение среднеизотопической массы молекулы, вычисленной с учетом естественного природного содержания изотопов, к 1/12 массы атома углерода изотопа 12C.
Моль - количество вещества, содержащее столько структурных или формульных единиц, сколько атомов содержится в 12 г углерода изотопа 12С.
Молярная масса – масса одного моля вещества.
Уравнение состояния идеального газа:
 ,
,
где m - масса газа (г или кг), М – его молярная масса (г/моль или кг/моль), р – давление (Па или кПа), V – объем (м3 или л), Т – абсолютная температура (К), R – универсальная газовая постоянная (8,314 Дж/моль×К).
Формульная единица вещества - простейшее соотношение между составляющими его элементами (брутто-формула).
Формульная масса – масса моля формульных единиц.
Химический элемент – совокупность атомов с одинаковым заряда ядра.
Число Авогадро – это число структурных элементов или формульных единиц в моле вещества (NA = 6,022×1023 моль-1).
Эквивалент - это реальная или условная частица, отдающая или присоединяющая один катион водорода в реакциях кислотно-основного взаимодействия, один электрон в окислительно-восстановительных реакциях или взаимодействующая с одним эквивалентом любого другого вещества в реакциях обмена.
Эквивалентная масса вещества - это молярная масса его эквивалента.
Поиск по сайту: