 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Номенклатура координационных соединений
При построении названий координационных соединений рекомендуется пользоваться системой, предложенной Комитетом по номенклатуре химических соединений Международного Союза по теоретической и прикладной химии (IUPAC). Основные положения номенклатуры IUPAC для координационных соединений можно сформулировать следующим образом:
1. Для координационных соединений, как и в случае простых соединений, первым называют анион в именительном падеже, а затем катион в родительном падеже (русскоязычный вариант системы).
2. При построении названия комплексной частицы сначала перечисляют лиганды, после чего называют центральный атом.
3. Лиганды перечисляются в алфавитном порядке. Если название аниона заканчивается на -ат или -ит (сульфат, сульфит и т.д.), то к названию добавляется суффикс "о"; в случае анионов, оканчивающихся на -ид (хлорид, цианид, гидроксид), суффикс "о" добавляется к корню названия аниона (например, сульфато-, сульфито-, но хлоро-, циано-, гидроксо-). Исключением является гидрид-анион Н-, называемый гидридо-. Ион NO 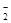 называют "нитро-", если он координируется через атом азота, и "нитрито-", если он присоединяется через атом кислорода. Названия нейтральных молекул пишут без изменений и заключают в круглые скобки, даже если в комплекс входит одна молекула лиганда. Лишь для некоторых молекул приняты специальные названия: Н2О - аква, NH3 - аммин, CO - карбонил, NO - нитрозил; для этих лигандов круглые скобки при названии единичных молекул опускаются. Число одинаковых лигандов в комплексе указывают числовыми приставками греческого алфавита (ди-, три-, тетра- и т.д.). Если в названии лиганда уже есть числовые приставки, то следует использовать второй ряд приставок: бис-, трис-, тетракис-. Например, если в комплекс входят две молекулы диметиламина, их следует назвать бис(диметиламин), а не ди(диметиламин).
называют "нитро-", если он координируется через атом азота, и "нитрито-", если он присоединяется через атом кислорода. Названия нейтральных молекул пишут без изменений и заключают в круглые скобки, даже если в комплекс входит одна молекула лиганда. Лишь для некоторых молекул приняты специальные названия: Н2О - аква, NH3 - аммин, CO - карбонил, NO - нитрозил; для этих лигандов круглые скобки при названии единичных молекул опускаются. Число одинаковых лигандов в комплексе указывают числовыми приставками греческого алфавита (ди-, три-, тетра- и т.д.). Если в названии лиганда уже есть числовые приставки, то следует использовать второй ряд приставок: бис-, трис-, тетракис-. Например, если в комплекс входят две молекулы диметиламина, их следует назвать бис(диметиламин), а не ди(диметиламин).
4. После перечисления лигандов называют центральный атом. При этом в случае катионных комплексов используют русское название элемента без дополнительных суффиксов, а в случае анионных комплексов - корень латинского названия элемента с суффиксом -ат. После названия центрального атома в круглых скобках римской цифрой записывают степень окисления этого атома (число Штока). Если степень окисления элемента очевидна, число Штока можно и не приводить.
5. Если координационное соединение является неэлектролитом, его называют как катион, но в именительном падеже.
Ниже приведены примеры названий координационных соединений по номенклатуре IUPAC.
[Pt(NH3)6]Cl4 - хлорид гексаамминплатины(IV);
[Cr(H2O)6]Cl3 - хлорид гексааквахрома(III); 
Li[AlH4] - тетрагидридоалюминат лития
K4[Fe(CN)6] - гексацианоферрат(II) калия;
[Co(H2N(CH2)2NH2)2Cl2]NO3 - нитрат дихлоробис(этилендиамин)кобальта(III);
K[Co(NO)(CO)2(CN)] - цианодикарбонилнитрозилкобальтат(0) калия;
[Cu(NH3)4][PtCl4] - тетрахлороплатинат(II) тетраамминмеди(II);
[Pt(NH3)2Cl2] - дихлородиамминплатина.
Поиск по сайту: