 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Энтропия. В классической механике и электродинамике мы привыкли к тому, что невозможность какого-то процесса, как правило
В классической механике и электродинамике мы привыкли к тому, что невозможность какого-то процесса, как правило, связана с каким-то законом сохранения (энергии, импульса, электрического заряда и т. п.). Почему же невозможен вечный двигатель второго рода? Казалось бы, он не нарушает никаких законов сохранения? Чтобы понять это, надо обратиться еще к одной функции состояния системы - к энтропии.
Путь к этой новой для нас функции состояния недолог: надо взять уравнение первого начала термодинамики

и разделить его обе части на температуру. Прежде всего учтем, что
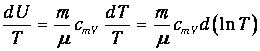
Далее в формуле для элементарной работы

выразим объем через давление и температуру из уравнения состояния идеального газа:
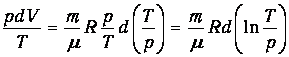
Получим в итоге с использованием соотношения Майера между молярными теплоемкостями

следующее выражение
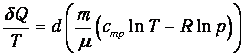
| (5.17) |
Правая часть (5.34) представляет собой дифференциал некоторой функции S состояния системы:

| (5.18) |
где S0 - постоянная интегрирования, не зависящая от термодинамических параметров системы (давления, объема, температуры). Эта функция S называется энтропией. Получилось так, что величина dQ, не являющаяся дифференциалом какой-либо функции состояния, при делении на T стала таковым:

При замкнутом обратимом цикле изменение любой функции состояния (в частности, энтропии) равно нулю:

| (5.19) |
Знак криволинейного интеграла означает, что интегрирование ведется по замкнутому контуру.
Проверим выполнение (5.19) на примере цикла Карно. Поскольку в этом цикле тепло получается системой и отдается только на изотермах (Т1,2=const), температуру можно вынести из-под знака интеграла, и тогда интегрирование даст просто количество теплоты, поделенное на температуру, при которой оно получается или отдается. И действительно, выше было найдено, что на изотермических ветвях цикла при температуре Т1 газ получает теплоту

а при температуре Т2 - отдает теплоту

Выполнение равенства

теперь очевидно. Напомним, что получаемое тепло имеет положительный знак, а отдаваемое - отрицательный; мы же определили ранее Q2 как абсолютную величину отдаваемого тепла, поэтому в формуле появился знак «-».
Проделаем теперь похожие выкладки с произвольным обратимым циклом. Выделим в нем две части: знаком «+» обозначим те фазы процесса, когда система получает тепло, а знаком «-» фазы, когда система отдает тепло. Поскольку полный интеграл равен нулю, аналогичные интегралы по двум частям цикла равны между собой:

| (5.20) |
Если обозначить через Т1 максимальную температуру в первой части цикла, то неравенство Т < Т1 влечет за собой неравенство

где Q1 как и прежде означает полное количество теплоты, полученное системой. Если ввести минимальную температуру Т2 во второй части цикла, то из Т > Т2 следует
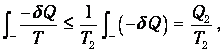
где Q2 - количество теплоты, отданное системой. Из этих неравенств и соотношения (5.20) следует, что

| (5.21) |
Наконец получаем неравенство для КПД цикла

| (5.22) |
С помощью понятия энтропии мы получили иным путем тот же результат: КПД любого замкнутого цикла не превышает КПД цикла Карно.
Таким образом, мы убедились, что новая функция состояния - энтропия - связана со вторым началом термодинамики. До сих пор мы ограничивались равновесными (обратимыми) процессами. Рассмотрим пример неравновесного процесса. Пусть в начальном состоянии имеются два одинаковых идеальных газа с равными массами m при одинаковой температуре Т, но разных давлениях р1 и р2. Определим изменение энтропии DS при соединении сосудов с газом.
В первый момент после соединения сосудов, когда газы еще не смешались, энтропия системы равна сумме энтропии газов в отдельных сосудах:

| (5.23) |
Найдем теперь объемы сосудов:
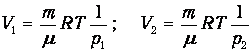
После соединения сосудов масса газа становится равной 2т, а объем - V=V1+V2. Значит, давление р после соединения сосудов равно

| (5.24) |
Поэтому энтропия газа после соединения сосудов равна

| (5.25) |
Изменение энтропии следует из (5.23) и (5.25):

| (5.26) |
Под знаком логарифма стоит величина, всегда большая единицы. Стало быть, энтропия увеличилась: DS>0.
Цель этого примера прежде всего состоит в том, чтобы на частном случае продемонстрировать, как работает закон возрастания энтропии:
| Если замкнутая система в некоторый момент времени находится в неравновесном состоянии, то процессы, протекающие в ней, приводят к возрастанию энтропии, которая достигнет максимума, когда система приходит в равновесие. |
После того как мы смешали газы и получили неравновесное состояние с энтропией, равной сумме энтропии, давления стали выравниваться, и энтропия возросла.
Поиск по сайту: