 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
ЛЕКЦІЯ № 16
Тема: Лікарські засоби групи гліцидів.
ПЛАН
· Загальна характеристика гліцидів.
· Глюкоза.
· Кальцію глюконат.
Гліциди (вуглеводи) – група органічних сполук, що складаються з вуглецю, водню та кисню. Більшість з них відповідають загальній формулі Сm(H2O)n. За хімічними властивостями гліциди – це полігідроксильні сполуки, що містять або утворюють під час гідролізу альдегідну або кетонну групи.
Гліциди (вуглеводи) класифікують:
· За кількістю атомів вуглецю в молекулі – тетрози, пентози, гексози, гептози та ін.;
· За основною функціональною групою – альдози і кетози;
· За кількістю атомів у циклі (для циклічних структур) – фуранози і піранози;
· За кількістю моносахаридних одиниць у молекулі – прості вуглеводи (моносахариди, монози), олігосахариди (від 2 до 10 моносахаридів) і плісахариди (понад 10 моносахаридів).
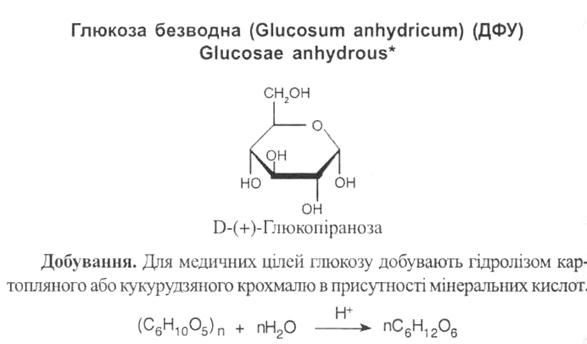
Очищають глюкозу перекристалізацією з водних або водно-спиртових розчинів, причому, якщо кристалізацію вести при температурі понад 30ºС – отримують безводну глюкозу, а при температурі нижчій від 30ºС – кристалогідрат, що містить одну молекулу води: C6H12O6. H2O.
Властивості: білий кристалічний порошок солодкого смаку, легко розчинний у воді, помірно – у 96% спирті.
І дентифікація:
Питоме обертання від + 52,5º до + 53,3º у перерахунку на суху речовину. Визначення проводять для 10% водного розчину в присутності розчину аміаку.
Для глюкози є характерним явище мутаротації, тобто зміни з часом кута обертання свіжовиготовлених розчинів вуглеводів. Для прискорення встановлення рівноваги як каталізатор додають декілька крапель розчину аміаку.
Тонкошарова хроматографія.
При нагріванні субстанції з розчином мідно-тартратного реактиву (реактив Фелінга) утворюється червоний осад, крім реактиву Фелінга для окиснення глюкози може бути використаний аміачний розчин срібла нітрату та реактив Несслера:
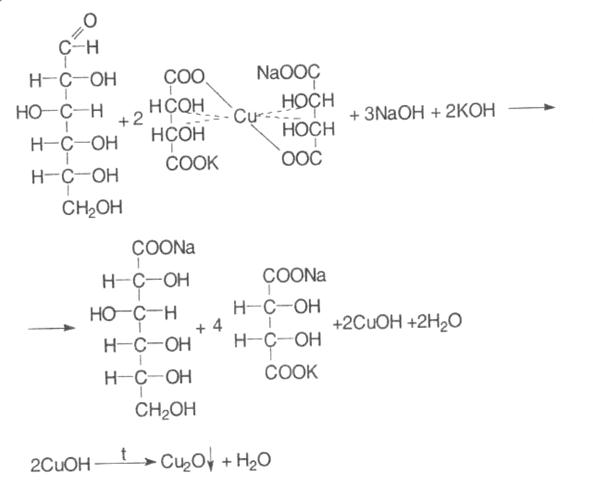
З фенілгідразином глюкоза утворює осад фенілгідразону, який при нагріванні утворює озазон жовтого кольору з характерною температурою топлення:
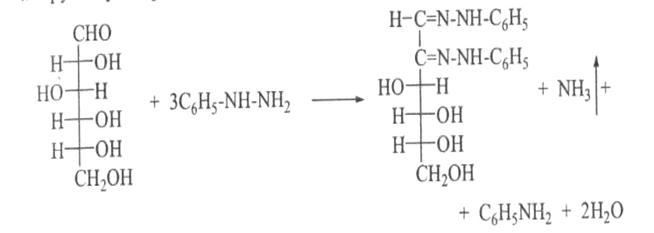
При взаємодії з мінеральними кислотами та кислотою щавлевою при нагріванні глюкоза утворює оксиметилфурфурол:
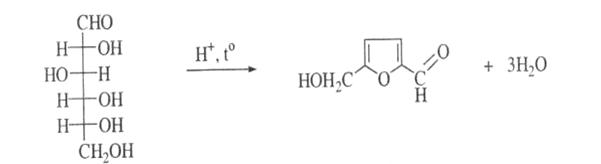
Оксиметилфурфурол – летка сполука, яка взаємодіє з аналіном або новокаїном, нанесеним на фільтрувальний папір, котрим закривають пробірку. Спочатку утворюється основа Шиффа світло-жовтого кольору, а потів фурановий цикл розкривається з утворенням поліметинового барвника, що має малиново-фіолетове забарвлення.
Експрес–реакція:
· з тимолом та кислотою сірчаною концентрованою утворюється темно-червоне забарвлення;
· при взаємодії з резорцином і кислотою хлористоводневою розведеною – при нагріванні до кипіння з’являється рожеве забарвлення.
Кількісне визначення: ДФУ не передбачає визначення кількісного вмісту глюкози в субстанції. Вміст глюкози в розчинах для ін’єкцій визначають:
· методом рефрактометрії;
· поляриметрія;
· йодометрія, зворотне титрування, індикатор крахмаль, s = 1.
До субстанції додають надлишок титрованого розчину йоду і розчин натрію гідроксиду:

Через 10-15 хвилин додають розчин кислоти сірчаної і надлишок йоду відтитровують натрію тіосульфатом:
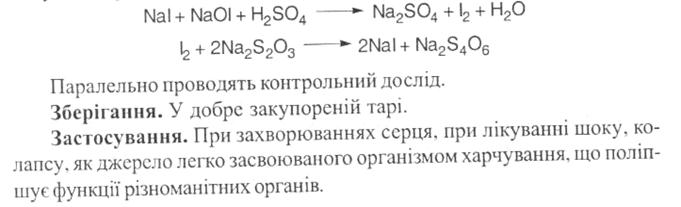

Властивості: білий кристалічний порошок, помірно розчинний у воді, легко розчинний у киплячій воді.
Ідентифікація:
· Метод тонкошарової хроматографії.
· Субстанція дає реакції на кальцій з оксалатом амонію утворюється білий осад.

· З гліоксальгідроксианілом в присутності натрію гідроокису, натрію карбонату та хлороформу. Хлороформний шар при струшуванні набуває червоного кольору:
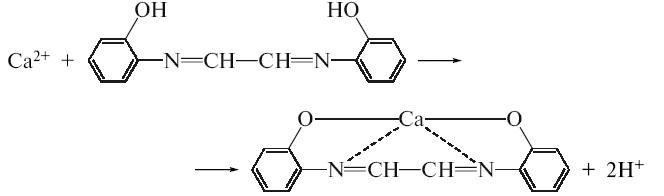
· З розчином хлориду заліза утворюється ясно-зелене забарвлення

(на глюконат-йон).
Кількісне визначення:
Метод комплексонометрії, в присутності аміачного буферного розчину, індикатор кислотний хром чорний спеціальний або кальконкарбонова кислота, титрують розчином едетату натрію від червоно-фіолетового до синього забарвлення, s = 1.
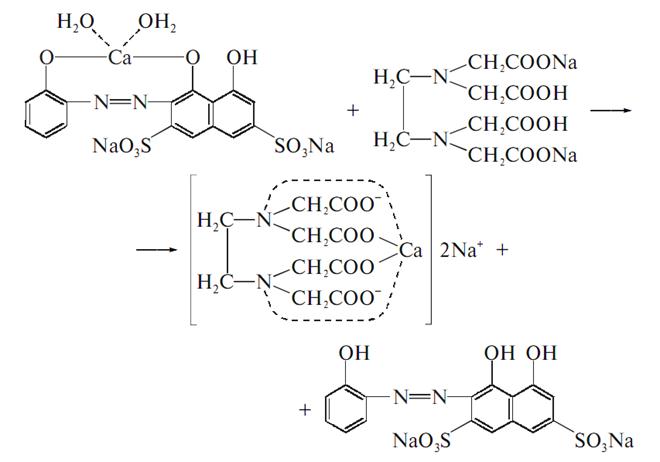
Зберігання: у добре укупореній тарі.
Застосування: є аналогом кальцію хлориду, антиалергійний, протизапальний, кровоспинний засіб.
Поиск по сайту: