 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Второй и третий законы термодинамики
Назовем термодинамическую систему изолированной, если она не обменивается с внешней средой ни энергией, ни веществом. Из определения энтропии по Больцману (25.2) видно, что энтропия изолированной системы при равновесных обратимых процессах остается постоянной и равна максимальному значению:
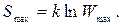
Это видно и из определения энтропии по Клаузиусу (25.7). При 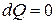
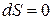 , т. е. S = const.
, т. е. S = const.
При необратимом процессе, когда изолированная система переходит из неравновесного состояния в равновесное, энтропия системы возрастает. Действительно, так как

то из неравенства
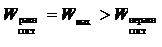
видно, что
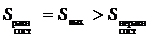
Возрастание энтропии при необратимом процессе видно и из выражения (25.8). При 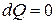
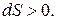
Из вышесказанного следует, что энтропия изолированной системы может только возрастать:
 (26.1)
(26.1)
Это утверждение называют законом возрастания энтропии или вторым законом термодинамики.
При температуре 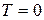 любая система находится в основном состоянии, термодинамическая вероятность которого
любая система находится в основном состоянии, термодинамическая вероятность которого 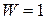 . При этом
. При этом
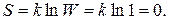
Отсюда можно сказать, что энтропия всякой системы стремится к нулю при стремлении к нулю температуры:
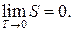 (26.2)
(26.2)
Это утверждение называют теоремой Нериста или третьим законом термодинамики.
Поиск по сайту: