 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Внутренняя энергия реального газа
Выражение для внутренней энергии идеального газа
 |
(30.1)
было получено без учета взаимодействия молекул. Для реального газа в выражении (30.1) необходимо прибавить потенциальную энергию П взаимодействия молекул газа:
 |
(30.2)
Потенциальная энергия П обусловлена силами межмолекулярного взаимодействия молекул. Найдем П для газа, удовлетворяющего уравнение Ван-дер-Вальса. При увеличении объема от 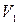 до
до 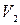 газ совершает работу против сил взаимного притяжения молекул
газ совершает работу против сил взаимного притяжения молекул
 |
(30.3)
где P доп — дополнительное давление, испытываемое газом вследствие сил межмолекулярного притяжения. Подставляя формулу (29.3) в выражениях (30.3) и интегрируя, имеем
 |
(30.4)
Так как эта работа идет на приращение потенциальной энергии взаимодействия молекул  можем написать
можем написать
 |
(30.5)
Сравнивая соотношение (30.4) и (30.5), получаем выражение для потенциальной энергии взаимодействия молекул:
 |
(30.6)
Подставляя формулу (30.6) в соотношение (30.2), получаем выражение для внутренней энергии газа:
 |
(30.7)
ЭКЗАМЕНАЦИОННЫЕ ВОПРОСЫ 2
1. Уравнение состояния идеального газа.
2. Внутренняя энергия идеального газа.
3. Распределение Максвелла.
4. Барометрическая формула.
5. Распределение Больцмана.
6. Явления переноса.
7. Первый закон термодинамики.
8. Теплоемкость идеального газа при постоянном объеме.
9. Теплоемкость идеального газа при постоянном давлении.
10. Адиабатический процесс.
11. Энтропия.
12. Второй и третий законы термодинамики.
13. Силы межмолекулярного взаимодействия в реальных газах.
14. Уравнение Ван-дер-Ваальса.
15. Внутренняя энергия реального газа.
Поиск по сайту: